¿Alguna vez te has preguntado por qué la sal se... Mostrar más
Tipos de Enlaces Químicos Explicados










Tipos de enlace químico
Los átomos se unen mediante fuerzas eléctricas para formar sustancias estables. Piensa en ello como diferentes tipos de "pegamento" que mantienen unida la materia que te rodea.
Existen tres tipos principales: enlace iónico (entre metales y no metales), enlace covalente (entre no metales) y enlace metálico (entre metales). La clave está en la electronegatividad - básicamente, lo "egoístas" que son los átomos con sus electrones.
Por ejemplo, el sodio (Na) y el flúor (F) forman un enlace iónico porque tienen electronegatividades muy diferentes. El bromo consigo mismo forma enlace covalente porque ambos átomos son idénticos.
¡Truco! Memoriza: Metal + No metal = Iónico; No metal + No metal = Covalente; Metal + Metal = Metálico

Configuraciones electrónicas en compuestos
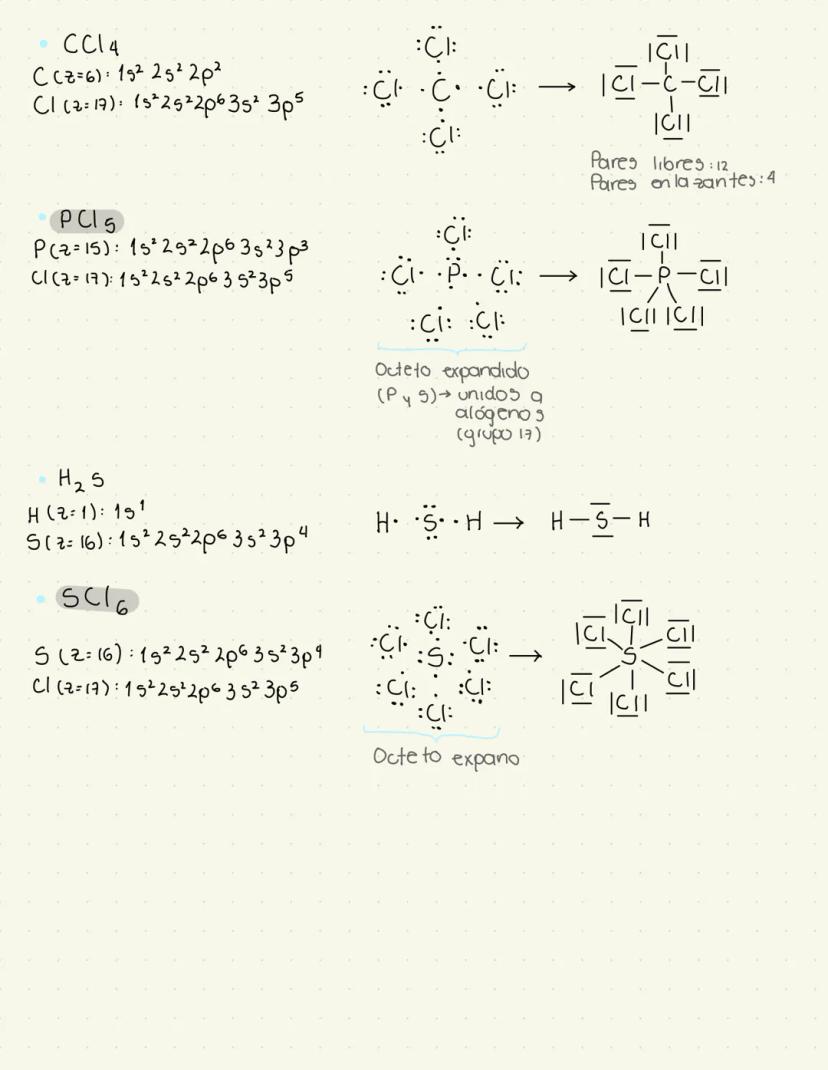
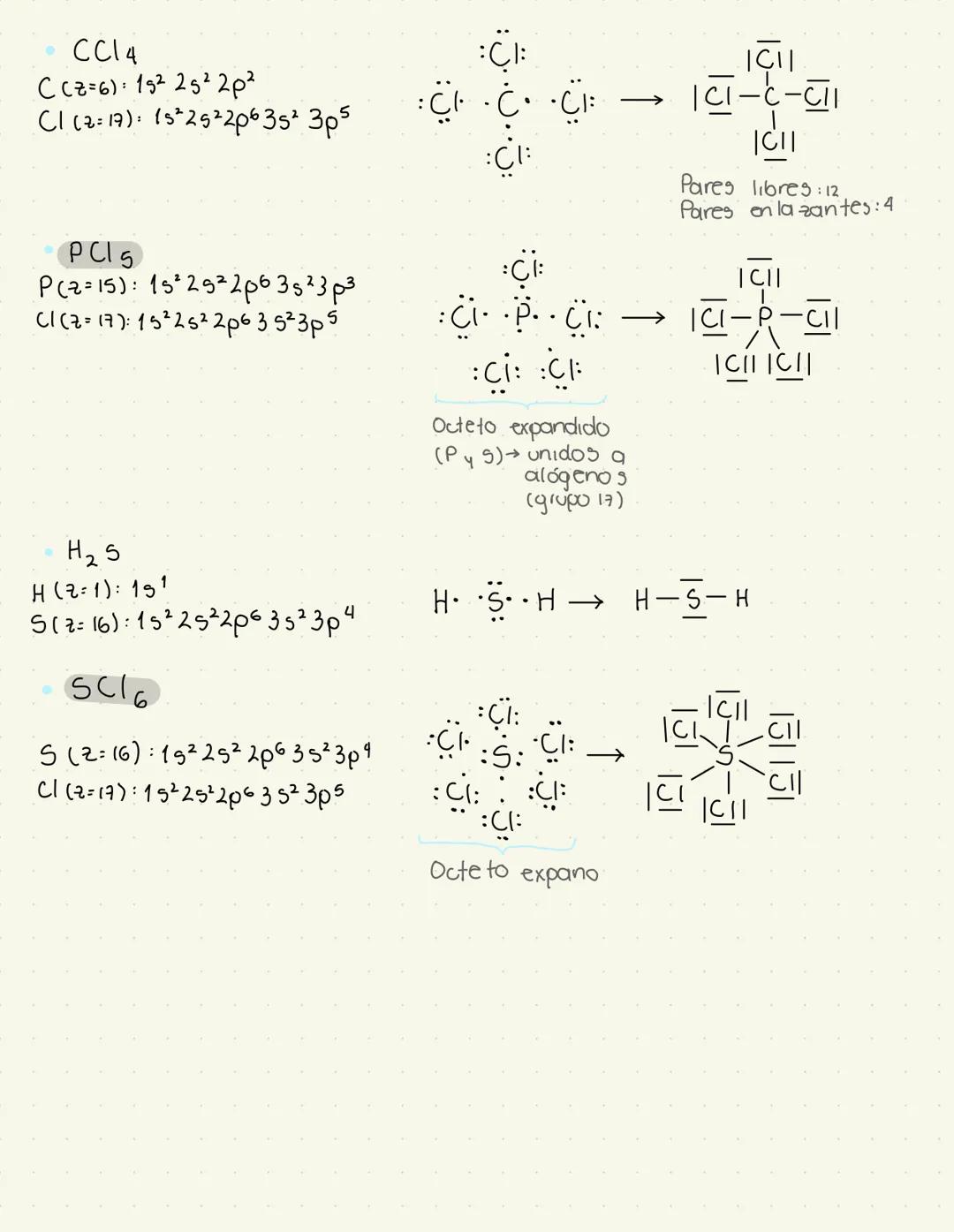
Aquí tienes las configuraciones electrónicas de elementos comunes que aparecen en exámenes. Estas te ayudan a predecir cómo se comportarán los átomos al formar enlaces.
El carbono (C) con 6 electrones puede formar hasta 4 enlaces, como en el CCl₄. El cloro (Cl) con 17 electrones tiende a ganar un electrón para completar su última capa.
Memorizar estas configuraciones te facilitará mucho resolver ejercicios de enlace químico. Son patrones que se repiten constantemente en química.
¡Dato curioso! El número atómico (z) te dice exactamente cuántos electrones tiene un átomo neutro

Enlace iónico: cuando los opuestos se atraen
Los compuestos iónicos se forman cuando los metales "regalan" electrones a los no metales. Es como un intercambio: uno pierde, otro gana, y ambos quedan contentos.
Estos compuestos forman redes cristalinas - estructuras tridimensionales súper ordenadas donde millones de iones se organizan perfectamente. Piensa en la sal de cocina: cada granito es en realidad un cristal microscópico.
La fórmula que escribimos (como NaCl) es una fórmula empírica - no te dice cuántos átomos hay exactamente, sino la proporción más simple entre ellos.
¡Importante! Los compuestos iónicos siempre son sólidos a temperatura ambiente debido a sus enlaces súper fuertes

Propiedades de los compuestos iónicos
Los compuestos iónicos tienen características muy específicas que los distinguen. Son duros (difíciles de rayar) pero frágiles (fáciles de romper) - como el cristal de una ventana.
Tienen puntos de fusión y ebullición elevados porque necesitas muchísima energía para romper esos enlaces tan fuertes. Por eso la sal no se derrite aunque esté al sol todo el día.
Se disuelven genial en disolventes polares como el agua. Cuando echas sal al agua, los iones se separan y se rodean de moléculas de agua.
¡Clave para exámenes! Los compuestos iónicos NO conducen electricidad en estado sólido, pero SÍ cuando están fundidos o disueltos

Conductividad eléctrica: todo sobre el movimiento
Para que algo conduzca electricidad necesitas dos cosas: cargas eléctricas (iones o electrones) y que esas cargas puedan moverse libremente.
En estado sólido, los iones están "atrapados" en la red cristalina - tienen carga pero no pueden moverse. En estado fundido o disuelto, los iones pueden moverse libremente y ¡zas! - conducen electricidad.
Los metales como el hierro (Fe) conducen siempre porque sus electrones están en un "mar de electrones" que se mueve libremente. Los compuestos covalentes como el agua (H₂O) normalmente no conducen.
¡Truco de examen! Si te preguntan por conductividad, siempre menciona: "¿Tiene cargas?" y "¿Pueden moverse?"
Enlace covalente: compartir es vivir
Los enlaces covalentes se forman cuando dos no metales "comparten" electrones. Es el enlace más fuerte de todos - estos átomos no se sueltan fácilmente.
La mayoría forman moléculas (entidades separadas), pero hay tres excepciones importantes que forman redes: el diamante (C), el grafito (C) y la sílice (SiO₂). Estas son súper duras y resistentes.
En las moléculas, la fórmula te dice exactamente cuántos átomos hay (H₂O tiene 2 hidrógenos y 1 oxígeno). En las redes, solo te da la proporción más simple.
¡Recuerda! Los compuestos covalentes pueden ser gases, líquidos o sólidos a temperatura ambiente

Fuerzas intermoleculares: las conexiones débiles
Las moléculas se atraen entre sí mediante fuerzas intermoleculares - mucho más débiles que los enlaces, pero importantes para las propiedades físicas.
Las fuerzas de Van der Waals aparecen en todos los compuestos moleculares. Cuanto más polar y pesada sea la molécula, más fuertes son estas fuerzas y mayores son los puntos de fusión y ebullición.
Los puentes de hidrógeno son especiales - solo aparecen cuando el hidrógeno está unido a N, O o F. Son más fuertes que las fuerzas de Van der Waals y explican por qué el agua tiene propiedades tan únicas.
¡Dato interesante! Los puentes de hidrógeno son los responsables de que el ADN mantenga su estructura de doble hélice

Enlace metálico: el mar de electrones
El enlace metálico es como un club exclusivo de metales. Los átomos metálicos pierden sus electrones de valencia, que quedan flotando en un "mar de electrones" compartido por todos.
Esta estructura especial explica por qué los metales conducen electricidad incluso en estado sólido - los electrones pueden moverse libremente por toda la estructura.
Los metales son dúctiles (se hacen hilos), maleables (se hacen láminas) y generalmente duros. Pueden deformarse sin romperse porque las capas de átomos pueden deslizarse unas sobre otras.
¡Aplicación real! Gracias al enlace metálico puedes cargar tu móvil - los cables de cobre conducen la electricidad perfectamente


Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: Resonancia Magnética Nuclear (NMR)
9Leyes fundamentales de la química
Resumen
Formulario MAS (movimiento armónico simple)
Formulario para ejercicios
Fórmulas Campo magnético e inducción electromagnética
Formulario Campo magnéticoinducción electromagnétic
Disoluciones y gases química 1° Bach
Tema 5: Leyes fundamentales de la química. Tema 6: Disoluciones y gases. Teoría y fórmulas de las disoluciones y de los gases.
Fórmulas Campo Eléctrico
Formularo de campo eléctrico
Mol y masas molares.
-la masa molecular relativa, composición centesimal, moles, leyes, teoría cinético molecular
Termoquímica
Resumen de termoquímica con ejercicios
GRAVITACIÓN FÍSICA 2BACH
contenido PAU y 2 Bachillerato física
Modelos atómicos
Apuntes modelos atómicos física y química teoría de los diferentes modelos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Tipos de Enlaces Químicos Explicados
¿Alguna vez te has preguntado por qué la sal se disuelve en agua pero el aceite no? Todo se debe a los enlaces químicos, las fuerzas invisibles que mantienen unidos a los átomos. Dominar este tema te ayudará a... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tipos de enlace químico
Los átomos se unen mediante fuerzas eléctricas para formar sustancias estables. Piensa en ello como diferentes tipos de "pegamento" que mantienen unida la materia que te rodea.
Existen tres tipos principales: enlace iónico (entre metales y no metales), enlace covalente (entre no metales) y enlace metálico (entre metales). La clave está en la electronegatividad - básicamente, lo "egoístas" que son los átomos con sus electrones.
Por ejemplo, el sodio (Na) y el flúor (F) forman un enlace iónico porque tienen electronegatividades muy diferentes. El bromo consigo mismo forma enlace covalente porque ambos átomos son idénticos.
¡Truco! Memoriza: Metal + No metal = Iónico; No metal + No metal = Covalente; Metal + Metal = Metálico

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Configuraciones electrónicas en compuestos
Aquí tienes las configuraciones electrónicas de elementos comunes que aparecen en exámenes. Estas te ayudan a predecir cómo se comportarán los átomos al formar enlaces.
El carbono (C) con 6 electrones puede formar hasta 4 enlaces, como en el CCl₄. El cloro (Cl) con 17 electrones tiende a ganar un electrón para completar su última capa.
Memorizar estas configuraciones te facilitará mucho resolver ejercicios de enlace químico. Son patrones que se repiten constantemente en química.
¡Dato curioso! El número atómico (z) te dice exactamente cuántos electrones tiene un átomo neutro

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace iónico: cuando los opuestos se atraen
Los compuestos iónicos se forman cuando los metales "regalan" electrones a los no metales. Es como un intercambio: uno pierde, otro gana, y ambos quedan contentos.
Estos compuestos forman redes cristalinas - estructuras tridimensionales súper ordenadas donde millones de iones se organizan perfectamente. Piensa en la sal de cocina: cada granito es en realidad un cristal microscópico.
La fórmula que escribimos (como NaCl) es una fórmula empírica - no te dice cuántos átomos hay exactamente, sino la proporción más simple entre ellos.
¡Importante! Los compuestos iónicos siempre son sólidos a temperatura ambiente debido a sus enlaces súper fuertes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades de los compuestos iónicos
Los compuestos iónicos tienen características muy específicas que los distinguen. Son duros (difíciles de rayar) pero frágiles (fáciles de romper) - como el cristal de una ventana.
Tienen puntos de fusión y ebullición elevados porque necesitas muchísima energía para romper esos enlaces tan fuertes. Por eso la sal no se derrite aunque esté al sol todo el día.
Se disuelven genial en disolventes polares como el agua. Cuando echas sal al agua, los iones se separan y se rodean de moléculas de agua.
¡Clave para exámenes! Los compuestos iónicos NO conducen electricidad en estado sólido, pero SÍ cuando están fundidos o disueltos

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Conductividad eléctrica: todo sobre el movimiento
Para que algo conduzca electricidad necesitas dos cosas: cargas eléctricas (iones o electrones) y que esas cargas puedan moverse libremente.
En estado sólido, los iones están "atrapados" en la red cristalina - tienen carga pero no pueden moverse. En estado fundido o disuelto, los iones pueden moverse libremente y ¡zas! - conducen electricidad.
Los metales como el hierro (Fe) conducen siempre porque sus electrones están en un "mar de electrones" que se mueve libremente. Los compuestos covalentes como el agua (H₂O) normalmente no conducen.
¡Truco de examen! Si te preguntan por conductividad, siempre menciona: "¿Tiene cargas?" y "¿Pueden moverse?"

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace covalente: compartir es vivir
Los enlaces covalentes se forman cuando dos no metales "comparten" electrones. Es el enlace más fuerte de todos - estos átomos no se sueltan fácilmente.
La mayoría forman moléculas (entidades separadas), pero hay tres excepciones importantes que forman redes: el diamante (C), el grafito (C) y la sílice (SiO₂). Estas son súper duras y resistentes.
En las moléculas, la fórmula te dice exactamente cuántos átomos hay (H₂O tiene 2 hidrógenos y 1 oxígeno). En las redes, solo te da la proporción más simple.
¡Recuerda! Los compuestos covalentes pueden ser gases, líquidos o sólidos a temperatura ambiente

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fuerzas intermoleculares: las conexiones débiles
Las moléculas se atraen entre sí mediante fuerzas intermoleculares - mucho más débiles que los enlaces, pero importantes para las propiedades físicas.
Las fuerzas de Van der Waals aparecen en todos los compuestos moleculares. Cuanto más polar y pesada sea la molécula, más fuertes son estas fuerzas y mayores son los puntos de fusión y ebullición.
Los puentes de hidrógeno son especiales - solo aparecen cuando el hidrógeno está unido a N, O o F. Son más fuertes que las fuerzas de Van der Waals y explican por qué el agua tiene propiedades tan únicas.
¡Dato interesante! Los puentes de hidrógeno son los responsables de que el ADN mantenga su estructura de doble hélice

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace metálico: el mar de electrones
El enlace metálico es como un club exclusivo de metales. Los átomos metálicos pierden sus electrones de valencia, que quedan flotando en un "mar de electrones" compartido por todos.
Esta estructura especial explica por qué los metales conducen electricidad incluso en estado sólido - los electrones pueden moverse libremente por toda la estructura.
Los metales son dúctiles (se hacen hilos), maleables (se hacen láminas) y generalmente duros. Pueden deformarse sin romperse porque las capas de átomos pueden deslizarse unas sobre otras.
¡Aplicación real! Gracias al enlace metálico puedes cargar tu móvil - los cables de cobre conducen la electricidad perfectamente

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: Resonancia Magnética Nuclear (NMR)
9Leyes fundamentales de la química
Resumen
Formulario MAS (movimiento armónico simple)
Formulario para ejercicios
Fórmulas Campo magnético e inducción electromagnética
Formulario Campo magnéticoinducción electromagnétic
Disoluciones y gases química 1° Bach
Tema 5: Leyes fundamentales de la química. Tema 6: Disoluciones y gases. Teoría y fórmulas de las disoluciones y de los gases.
Fórmulas Campo Eléctrico
Formularo de campo eléctrico
Mol y masas molares.
-la masa molecular relativa, composición centesimal, moles, leyes, teoría cinético molecular
Termoquímica
Resumen de termoquímica con ejercicios
GRAVITACIÓN FÍSICA 2BACH
contenido PAU y 2 Bachillerato física
Modelos atómicos
Apuntes modelos atómicos física y química teoría de los diferentes modelos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.