Las disoluciones son mezclas homogéneas formadas por solutos y disolventes.... Mostrar más
Concentración de Disoluciones: Unidades Explicadas
Unidades de Concentración en Disoluciones
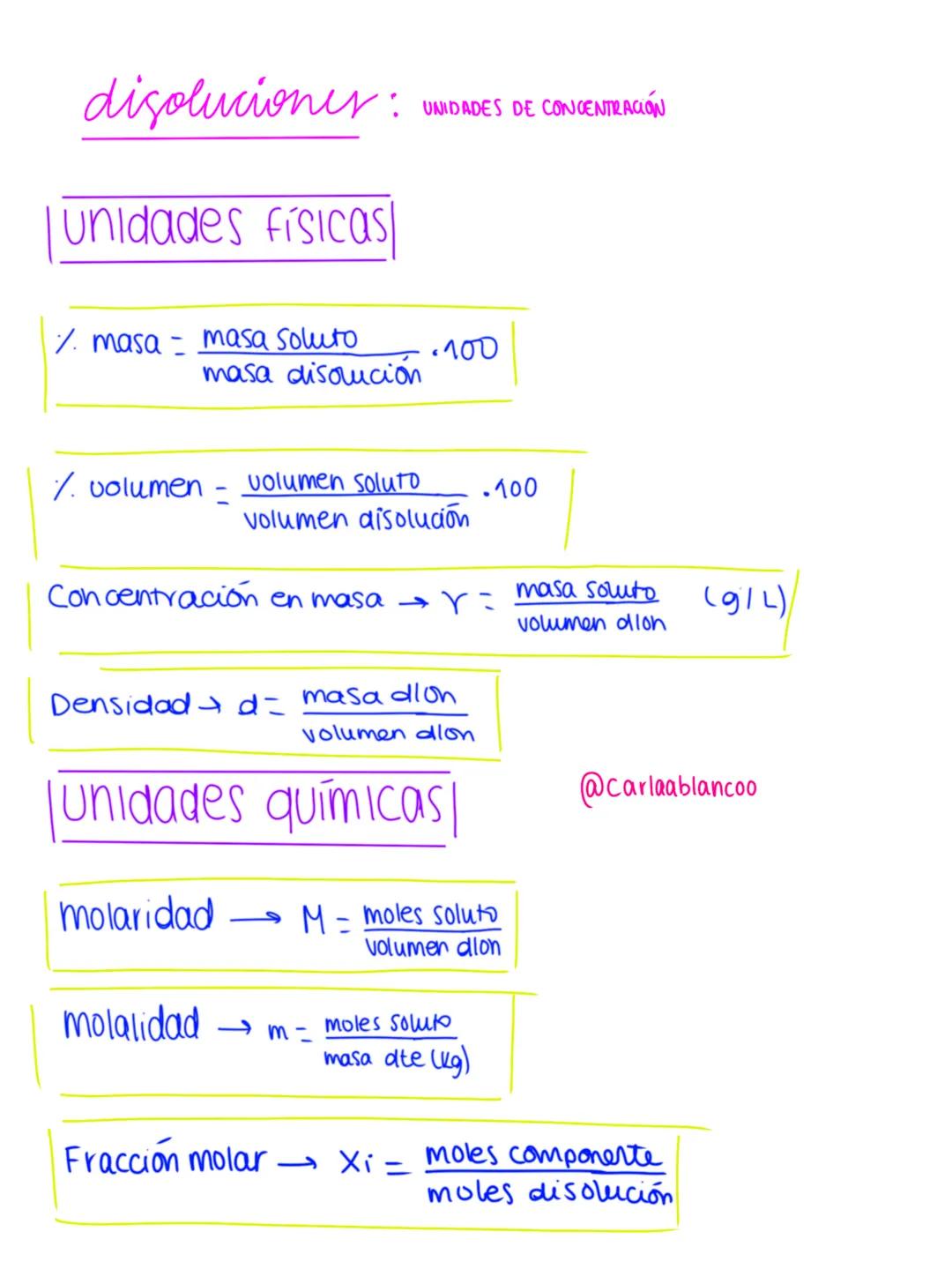
Las concentraciones de disoluciones se pueden expresar mediante unidades físicas o unidades químicas. Cada tipo tiene sus aplicaciones específicas según el contexto.
Entre las unidades físicas encontramos el porcentaje en masa (masa de soluto dividida por masa de disolución, multiplicado por 100), el porcentaje en volumen (volumen de soluto dividido por volumen de disolución, por 100) y la concentración en masa (gramos de soluto por litro de disolución). La densidad también es importante, calculada como la masa de la disolución entre su volumen.
Las unidades químicas incluyen la molaridad (M), definida como los moles de soluto por litro de disolución; la molalidad (m), que son los moles de soluto por kilogramo de disolvente; y la fracción molar (Xi), calculada como los moles de un componente divididos por los moles totales de la disolución.
💡 Consejo práctico: Para elegir la unidad adecuada, piensa en el contexto del problema. Para reacciones químicas suele ser más útil la molaridad, mientras que para propiedades coligativas la molalidad es más apropiada.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: densidad
9Disolución de Solutos en Fórmula de DancCion
Discusión sobre la disolución de solutos en la fórmula de DancCion y sus propiedades químicas. Artículo técnico de química.
Disoluciones: tipos, concentración, porcentaje en masa y en volumen, y solubilidad
Apuntes de las disoluciones: tipos, concentración, porcentaje en masa y en volumen, y solubilidad. 3°ESO. Suerte!
Formulario Leyes Ponderales 1 Bachillerato
Tema 1
La densidad F & Q
la densidad de física y química, son apuntes que he copiado en clase.
FORMULACIÓN Y NOMENCLATURA
Compuestos de oxígeno, compuesto de hidrógeno, sales binarias y hidróxidos
La materia
Propiedades generales y específicas de la materia. Masa, peso, volumen, capacidad, densidad, punto de fusión, punto de ebullición, solubilidad.
Instrumentos de laboratorio
Instrumentos de laboratorio y sus definiciones
Disoluciones química
Formulario disoluciones
Tema 3. La materia y su aspecto (FYQ 3ESO)
Sustancias puras y mezclas Porcentaje en masa, porcentaje en volumen y concentración en masa y solubilidad.
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Concentración de Disoluciones: Unidades Explicadas
Las disoluciones son mezclas homogéneas formadas por solutos y disolventes. Para describir cuánto soluto hay en una disolución, utilizamos diferentes unidades de concentración. Estas unidades son fundamentales en química para preparar disoluciones y realizar cálculos estequiométricos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Unidades de Concentración en Disoluciones
Las concentraciones de disoluciones se pueden expresar mediante unidades físicas o unidades químicas. Cada tipo tiene sus aplicaciones específicas según el contexto.
Entre las unidades físicas encontramos el porcentaje en masa (masa de soluto dividida por masa de disolución, multiplicado por 100), el porcentaje en volumen (volumen de soluto dividido por volumen de disolución, por 100) y la concentración en masa (gramos de soluto por litro de disolución). La densidad también es importante, calculada como la masa de la disolución entre su volumen.
Las unidades químicas incluyen la molaridad (M), definida como los moles de soluto por litro de disolución; la molalidad (m), que son los moles de soluto por kilogramo de disolvente; y la fracción molar (Xi), calculada como los moles de un componente divididos por los moles totales de la disolución.
💡 Consejo práctico: Para elegir la unidad adecuada, piensa en el contexto del problema. Para reacciones químicas suele ser más útil la molaridad, mientras que para propiedades coligativas la molalidad es más apropiada.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: densidad
9Disolución de Solutos en Fórmula de DancCion
Discusión sobre la disolución de solutos en la fórmula de DancCion y sus propiedades químicas. Artículo técnico de química.
Disoluciones: tipos, concentración, porcentaje en masa y en volumen, y solubilidad
Apuntes de las disoluciones: tipos, concentración, porcentaje en masa y en volumen, y solubilidad. 3°ESO. Suerte!
Formulario Leyes Ponderales 1 Bachillerato
Tema 1
La densidad F & Q
la densidad de física y química, son apuntes que he copiado en clase.
FORMULACIÓN Y NOMENCLATURA
Compuestos de oxígeno, compuesto de hidrógeno, sales binarias y hidróxidos
La materia
Propiedades generales y específicas de la materia. Masa, peso, volumen, capacidad, densidad, punto de fusión, punto de ebullición, solubilidad.
Instrumentos de laboratorio
Instrumentos de laboratorio y sus definiciones
Disoluciones química
Formulario disoluciones
Tema 3. La materia y su aspecto (FYQ 3ESO)
Sustancias puras y mezclas Porcentaje en masa, porcentaje en volumen y concentración en masa y solubilidad.
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.