¡Los enlaces químicos son como las amistades entre átomos! Imagínate... Mostrar más
Compuestos Químicos: Una Guía Completa






Compuestos Químicos - Introducción
¿Sabías que todo lo que tocas, desde tu móvil hasta el agua que bebes, está formado por átomos unidos de diferentes maneras? Los átomos son como pequeños bloques de construcción que se combinan siguiendo reglas específicas.
La clave está en que los átomos no se conforman con estar solos. Buscan constantemente estabilidad, y para conseguirla necesitan unirse con otros átomos. Es como si cada átomo tuviera una "zona de confort" que solo puede alcanzar cuando se asocia con otros.
💡 Recuerda: Los átomos siempre buscan parecerse a los gases nobles, que son los elementos más estables de la tabla periódica.
¿Por qué se Unen los Átomos?
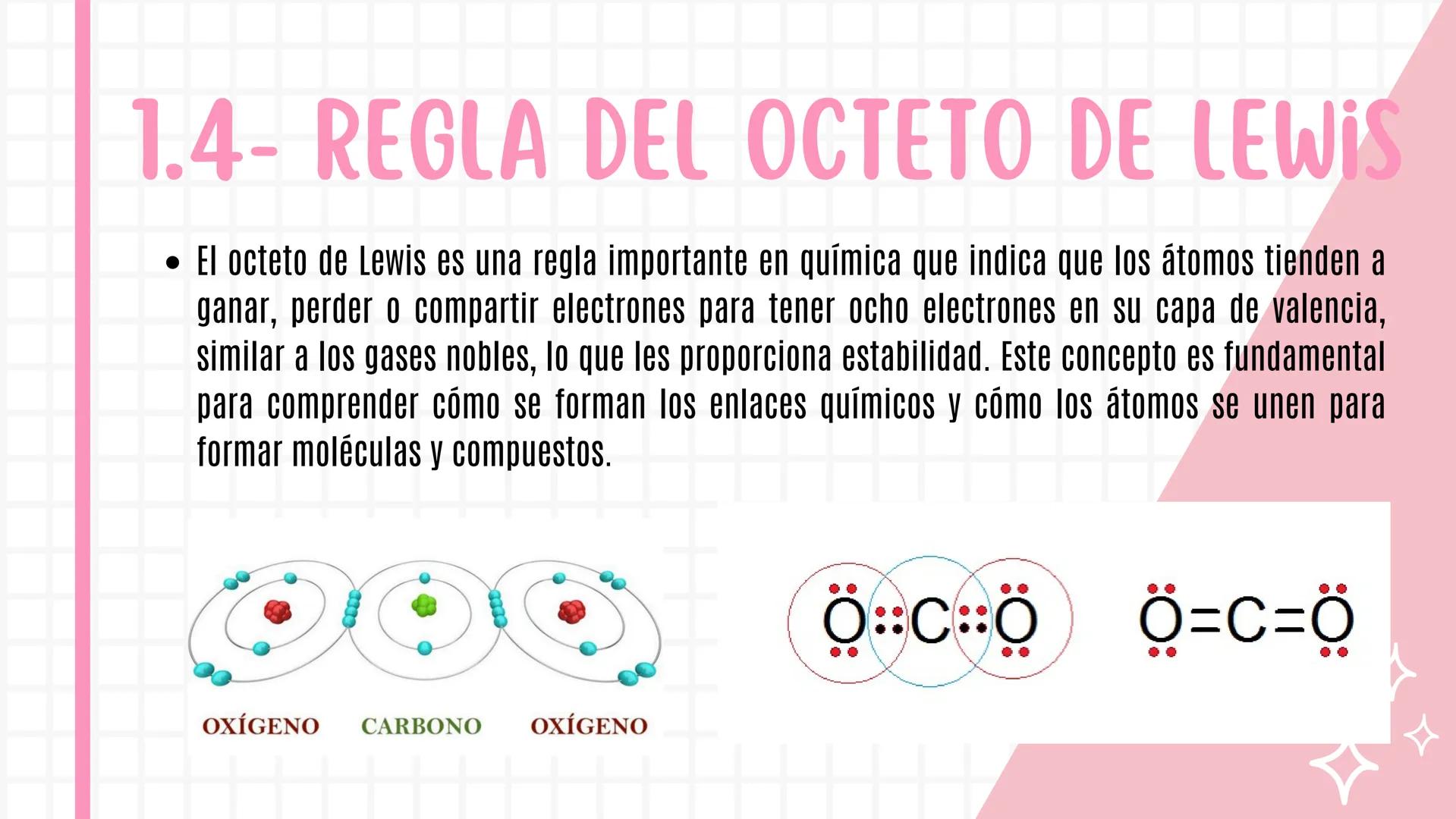
Los átomos se comportan como personas que buscan completar algo que les falta. Específicamente, quieren tener ocho electrones en su capa externa (esto se llama regla del octeto de Lewis).
Para conseguir estos ocho electrones, los átomos pueden hacer tres cosas: ganar electrones, perder electrones o compartir electrones con otros átomos. Es como intercambiar cromos para completar una colección.
Un enlace químico es exactamente esa fuerza invisible que mantiene unidos a los átomos. Sin estos enlaces, no existirían las moléculas ni los compuestos que forman todo lo que conoces.
💡 Dato curioso: Los gases nobles ya tienen ocho electrones en su capa externa, por eso son tan "antisociales" y rara vez se unen con otros átomos.

Enlaces Fuertes vs Enlaces Débiles
No todos los enlaces son igual de potentes. Imagina la diferencia entre un apretón de manos y un abrazo fuerte: así funcionan los enlaces fuertes y los enlaces débiles.
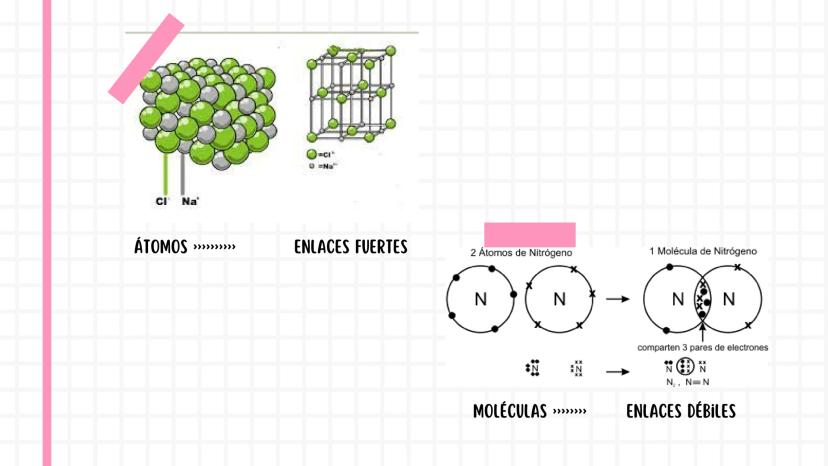
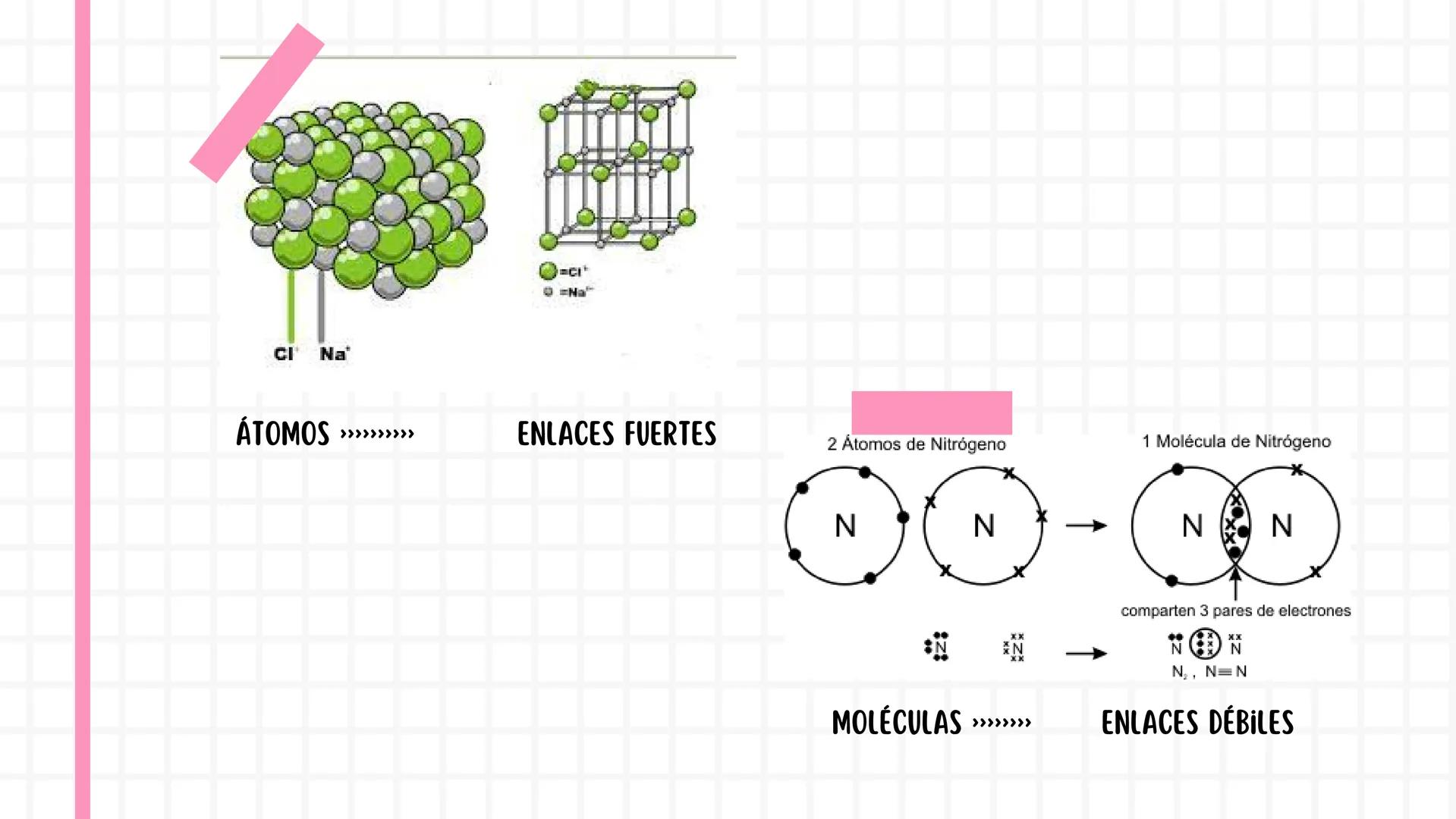
Los enlaces fuertes se forman entre átomos individuales y crean moléculas estables. Por ejemplo, cuando dos átomos de nitrógeno comparten tres pares de electrones, forman una molécula súper resistente.
Los enlaces débiles actúan entre moléculas ya formadas. Son como las fuerzas que mantienen unidas las páginas de un libro: individualmente son suaves, pero juntas crean estructuras sólidas.
💡 Para el examen: Recuerda que los enlaces dentro de las moléculas son fuertes, pero entre moléculas diferentes son débiles.
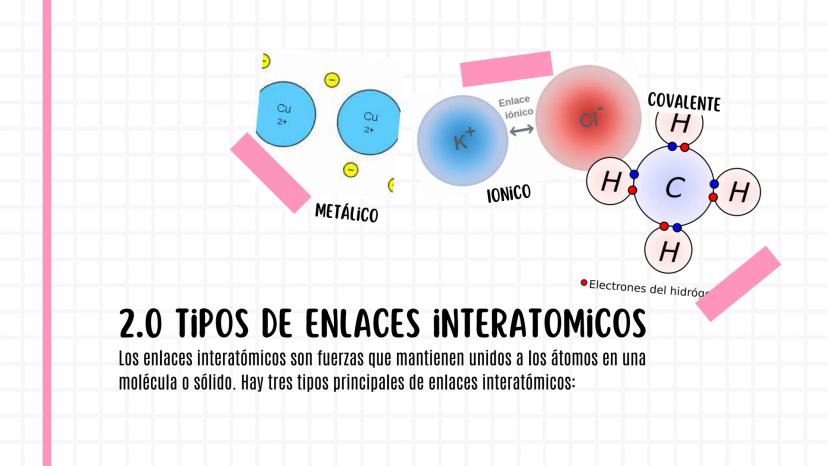
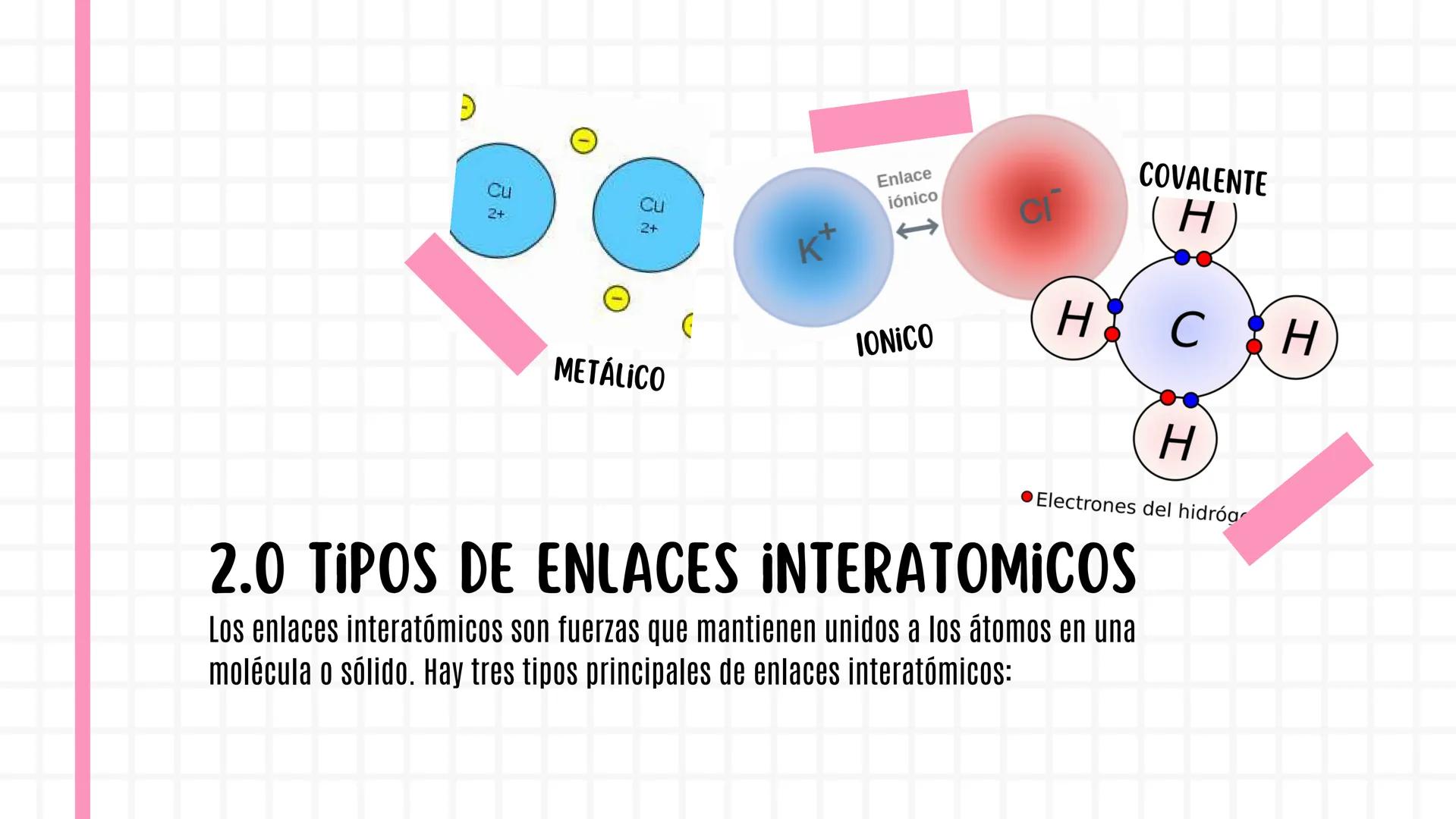
Tipos de Enlaces Interatómicos
Existen tres tipos principales de enlaces interatómicos: iónico, covalente y metálico. Cada uno funciona de manera diferente, como tres tipos distintos de amistad.
El enlace iónico se forma cuando un átomo le "regala" electrones a otro. Es como cuando alguien te da algo que necesitas y tú le das algo que necesita esa persona.
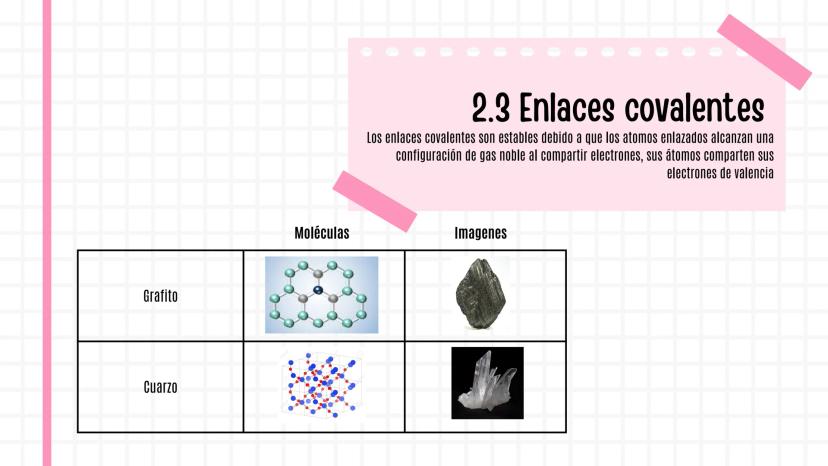
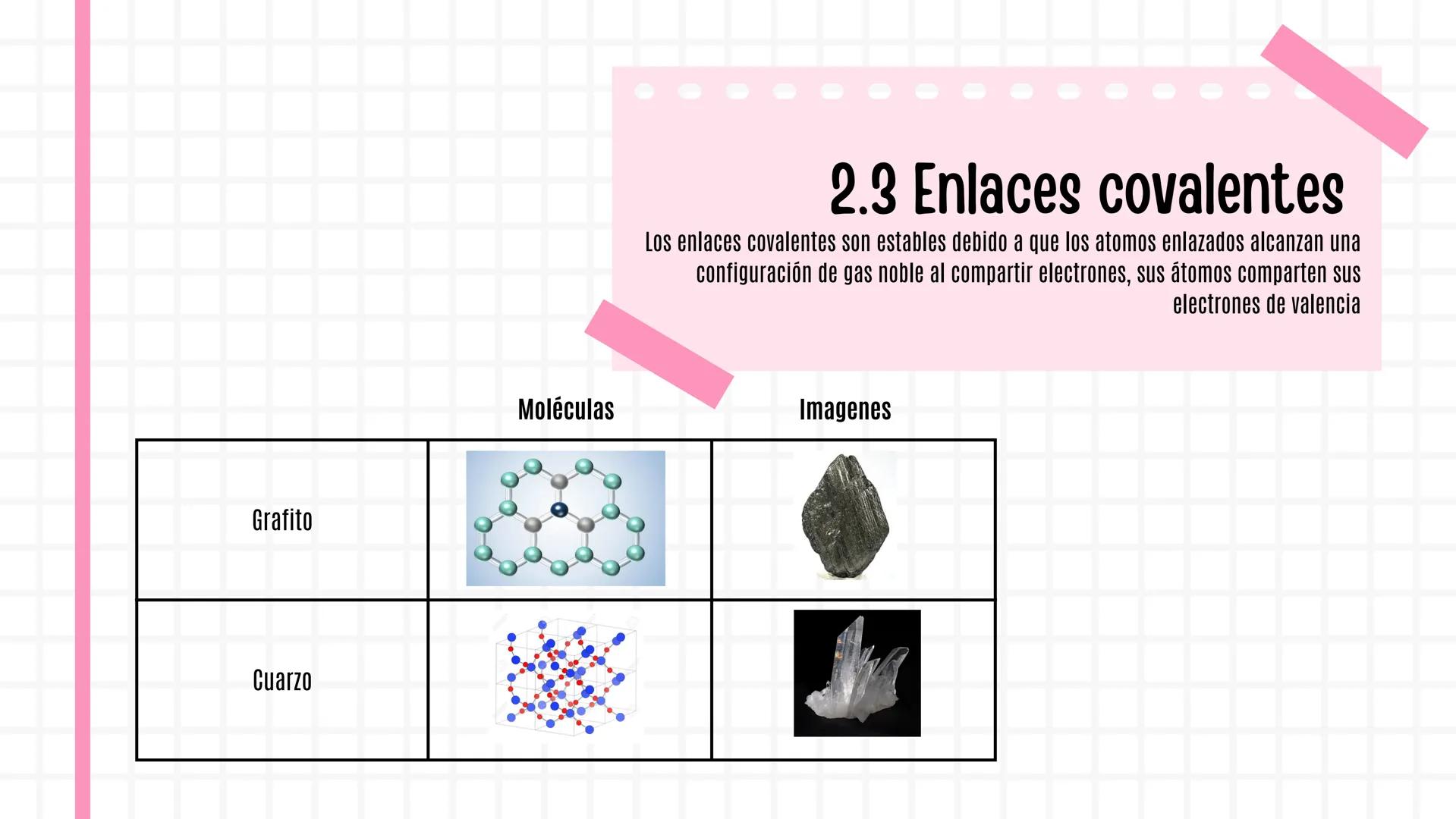
El enlace covalente ocurre cuando dos átomos deciden "compartir" sus electrones. Es como compartir unos auriculares: ambos se benefician al mismo tiempo.
💡 Truco memorización: Iónico = intercambio, Covalente = compartir, Metálico = comunidad de electrones.
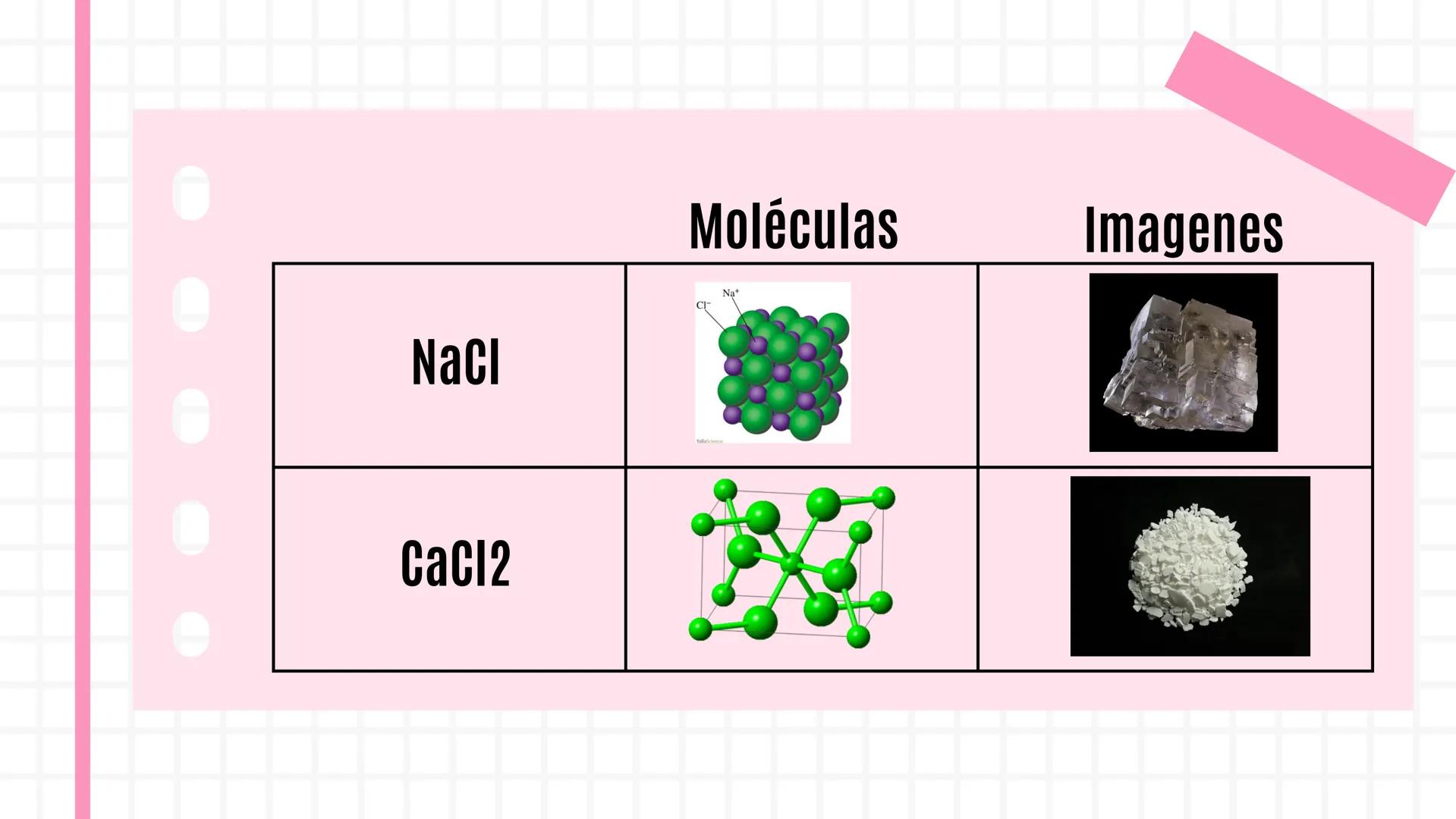
Enlace Iónico
El enlace iónico es pura atracción entre opuestos. Se forma entre un catión (átomo con carga positiva) y un anión (átomo with carga negativa). Es como los imanes: los polos opuestos se atraen irresistiblemente.
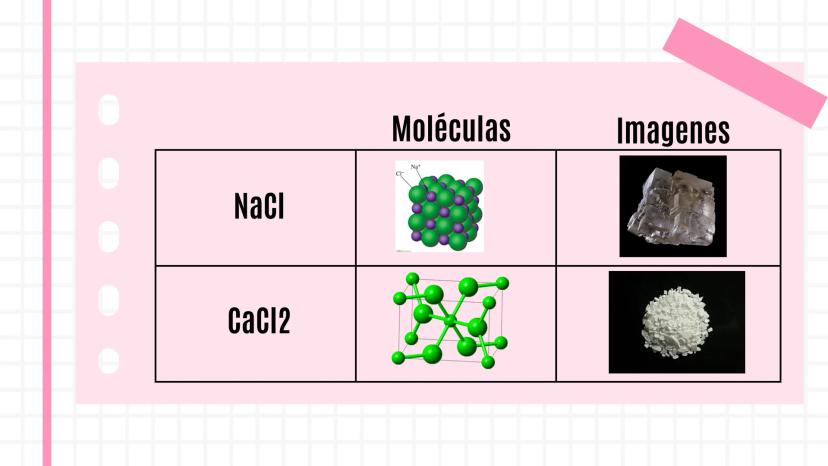
Normalmente, los metales pierden electrones y se convierten en cationes, mientras que los no metales ganan esos electrones y se vuelven aniones. El resultado son compuestos como la sal de cocina (NaCl) que usas todos los días.
Esta atracción electrostática es tan fuerte que forma cristales sólidos. Por eso la sal tiene esa forma cristalina característica que puedes ver con una lupa.
💡 Ejemplo cotidiano: La sal que echas a las patatas fritas es cloruro de sodio (NaCl), un perfecto ejemplo de enlace iónico.
Enlaces Covalentes y Electronegatividad
Los enlaces covalentes se forman cuando los átomos comparten electrones para alcanzar estabilidad. Es como dos amigos que comparten una pizza: ambos quedan satisfechos.
La electronegatividad es súper importante aquí. Es la "fuerza" que tiene cada átomo para atraer electrones hacia sí mismo. Piénsalo como la capacidad de convencer: algunos átomos son más persuasivos que otros.
La escala de Pauling mide esta electronegatividad del 0 al 4. El flúor es el más "egoísta" con los electrones (3,98), mientras que elementos como el cesio son más "generosos" (0,79). Esta diferencia determina cómo se comportan los enlaces.
💡 Para recordar: Mayor electronegatividad = más "hambre" de electrones. El flúor es el más "goloso" de todos.


Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: partículas atómicas
9El átomo
El átomo
Tabla Periódica Frases
Frases de algunas columnas para ayudar a memorizar la tabla periódica
Propiedades periódicas
Apuntes propiedades periódicas 1bach, las actividades son de emestrada.
Enlaces químicos, uniones intermoleculares, reacciones químicas e industria química.
Apunets sobre los enlaces químicos y sus tipos, las uniones intermoleculares, reacciones químicas con sus procesos y factores e información y estaciones en la industria química.
Identificación de Átomos: Número Atómico
El número atómico y el número másico son clave para diferenciar átomos de distintos elementos. Ejemplo con el sodio.
Tabla periódica (solo los símbolos químicos y sus nombres 🕺🏼🕺🏼🕺🏼
Faltan algún ya que esos son los que pidió mi profesor espero ayudar 😰😰😰
El enlace químico
Profundizamos en el enlace químico
La jerga química: formulación inorgánica
LA JERGA QUÍMICA: FORMULACIÓN INORGÁNICA
Peroxidos
Formulación
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Compuestos Químicos: Una Guía Completa
¡Los enlaces químicos son como las amistades entre átomos! Imagínate que los átomos buscan constantemente sentirse más estables y seguros, igual que nosotros buscamos amistades que nos aporten bienestar. En esta unidad vas a descubrir cómo y por qué los... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Compuestos Químicos - Introducción
¿Sabías que todo lo que tocas, desde tu móvil hasta el agua que bebes, está formado por átomos unidos de diferentes maneras? Los átomos son como pequeños bloques de construcción que se combinan siguiendo reglas específicas.
La clave está en que los átomos no se conforman con estar solos. Buscan constantemente estabilidad, y para conseguirla necesitan unirse con otros átomos. Es como si cada átomo tuviera una "zona de confort" que solo puede alcanzar cuando se asocia con otros.
💡 Recuerda: Los átomos siempre buscan parecerse a los gases nobles, que son los elementos más estables de la tabla periódica.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
¿Por qué se Unen los Átomos?
Los átomos se comportan como personas que buscan completar algo que les falta. Específicamente, quieren tener ocho electrones en su capa externa (esto se llama regla del octeto de Lewis).
Para conseguir estos ocho electrones, los átomos pueden hacer tres cosas: ganar electrones, perder electrones o compartir electrones con otros átomos. Es como intercambiar cromos para completar una colección.
Un enlace químico es exactamente esa fuerza invisible que mantiene unidos a los átomos. Sin estos enlaces, no existirían las moléculas ni los compuestos que forman todo lo que conoces.
💡 Dato curioso: Los gases nobles ya tienen ocho electrones en su capa externa, por eso son tan "antisociales" y rara vez se unen con otros átomos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces Fuertes vs Enlaces Débiles
No todos los enlaces son igual de potentes. Imagina la diferencia entre un apretón de manos y un abrazo fuerte: así funcionan los enlaces fuertes y los enlaces débiles.
Los enlaces fuertes se forman entre átomos individuales y crean moléculas estables. Por ejemplo, cuando dos átomos de nitrógeno comparten tres pares de electrones, forman una molécula súper resistente.
Los enlaces débiles actúan entre moléculas ya formadas. Son como las fuerzas que mantienen unidas las páginas de un libro: individualmente son suaves, pero juntas crean estructuras sólidas.
💡 Para el examen: Recuerda que los enlaces dentro de las moléculas son fuertes, pero entre moléculas diferentes son débiles.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tipos de Enlaces Interatómicos
Existen tres tipos principales de enlaces interatómicos: iónico, covalente y metálico. Cada uno funciona de manera diferente, como tres tipos distintos de amistad.
El enlace iónico se forma cuando un átomo le "regala" electrones a otro. Es como cuando alguien te da algo que necesitas y tú le das algo que necesita esa persona.
El enlace covalente ocurre cuando dos átomos deciden "compartir" sus electrones. Es como compartir unos auriculares: ambos se benefician al mismo tiempo.
💡 Truco memorización: Iónico = intercambio, Covalente = compartir, Metálico = comunidad de electrones.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace Iónico
El enlace iónico es pura atracción entre opuestos. Se forma entre un catión (átomo con carga positiva) y un anión (átomo with carga negativa). Es como los imanes: los polos opuestos se atraen irresistiblemente.
Normalmente, los metales pierden electrones y se convierten en cationes, mientras que los no metales ganan esos electrones y se vuelven aniones. El resultado son compuestos como la sal de cocina (NaCl) que usas todos los días.
Esta atracción electrostática es tan fuerte que forma cristales sólidos. Por eso la sal tiene esa forma cristalina característica que puedes ver con una lupa.
💡 Ejemplo cotidiano: La sal que echas a las patatas fritas es cloruro de sodio (NaCl), un perfecto ejemplo de enlace iónico.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces Covalentes y Electronegatividad
Los enlaces covalentes se forman cuando los átomos comparten electrones para alcanzar estabilidad. Es como dos amigos que comparten una pizza: ambos quedan satisfechos.
La electronegatividad es súper importante aquí. Es la "fuerza" que tiene cada átomo para atraer electrones hacia sí mismo. Piénsalo como la capacidad de convencer: algunos átomos son más persuasivos que otros.
La escala de Pauling mide esta electronegatividad del 0 al 4. El flúor es el más "egoísta" con los electrones (3,98), mientras que elementos como el cesio son más "generosos" (0,79). Esta diferencia determina cómo se comportan los enlaces.
💡 Para recordar: Mayor electronegatividad = más "hambre" de electrones. El flúor es el más "goloso" de todos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: partículas atómicas
9El átomo
El átomo
Tabla Periódica Frases
Frases de algunas columnas para ayudar a memorizar la tabla periódica
Propiedades periódicas
Apuntes propiedades periódicas 1bach, las actividades son de emestrada.
Enlaces químicos, uniones intermoleculares, reacciones químicas e industria química.
Apunets sobre los enlaces químicos y sus tipos, las uniones intermoleculares, reacciones químicas con sus procesos y factores e información y estaciones en la industria química.
Identificación de Átomos: Número Atómico
El número atómico y el número másico son clave para diferenciar átomos de distintos elementos. Ejemplo con el sodio.
Tabla periódica (solo los símbolos químicos y sus nombres 🕺🏼🕺🏼🕺🏼
Faltan algún ya que esos son los que pidió mi profesor espero ayudar 😰😰😰
El enlace químico
Profundizamos en el enlace químico
La jerga química: formulación inorgánica
LA JERGA QUÍMICA: FORMULACIÓN INORGÁNICA
Peroxidos
Formulación
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.