¿Alguna vez te has preguntado por qué algunos materiales brillan... Mostrar más
El Sistema Periódico y Enlaces Químicos: Guía Completa


Sistema Periódico y Propiedades de los Elementos
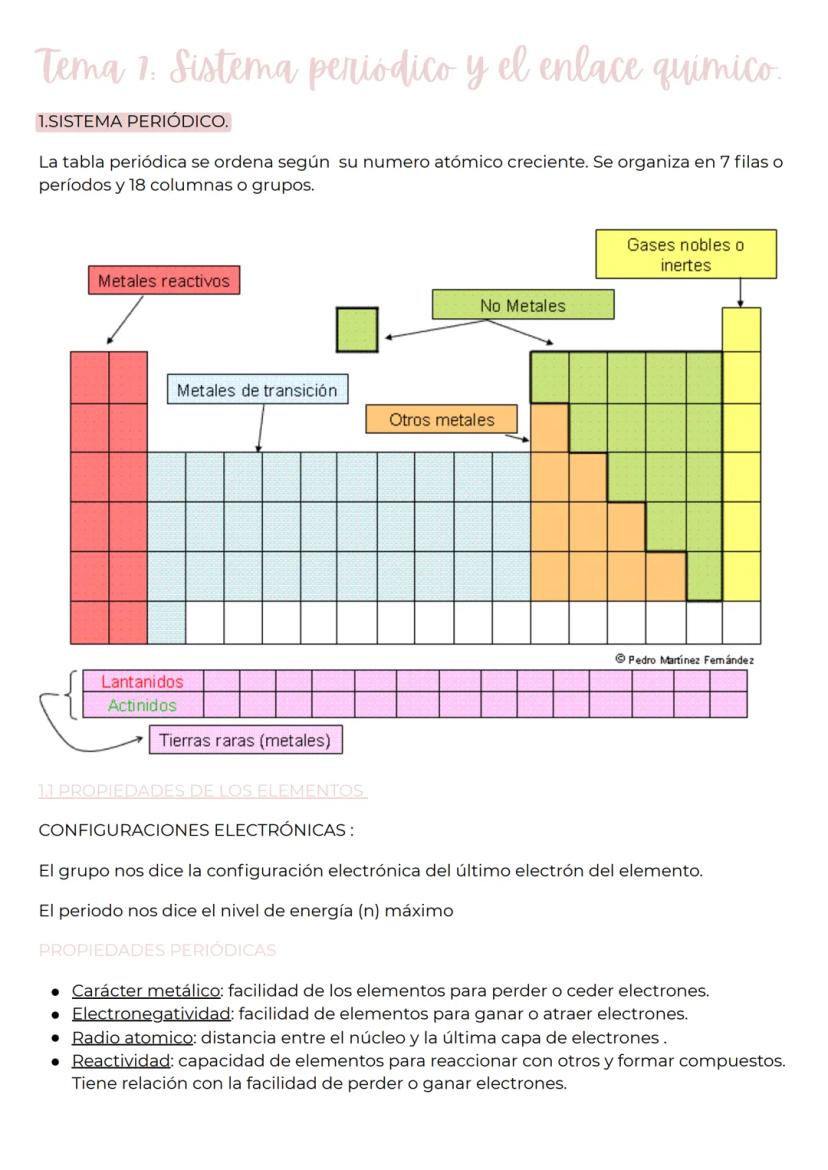
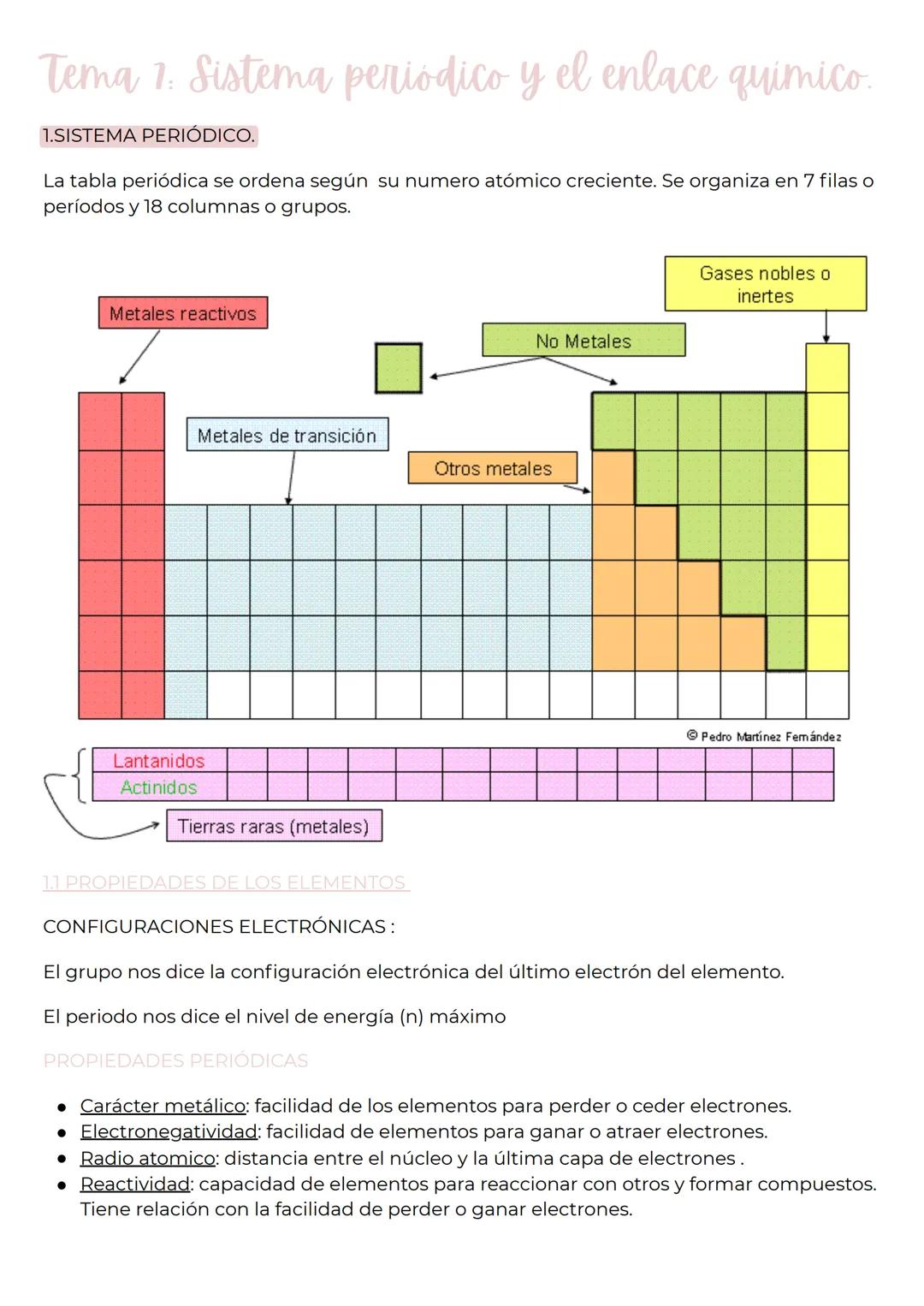
La tabla periódica no es solo una lista aleatoria de elementos - está súper organizada por número atómico creciente con 7 filas (períodos) and 18 columnas (grupos). Piénsalo como un mapa donde cada posición te dice algo específico sobre el elemento.
El grupo te indica la configuración electrónica del último electrón, mientras que el período te dice el nivel de energía máximo. Es como tener la dirección exacta de cada elemento.
Las propiedades periódicas más importantes son cuatro: el carácter metálico (facilidad para perder electrones), la electronegatividad (facilidad para ganar electrones), el radio atómico (tamaño del átomo) y la reactividad (capacidad de formar compuestos). Todas estas propiedades siguen patrones predecibles en la tabla.
¡Dato curioso! Si conoces la posición de un elemento en la tabla, puedes predecir muchas de sus propiedades sin memorizarlas.

Tendencias Periódicas y Enlace Covalente
Las propiedades cambian siguiendo patrones específicos: hacia la derecha aumentan la electronegatividad y disminuyen el carácter metálico y el radio atómico. Hacia abajo aumenta el radio atómico. ¡Es como seguir instrucciones en un videojuego!
El enlace químico es simplemente una fuerza que mantiene unidos a los átomos. La regla del octeto explica que los átomos buscan tener 8 electrones en su última capa - es su estado más estable.
El enlace covalente ocurre entre no metales que comparten electrones. Las sustancias covalentes moleculares forman moléculas que puedes representar con diagramas de Lewis usando los electrones de valencia.
La polaridad divide las moléculas en dos tipos: apolares (electrones distribuidos uniformemente) y polares (distribución desigual que crea polos de carga). Las fuerzas intermoleculares incluyen las débiles fuerzas de Van der Waals y los más fuertes enlaces de hidrógeno.
Consejo de estudio: Practica dibujando estructuras de Lewis - te ayudará a visualizar cómo se comparten los electrones.

Sustancias Covalentes Cristalinas y Enlace Iónico
Las sustancias covalentes moleculares tienen puntos de fusión y ebullición bajos, densidad baja y poca conductividad. La mayoría son gases o líquidos a temperatura ambiente - como el agua que bebes.
Los cristales covalentes son diferentes: átomos organizados simétricamente en tres dimensiones. Hay cristales moleculares (sustancias moleculares congeladas) y cristales atómicos (como los del carbono). Estos tienen gran dureza, puntos de fusión altísimos y son prácticamente insolubles.
El enlace iónico une metales con no metales mediante transferencia de electrones. Los metales se convierten en cationes y los no metales en aniones. Es como un intercambio: uno da, otro recibe.
Las propiedades iónicas son distintivas: forman redes cristalinas sólidas, tienen puntos de fusión altos, conducen electricidad cuando están disueltos, pero son frágiles porque las capas pueden desplazarse.
Recuerda: Covalente = compartir electrones, Iónico = transferir electrones.
Enlace Metálico y sus Propiedades
El enlace metálico es único: los metales forman cationes que expulsan electrones de su última capa, creando una nube electrónica móvil. Es como si los electrones fueran un mar que rodea islas de cationes.
Esta estructura especial explica por qué los cationes no se repelen - los electrones móviles neutralizan constantemente las cargas. Es un sistema súper eficiente que la naturaleza ha perfeccionado.
Las propiedades metálicas son fáciles de recordar porque las ves constantemente: brillo característico, conductividad eléctrica y térmica excelente, ductilidad y maleabilidad (se pueden estirar y moldear). Los puntos de fusión varían mucho según el metal.
Ahora entiendes por qué el cobre conduce electricidad, por qué puedes doblar el aluminio, y por qué los metales brillan. Todo está en su estructura de enlace único.
Aplicación práctica: La próxima vez que uses un cable o veas joyas brillantes, recordarás que todo se debe a esa nube electrónica móvil.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
Introducción a la Tabla Periódica
Identifica los símbolos de los elementos químicos y la organización básica en grupos y periodos de la tabla periódica.
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
Contenidos más populares
9Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
QUIZZ VIDA DIARIA#1
QUIZZ sobre tu vida diaria, psicológico para mejorar el estudio.:] [ Cualquier pregunta, la responderé ]^^
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
El Sistema Periódico y Enlaces Químicos: Guía Completa
¿Alguna vez te has preguntado por qué algunos materiales brillan mientras otros no, o por qué el agua hierve a 100°C pero otros líquidos a temperaturas completamente diferentes? Todo tiene que ver con cómo se organizan los elementos en la... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sistema Periódico y Propiedades de los Elementos
La tabla periódica no es solo una lista aleatoria de elementos - está súper organizada por número atómico creciente con 7 filas (períodos) and 18 columnas (grupos). Piénsalo como un mapa donde cada posición te dice algo específico sobre el elemento.
El grupo te indica la configuración electrónica del último electrón, mientras que el período te dice el nivel de energía máximo. Es como tener la dirección exacta de cada elemento.
Las propiedades periódicas más importantes son cuatro: el carácter metálico (facilidad para perder electrones), la electronegatividad (facilidad para ganar electrones), el radio atómico (tamaño del átomo) y la reactividad (capacidad de formar compuestos). Todas estas propiedades siguen patrones predecibles en la tabla.
¡Dato curioso! Si conoces la posición de un elemento en la tabla, puedes predecir muchas de sus propiedades sin memorizarlas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tendencias Periódicas y Enlace Covalente
Las propiedades cambian siguiendo patrones específicos: hacia la derecha aumentan la electronegatividad y disminuyen el carácter metálico y el radio atómico. Hacia abajo aumenta el radio atómico. ¡Es como seguir instrucciones en un videojuego!
El enlace químico es simplemente una fuerza que mantiene unidos a los átomos. La regla del octeto explica que los átomos buscan tener 8 electrones en su última capa - es su estado más estable.
El enlace covalente ocurre entre no metales que comparten electrones. Las sustancias covalentes moleculares forman moléculas que puedes representar con diagramas de Lewis usando los electrones de valencia.
La polaridad divide las moléculas en dos tipos: apolares (electrones distribuidos uniformemente) y polares (distribución desigual que crea polos de carga). Las fuerzas intermoleculares incluyen las débiles fuerzas de Van der Waals y los más fuertes enlaces de hidrógeno.
Consejo de estudio: Practica dibujando estructuras de Lewis - te ayudará a visualizar cómo se comparten los electrones.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sustancias Covalentes Cristalinas y Enlace Iónico
Las sustancias covalentes moleculares tienen puntos de fusión y ebullición bajos, densidad baja y poca conductividad. La mayoría son gases o líquidos a temperatura ambiente - como el agua que bebes.
Los cristales covalentes son diferentes: átomos organizados simétricamente en tres dimensiones. Hay cristales moleculares (sustancias moleculares congeladas) y cristales atómicos (como los del carbono). Estos tienen gran dureza, puntos de fusión altísimos y son prácticamente insolubles.
El enlace iónico une metales con no metales mediante transferencia de electrones. Los metales se convierten en cationes y los no metales en aniones. Es como un intercambio: uno da, otro recibe.
Las propiedades iónicas son distintivas: forman redes cristalinas sólidas, tienen puntos de fusión altos, conducen electricidad cuando están disueltos, pero son frágiles porque las capas pueden desplazarse.
Recuerda: Covalente = compartir electrones, Iónico = transferir electrones.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace Metálico y sus Propiedades
El enlace metálico es único: los metales forman cationes que expulsan electrones de su última capa, creando una nube electrónica móvil. Es como si los electrones fueran un mar que rodea islas de cationes.
Esta estructura especial explica por qué los cationes no se repelen - los electrones móviles neutralizan constantemente las cargas. Es un sistema súper eficiente que la naturaleza ha perfeccionado.
Las propiedades metálicas son fáciles de recordar porque las ves constantemente: brillo característico, conductividad eléctrica y térmica excelente, ductilidad y maleabilidad (se pueden estirar y moldear). Los puntos de fusión varían mucho según el metal.
Ahora entiendes por qué el cobre conduce electricidad, por qué puedes doblar el aluminio, y por qué los metales brillan. Todo está en su estructura de enlace único.
Aplicación práctica: La próxima vez que uses un cable o veas joyas brillantes, recordarás que todo se debe a esa nube electrónica móvil.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
Introducción a la Tabla Periódica
Identifica los símbolos de los elementos químicos y la organización básica en grupos y periodos de la tabla periódica.
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
Contenidos más populares
9Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
QUIZZ VIDA DIARIA#1
QUIZZ sobre tu vida diaria, psicológico para mejorar el estudio.:] [ Cualquier pregunta, la responderé ]^^
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.