Las leyes de los gases explican cómo se comportan los... Mostrar más
Comprensión de las leyes de los gases









Las leyes de los gases
Los gases son un estado de la materia con características únicas: ocupan todo el volumen disponible y se adaptan a la forma del recipiente que los contiene. A diferencia de los sólidos y líquidos, sus partículas se mueven libremente y con mucha energía.
Cuando estudiamos los gases, nos centramos en tres propiedades principales que están íntimamente relacionadas: presión, volumen y temperatura. Si modificamos una de estas propiedades, las otras también cambian siguiendo patrones muy precisos.
En esta unidad, descubriremos las leyes que gobiernan el comportamiento de los gases y aprenderemos a predecir qué sucederá cuando cambiamos alguna de sus propiedades. ¡Esto te ayudará a entender muchos fenómenos que ves todos los días!
💡 ¿Sabías que? Los globos aerostáticos funcionan gracias a las leyes de los gases: al calentar el aire de su interior, este se expande y se vuelve menos denso que el aire exterior, lo que hace que el globo se eleve.

Modelo cinético-corpuscular de los gases
Para entender bien cómo funcionan los gases, necesitamos conocer el modelo cinético-corpuscular. Según este modelo, los gases están formados por pequeñísimas partículas (átomos o moléculas) en constante movimiento, separadas por espacios vacíos.
Las partículas de los gases:
- Se mueven a gran velocidad y de forma desordenada
- Chocan entre sí y contra las paredes del recipiente
- Apenas tienen fuerzas de atracción entre ellas
La temperatura de un gas está directamente relacionada con la velocidad de sus partículas. Cuando calentamos un gas, sus partículas se mueven más rápido y tienen más energía cinética. Cuando lo enfriamos, ocurre lo contrario.
La presión es el resultado de las colisiones de las partículas contra las paredes del recipiente. Cuantas más colisiones y más fuertes sean, mayor será la presión. La presión depende de:
- La velocidad con que chocan las partículas
- El número de colisiones por segundo
Cuando modificamos el volumen de un recipiente con gas, cambiamos el espacio disponible para las partículas y, por tanto, la frecuencia de las colisiones y la presión.
🔬 Cuando inflas un globo y lo aprietas, reduces el espacio para las partículas de aire, aumentando las colisiones contra las paredes del globo y, por tanto, la presión.

La ley de Boyle y Mariotte
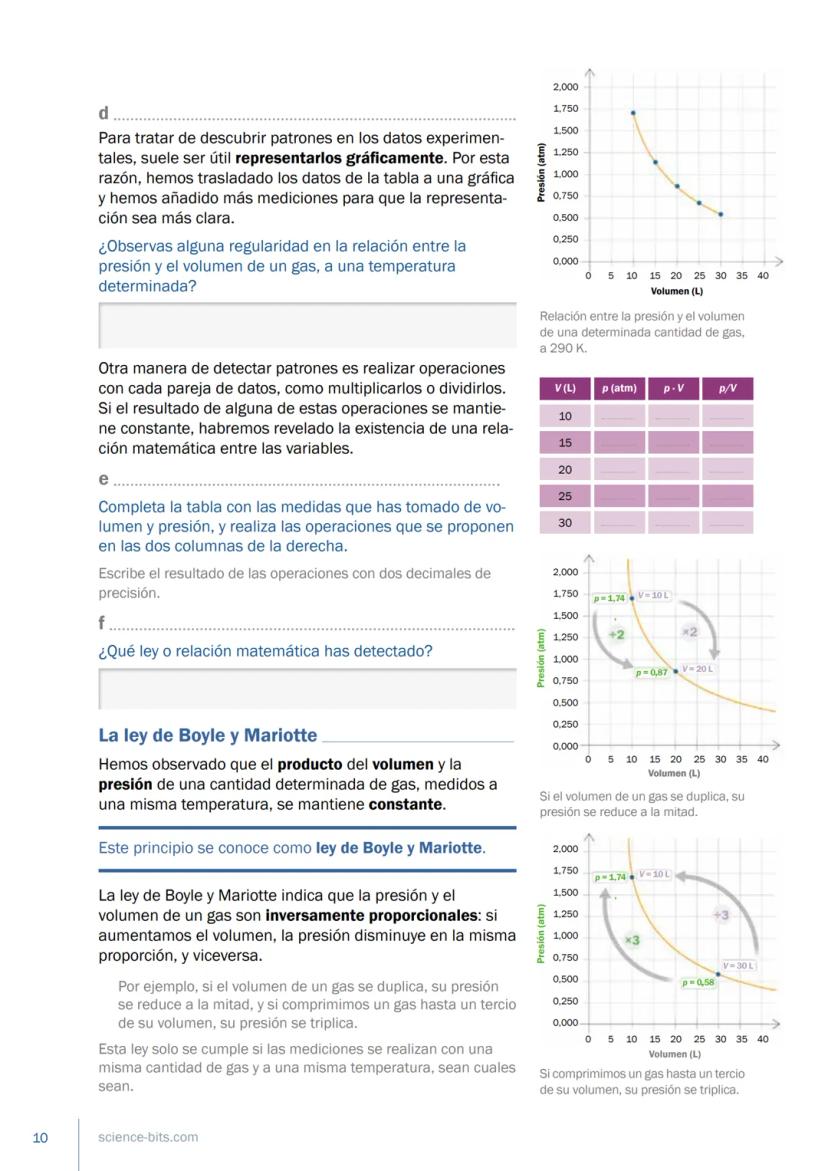
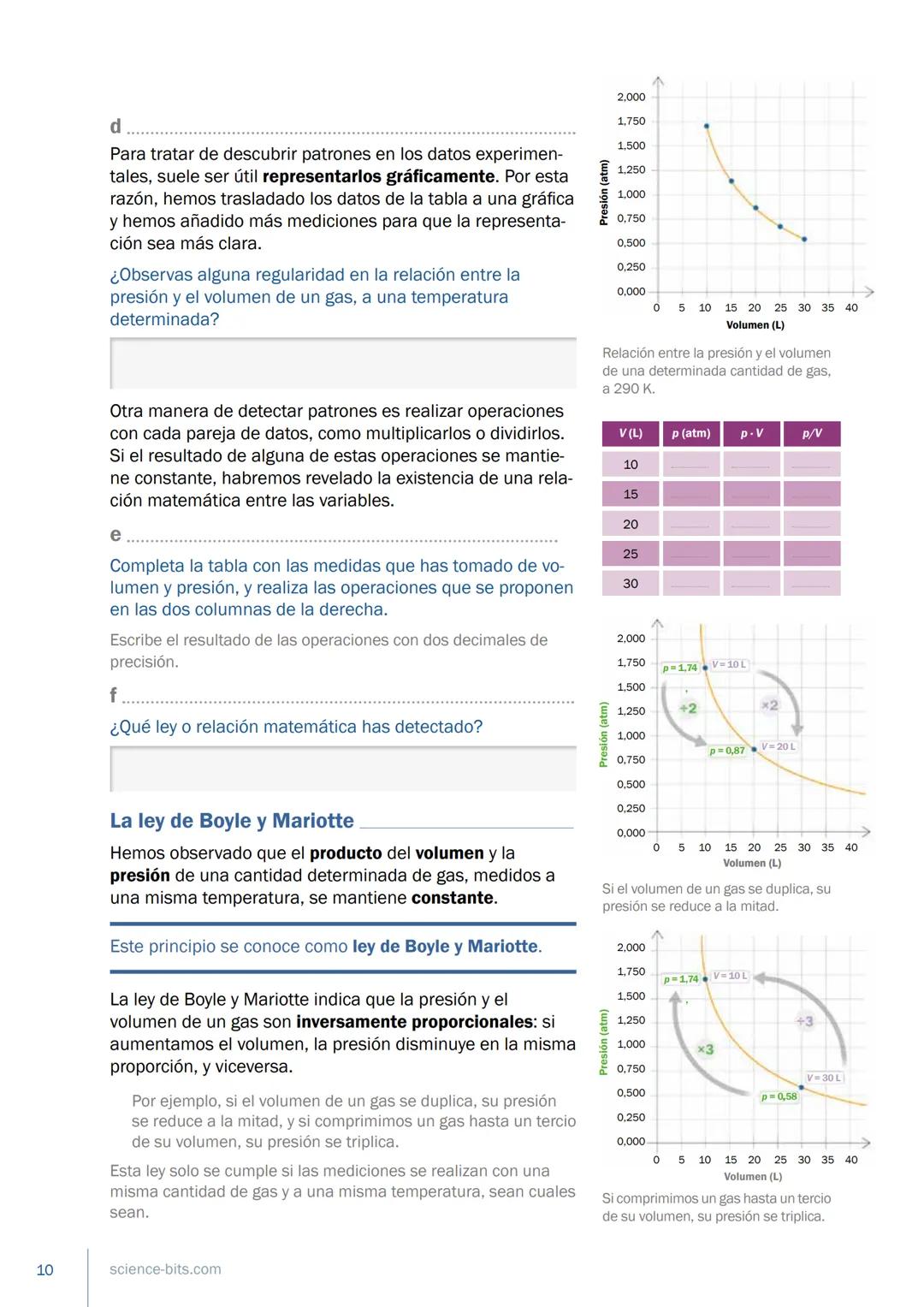
La primera ley de los gases que estudiaremos relaciona la presión y el volumen cuando la temperatura se mantiene constante.
La ley de Boyle y Mariotte establece que, a temperatura constante, la presión y el volumen de un gas son inversamente proporcionales. Esto significa que:
- Si el volumen aumenta, la presión disminuye
- Si el volumen disminuye, la presión aumenta
Matemáticamente lo expresamos como: P × V = constante
Por ejemplo, si duplicamos el volumen de un gas, su presión se reduce a la mitad. Si comprimimos un gas a un tercio de su volumen, su presión se triplica.
Según el modelo cinético-corpuscular, cuando reducimos el volumen de un gas:
- Las partículas tienen menos espacio para moverse
- Aumenta el número de colisiones con las paredes
- La presión aumenta
Al contrario, cuando aumentamos el volumen:
- Las partículas tienen más espacio
- Disminuye el número de colisiones
- La presión disminuye
Esta ley explica por qué cuando comprimes el émbolo de una jeringa tapada, se vuelve cada vez más difícil seguir empujando: ¡la presión del aire en el interior aumenta!
💡 Las ventosas se adhieren a las superficies gracias a la ley de Boyle y Mariotte. Al presionarlas, expulsan aire y crean un espacio con baja presión que hace que la presión atmosférica las mantenga pegadas.
La ley de Gay-Lussac
La segunda ley que estudiaremos relaciona la temperatura y la presión cuando el volumen se mantiene constante.
La ley de Gay-Lussac establece que, a volumen constante, la presión y la temperatura de un gas son directamente proporcionales. Esto significa que:
- Si la temperatura aumenta, la presión también aumenta
- Si la temperatura disminuye, la presión también disminuye
Matemáticamente se expresa como: P/T = constante
Por ejemplo, si duplicamos la temperatura absoluta de un gas (en Kelvin), su presión también se duplicará. Si reducimos la temperatura a la mitad, la presión también se reducirá a la mitad.
Según el modelo cinético-corpuscular, cuando calentamos un gas en un recipiente cerrado de paredes rígidas:
- Las partículas se mueven más rápido
- Chocan con más fuerza contra las paredes
- La presión aumenta
Al enfriar el gas:
- Las partículas se mueven más lentamente
- Chocan con menos fuerza
- La presión disminuye
Es importante recordar que, para que esta ley se cumpla, la temperatura debe expresarse en la escala Kelvin (K), no en grados Celsius.
⚠️ Nunca expongas un bote de aerosol al calor. Al aumentar la temperatura, la presión interior aumenta y podría explotar. Por la misma razón, debes revisar la presión de los neumáticos de tu bici después de circular en un día caluroso.

La ley de Charles y Gay-Lussac
La tercera ley relaciona la temperatura y el volumen cuando la presión se mantiene constante.
La ley de Charles y Gay-Lussac establece que, a presión constante, el volumen y la temperatura de un gas son directamente proporcionales. Esto significa que:
- Si la temperatura aumenta, el volumen también aumenta
- Si la temperatura disminuye, el volumen también disminuye
Matemáticamente se expresa como: V/T = constante
Por ejemplo, si aumentamos la temperatura absoluta de un gas un 20%, su volumen también aumentará un 20%, siempre que la presión se mantenga constante.
Según el modelo cinético-corpuscular, cuando calentamos un gas en un recipiente con una pared móvil (como un émbolo):
- Las partículas se mueven más rápido
- Chocan con más fuerza contra el émbolo
- El émbolo se desplaza y el volumen aumenta
Al enfriar el gas:
- Las partículas se mueven más lentamente
- Ejercen menos fuerza sobre el émbolo
- El gas se comprime y el volumen disminuye
Como en la ley de Gay-Lussac, la temperatura debe expresarse en Kelvin para que se cumpla esta relación.
🎈 ¿Has notado que un globo se desinfla cuando lo metes en el frigorífico? Esto ocurre porque, al disminuir la temperatura, el volumen del aire en su interior también disminuye según la ley de Charles y Gay-Lussac.

Límites de las leyes de los gases y el cero absoluto
Las leyes que hemos estudiado funcionan muy bien en condiciones normales, pero tienen sus límites. Se cumplen cuando las partículas de gas se mueven libremente e independientemente unas de otras, lo que se conoce como comportamiento de gas ideal.
Sin embargo, las leyes de los gases pueden fallar en estas condiciones:
-
Temperaturas muy bajas: Cuando un gas se enfría mucho, las partículas se mueven tan lentamente que empiezan a atraerse entre sí, pudiendo condensarse en líquido o solidificarse.
-
Presiones muy altas: Cuando comprimimos mucho un gas, las partículas están tan cerca que las fuerzas entre ellas se vuelven importantes y ya no se comportan independientemente.
Otro aspecto interesante es el punto de ebullición. La temperatura a la que hierve un líquido depende de la presión:
- A mayor presión, mayor punto de ebullición
- A menor presión, menor punto de ebullición
Por eso, en la cima de una montaña (donde la presión atmosférica es menor), el agua hierve a menos de 100°C, lo que dificulta cocinar alimentos.
Las leyes de los gases nos llevan al concepto del cero absoluto , la temperatura teórica más baja posible. A esta temperatura, las partículas de gas tendrían la mínima energía posible. En la práctica, es imposible alcanzar exactamente el cero absoluto.
🌡️ En la cima del Everest, a 8.848 metros de altitud y con una presión atmosférica de sólo 0,34 atm, el agua hierve a apenas 71°C. ¡Preparar un té caliente sería todo un desafío!

Aplicaciones prácticas de las leyes de los gases
Las leyes de los gases no son solo teorías abstractas; explican numerosos fenómenos cotidianos y tienen aplicaciones muy importantes.
Aplicaciones en la vida diaria:
- Neumáticos de vehículos: La presión aumenta cuando se calientan al circular, por eso es importante revisarla cuando están fríos.
- Ollas a presión: Aumentan el punto de ebullición del agua, cocinando los alimentos más rápido.
- Globos aerostáticos: Se elevan porque el aire caliente del interior ocupa más volumen y es menos denso que el aire exterior.
- Buceo: Los tanques de aire comprimido permiten llevar mucho aire en poco espacio.
En el laboratorio:
- Jeringuillas: Son herramientas perfectas para demostrar la relación entre presión y volumen.
- Manómetros: Miden la presión de gases en recipientes cerrados.
- Termómetros de gas: Utilizan la expansión de gases para medir temperaturas.
En la industria:
- Refrigeración: Los refrigeradores aprovechan los cambios de presión para alterar la temperatura de los gases refrigerantes.
- Motores de combustión interna: Funcionan gracias a la expansión de gases calientes.
- Generación de electricidad: Muchas centrales eléctricas utilizan vapor a presión para mover turbinas.
Entender estas leyes nos ayuda a diseñar mejor muchos dispositivos y a predecir cómo se comportarán los gases en diferentes situaciones.
🚗 Cuando inflas las ruedas de tu bici o coche en invierno y luego hace mucho calor, la presión puede aumentar tanto que podrían dañarse. Siempre revisa la presión con cambios de temperatura significativos.


Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: termodinámica de los gases
8Leyes de los gases
Ley de clapeyron, ley de gay lussac , ley de charles y ley de boyle mariotte
Gases y disoluciones
3° ESO
Leyes de los gases
Las tres leyes
Teoría Cinética y Leyes de los Gases
Resumen sobre la Teoría Cinética y Leyes de los Gases
Los Gases 3ro ESO
Tema de los gases física y quimica
Leyes Y conceptos básicos en química
Apuntes del profesor de la asignatura
Leyes de los Gases
Este artículo explora las leyes de los gases, incluyendo la ley de Charles y la ley de Gay-Lussac, y su relación con la presión, volumen y temperatura.
Propiedades de los gases.
Unidades de los gases. Ley de Boyle Mariotte, ley de Gay-Lussac y Charles.
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Comprensión de las leyes de los gases
Las leyes de los gases explican cómo se comportan los gases cuando cambian su presión, volumen o temperatura. Estas relaciones matemáticas, descubiertas por científicos como Boyle, Mariotte, Gay-Lussac y Charles, nos ayudan a entender fenómenos cotidianos como por qué se... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Las leyes de los gases
Los gases son un estado de la materia con características únicas: ocupan todo el volumen disponible y se adaptan a la forma del recipiente que los contiene. A diferencia de los sólidos y líquidos, sus partículas se mueven libremente y con mucha energía.
Cuando estudiamos los gases, nos centramos en tres propiedades principales que están íntimamente relacionadas: presión, volumen y temperatura. Si modificamos una de estas propiedades, las otras también cambian siguiendo patrones muy precisos.
En esta unidad, descubriremos las leyes que gobiernan el comportamiento de los gases y aprenderemos a predecir qué sucederá cuando cambiamos alguna de sus propiedades. ¡Esto te ayudará a entender muchos fenómenos que ves todos los días!
💡 ¿Sabías que? Los globos aerostáticos funcionan gracias a las leyes de los gases: al calentar el aire de su interior, este se expande y se vuelve menos denso que el aire exterior, lo que hace que el globo se eleve.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Modelo cinético-corpuscular de los gases
Para entender bien cómo funcionan los gases, necesitamos conocer el modelo cinético-corpuscular. Según este modelo, los gases están formados por pequeñísimas partículas (átomos o moléculas) en constante movimiento, separadas por espacios vacíos.
Las partículas de los gases:
- Se mueven a gran velocidad y de forma desordenada
- Chocan entre sí y contra las paredes del recipiente
- Apenas tienen fuerzas de atracción entre ellas
La temperatura de un gas está directamente relacionada con la velocidad de sus partículas. Cuando calentamos un gas, sus partículas se mueven más rápido y tienen más energía cinética. Cuando lo enfriamos, ocurre lo contrario.
La presión es el resultado de las colisiones de las partículas contra las paredes del recipiente. Cuantas más colisiones y más fuertes sean, mayor será la presión. La presión depende de:
- La velocidad con que chocan las partículas
- El número de colisiones por segundo
Cuando modificamos el volumen de un recipiente con gas, cambiamos el espacio disponible para las partículas y, por tanto, la frecuencia de las colisiones y la presión.
🔬 Cuando inflas un globo y lo aprietas, reduces el espacio para las partículas de aire, aumentando las colisiones contra las paredes del globo y, por tanto, la presión.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La ley de Boyle y Mariotte
La primera ley de los gases que estudiaremos relaciona la presión y el volumen cuando la temperatura se mantiene constante.
La ley de Boyle y Mariotte establece que, a temperatura constante, la presión y el volumen de un gas son inversamente proporcionales. Esto significa que:
- Si el volumen aumenta, la presión disminuye
- Si el volumen disminuye, la presión aumenta
Matemáticamente lo expresamos como: P × V = constante
Por ejemplo, si duplicamos el volumen de un gas, su presión se reduce a la mitad. Si comprimimos un gas a un tercio de su volumen, su presión se triplica.
Según el modelo cinético-corpuscular, cuando reducimos el volumen de un gas:
- Las partículas tienen menos espacio para moverse
- Aumenta el número de colisiones con las paredes
- La presión aumenta
Al contrario, cuando aumentamos el volumen:
- Las partículas tienen más espacio
- Disminuye el número de colisiones
- La presión disminuye
Esta ley explica por qué cuando comprimes el émbolo de una jeringa tapada, se vuelve cada vez más difícil seguir empujando: ¡la presión del aire en el interior aumenta!
💡 Las ventosas se adhieren a las superficies gracias a la ley de Boyle y Mariotte. Al presionarlas, expulsan aire y crean un espacio con baja presión que hace que la presión atmosférica las mantenga pegadas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La ley de Gay-Lussac
La segunda ley que estudiaremos relaciona la temperatura y la presión cuando el volumen se mantiene constante.
La ley de Gay-Lussac establece que, a volumen constante, la presión y la temperatura de un gas son directamente proporcionales. Esto significa que:
- Si la temperatura aumenta, la presión también aumenta
- Si la temperatura disminuye, la presión también disminuye
Matemáticamente se expresa como: P/T = constante
Por ejemplo, si duplicamos la temperatura absoluta de un gas (en Kelvin), su presión también se duplicará. Si reducimos la temperatura a la mitad, la presión también se reducirá a la mitad.
Según el modelo cinético-corpuscular, cuando calentamos un gas en un recipiente cerrado de paredes rígidas:
- Las partículas se mueven más rápido
- Chocan con más fuerza contra las paredes
- La presión aumenta
Al enfriar el gas:
- Las partículas se mueven más lentamente
- Chocan con menos fuerza
- La presión disminuye
Es importante recordar que, para que esta ley se cumpla, la temperatura debe expresarse en la escala Kelvin (K), no en grados Celsius.
⚠️ Nunca expongas un bote de aerosol al calor. Al aumentar la temperatura, la presión interior aumenta y podría explotar. Por la misma razón, debes revisar la presión de los neumáticos de tu bici después de circular en un día caluroso.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La ley de Charles y Gay-Lussac
La tercera ley relaciona la temperatura y el volumen cuando la presión se mantiene constante.
La ley de Charles y Gay-Lussac establece que, a presión constante, el volumen y la temperatura de un gas son directamente proporcionales. Esto significa que:
- Si la temperatura aumenta, el volumen también aumenta
- Si la temperatura disminuye, el volumen también disminuye
Matemáticamente se expresa como: V/T = constante
Por ejemplo, si aumentamos la temperatura absoluta de un gas un 20%, su volumen también aumentará un 20%, siempre que la presión se mantenga constante.
Según el modelo cinético-corpuscular, cuando calentamos un gas en un recipiente con una pared móvil (como un émbolo):
- Las partículas se mueven más rápido
- Chocan con más fuerza contra el émbolo
- El émbolo se desplaza y el volumen aumenta
Al enfriar el gas:
- Las partículas se mueven más lentamente
- Ejercen menos fuerza sobre el émbolo
- El gas se comprime y el volumen disminuye
Como en la ley de Gay-Lussac, la temperatura debe expresarse en Kelvin para que se cumpla esta relación.
🎈 ¿Has notado que un globo se desinfla cuando lo metes en el frigorífico? Esto ocurre porque, al disminuir la temperatura, el volumen del aire en su interior también disminuye según la ley de Charles y Gay-Lussac.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Límites de las leyes de los gases y el cero absoluto
Las leyes que hemos estudiado funcionan muy bien en condiciones normales, pero tienen sus límites. Se cumplen cuando las partículas de gas se mueven libremente e independientemente unas de otras, lo que se conoce como comportamiento de gas ideal.
Sin embargo, las leyes de los gases pueden fallar en estas condiciones:
-
Temperaturas muy bajas: Cuando un gas se enfría mucho, las partículas se mueven tan lentamente que empiezan a atraerse entre sí, pudiendo condensarse en líquido o solidificarse.
-
Presiones muy altas: Cuando comprimimos mucho un gas, las partículas están tan cerca que las fuerzas entre ellas se vuelven importantes y ya no se comportan independientemente.
Otro aspecto interesante es el punto de ebullición. La temperatura a la que hierve un líquido depende de la presión:
- A mayor presión, mayor punto de ebullición
- A menor presión, menor punto de ebullición
Por eso, en la cima de una montaña (donde la presión atmosférica es menor), el agua hierve a menos de 100°C, lo que dificulta cocinar alimentos.
Las leyes de los gases nos llevan al concepto del cero absoluto , la temperatura teórica más baja posible. A esta temperatura, las partículas de gas tendrían la mínima energía posible. En la práctica, es imposible alcanzar exactamente el cero absoluto.
🌡️ En la cima del Everest, a 8.848 metros de altitud y con una presión atmosférica de sólo 0,34 atm, el agua hierve a apenas 71°C. ¡Preparar un té caliente sería todo un desafío!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Aplicaciones prácticas de las leyes de los gases
Las leyes de los gases no son solo teorías abstractas; explican numerosos fenómenos cotidianos y tienen aplicaciones muy importantes.
Aplicaciones en la vida diaria:
- Neumáticos de vehículos: La presión aumenta cuando se calientan al circular, por eso es importante revisarla cuando están fríos.
- Ollas a presión: Aumentan el punto de ebullición del agua, cocinando los alimentos más rápido.
- Globos aerostáticos: Se elevan porque el aire caliente del interior ocupa más volumen y es menos denso que el aire exterior.
- Buceo: Los tanques de aire comprimido permiten llevar mucho aire en poco espacio.
En el laboratorio:
- Jeringuillas: Son herramientas perfectas para demostrar la relación entre presión y volumen.
- Manómetros: Miden la presión de gases en recipientes cerrados.
- Termómetros de gas: Utilizan la expansión de gases para medir temperaturas.
En la industria:
- Refrigeración: Los refrigeradores aprovechan los cambios de presión para alterar la temperatura de los gases refrigerantes.
- Motores de combustión interna: Funcionan gracias a la expansión de gases calientes.
- Generación de electricidad: Muchas centrales eléctricas utilizan vapor a presión para mover turbinas.
Entender estas leyes nos ayuda a diseñar mejor muchos dispositivos y a predecir cómo se comportarán los gases en diferentes situaciones.
🚗 Cuando inflas las ruedas de tu bici o coche en invierno y luego hace mucho calor, la presión puede aumentar tanto que podrían dañarse. Siempre revisa la presión con cambios de temperatura significativos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: termodinámica de los gases
8Leyes de los gases
Ley de clapeyron, ley de gay lussac , ley de charles y ley de boyle mariotte
Gases y disoluciones
3° ESO
Leyes de los gases
Las tres leyes
Teoría Cinética y Leyes de los Gases
Resumen sobre la Teoría Cinética y Leyes de los Gases
Los Gases 3ro ESO
Tema de los gases física y quimica
Leyes Y conceptos básicos en química
Apuntes del profesor de la asignatura
Leyes de los Gases
Este artículo explora las leyes de los gases, incluyendo la ley de Charles y la ley de Gay-Lussac, y su relación con la presión, volumen y temperatura.
Propiedades de los gases.
Unidades de los gases. Ley de Boyle Mariotte, ley de Gay-Lussac y Charles.
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.