¿Te lías con "que" y "de que"? ¿Te parece imposible... Mostrar más
La Teoría Atómica de Dalton y las Partículas Fundamentales del Átomo










Uso correcto de "que" y "de que" + Teoría atómica de Dalton
El truco infalible para "que" vs "de que": convierte la frase en pregunta. Si la pregunta lleva "de", tu frase también. Por ejemplo: "Estoy seguro de que llueve" → ¿De qué estoy seguro? Pero "Me dijo que llueve" → ¿Qué me dijo?
Los antiguos griegos ya debatían sobre la teoría atomista. Leucipo y Demócrito creían que todo estaba hecho de átomos (partículas súper pequeñas), pero Platón y Aristóteles pensaban que la materia era continua y se podía dividir infinitamente.
En 1808, John Dalton retomó la idea atomista con tres postulados clave: la materia está hecha de átomos indivisibles, todos los átomos de un elemento son iguales, y los compuestos se forman combinando átomos diferentes en proporciones fijas.
💡 Dato curioso: El agua siempre tiene 2 átomos de hidrógeno y 1 de oxígeno, da igual si viene del Ártico o del Caribe.

Clasificación de la materia según Dalton
Los elementos son sustancias con átomos idénticos (como el oxígeno). Los compuestos tienen átomos diferentes combinados (como el agua). Las mezclas son combinaciones de sustancias diferentes (como el aire).
La teoría de Dalton explica por qué existen tantos compuestos químicos. Es como formar palabras con letras: con unas pocas letras puedes crear miles de palabras diferentes. Con pocos elementos químicos, la naturaleza crea infinidad de compuestos.
Dos elementos pueden combinarse de formas diferentes. El carbono y el oxígeno forman dos compuestos distintos: CO (monóxido de carbono, súper tóxico) y CO₂ (dióxido de carbono, el de las bebidas con gas).
Dalton creó símbolos especiales para cada elemento, pero ahora usamos los de la tabla periódica que conoces.
⚗️ Para el examen: Recuerda que un elemento = átomos iguales, un compuesto = átomos diferentes en proporciones fijas.

Naturaleza eléctrica de la materia
¿Has notado que se te pega el pelo al quitarte un jersey? ¿O que al frotar un globo se pega a la pared? Todo esto pasa por la carga eléctrica, una propiedad fundamental de la materia.
Existen dos tipos de fenómenos eléctricos: atracción y repulsión. Los científicos explican esto con dos tipos de carga eléctrica: positiva y negativa. La regla es simple: cargas iguales se repelen, cargas diferentes se atraen.
Normalmente la materia es eléctricamente neutra (tiene la misma cantidad de carga positiva y negativa). Solo cuando tiene más de un tipo que del otro es cuando vemos efectos eléctricos, como los rayos en las tormentas.
La unidad de carga eléctrica es el culombio (C), aunque a escala atómica se usa la carga elemental porque el culombio es enorme.
⚡ Dato flipante: Para sumar un culombio necesitas juntar 624.000.000.000.000.000 electrones. ¡Por eso es mejor usar otras unidades!

Descubrimiento de las partículas atómicas
A finales del siglo XIX surgió una pregunta clave: si los átomos son indivisibles según Dalton, ¿cómo pueden ganar o perder carga eléctrica? La respuesta cambió la ciencia para siempre.
J.J. Thomson en 1897 descubrió el electrón usando tubos de descarga. Estos tubos tenían gas a baja presión y dos placas metálicas. Al aplicar voltaje, aparecía un rayo luminoso (los rayos catódicos) que iba del polo negativo al positivo.
Thomson demostró que estos rayos eran partículas con carga negativa presentes en todos los átomos. Como tenían masa, podían mover objetos. Como tenían carga negativa, se desviaban hacia las placas positivas.
El descubrimiento fue revolucionario: todos los átomos contienen electrones, partículas cargadas negativamente. Esto significaba que los átomos sí eran divisibles, contradiciendo a Dalton.
🔬 Experimento clave: Los rayos catódicos se comportaban igual sin importar qué gas hubiera en el tubo, demostrando que los electrones están en todos los átomos.

Protones, neutrones y modelos atómicos
Como la materia es neutra, si tiene electrones (carga negativa), debe tener algo con carga positiva para compensar. Ernest Rutherford descubrió el protón: misma carga que el electrón pero positiva, y 1840 veces más masivo.
James Chadwick en 1931 completó el puzzle descubriendo el neutrón: sin carga eléctrica pero con masa similar al protón. Ya teníamos las tres partículas fundamentales del átomo.
Con estos descubrimientos, los científicos crearon modelos atómicos para explicar cómo se organizan estas partículas. Thomson propuso el modelo del "bizcocho con pasas": una gran esfera positiva con electrones incrustados, como pasas en un bizcocho.
Sin embargo, este modelo no duró mucho. Los experimentos de Rutherford demostraron que la realidad era muy diferente.
📊 Datos importantes: Protón = +1 carga, masa 1u; Electrón = -1 carga, masa 1/1840 u; Neutrón = 0 carga, masa 1u.

El revolucionario modelo de Rutherford
Rutherford diseñó un experimento genial: lanzar partículas positivas contra una lámina de oro súper fina. Según el modelo de Thomson, todas deberían pasar sin desviarse mucho. Pero la realidad fue otra.
La mayoría de partículas atravesaban la lámina, pero algunas (1 de cada 10.000) rebotaban completamente. Era como si una pelota de ping-pong rebotara contra una hoja de papel. ¡Imposible con el modelo de Thomson!
Rutherford concluyó que casi toda la masa del átomo estaba concentrada en un punto minúsculo: el núcleo atómico. El resto del átomo estaba prácticamente vacío, con electrones girando alrededor del núcleo como planetas alrededor del Sol.
El modelo de Rutherford establece que los átomos tienen dos zonas: el núcleo (contiene protones y neutrones, casi toda la masa) y la corteza electrónica (donde giran los electrones a gran distancia).
🏟️ Para visualizarlo: Si el átomo fuera un estadio de fútbol, el núcleo sería como un guisante en el centro del campo. ¡El resto sería espacio vacío!

Número atómico, número másico e isótopos
Para identificar cualquier átomo necesitas dos números súper importantes. El número atómico (Z) es el número de protones que tiene un átomo. Cada elemento químico se caracteriza por tener siempre el mismo Z.
El número másico (A) es la suma de protones y neutrones en el núcleo. Para calcular los neutrones usas la fórmula: N = A - Z.
Cualquier átomo se representa como ᴬzX. Por ejemplo, el ¹⁶₈O tiene 8 protones, 8 electrones (en átomos neutros) y 8 neutrones (16-8=8).
Los isótopos son átomos del mismo elemento (mismo Z) pero con diferente número de neutrones (diferente A). El cloro-35 y el cloro-37 son isótopos: ambos tienen 17 protones pero diferentes neutrones.
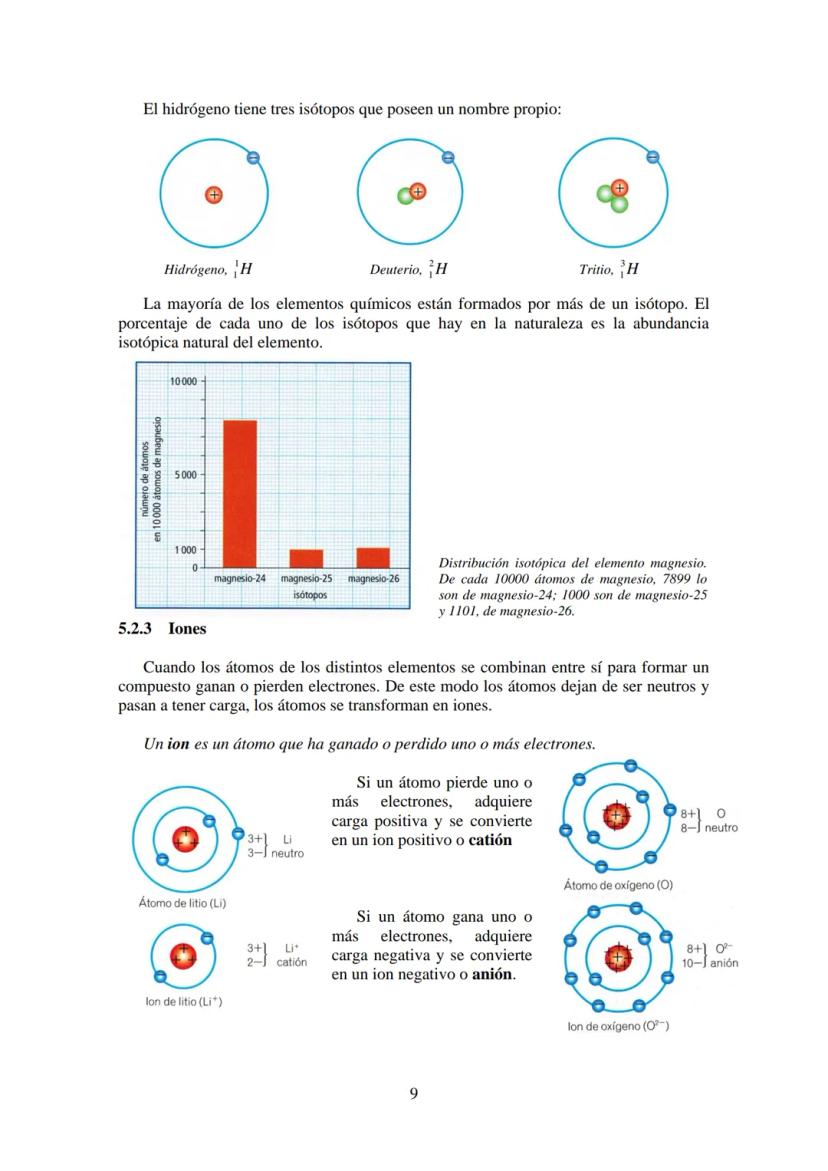
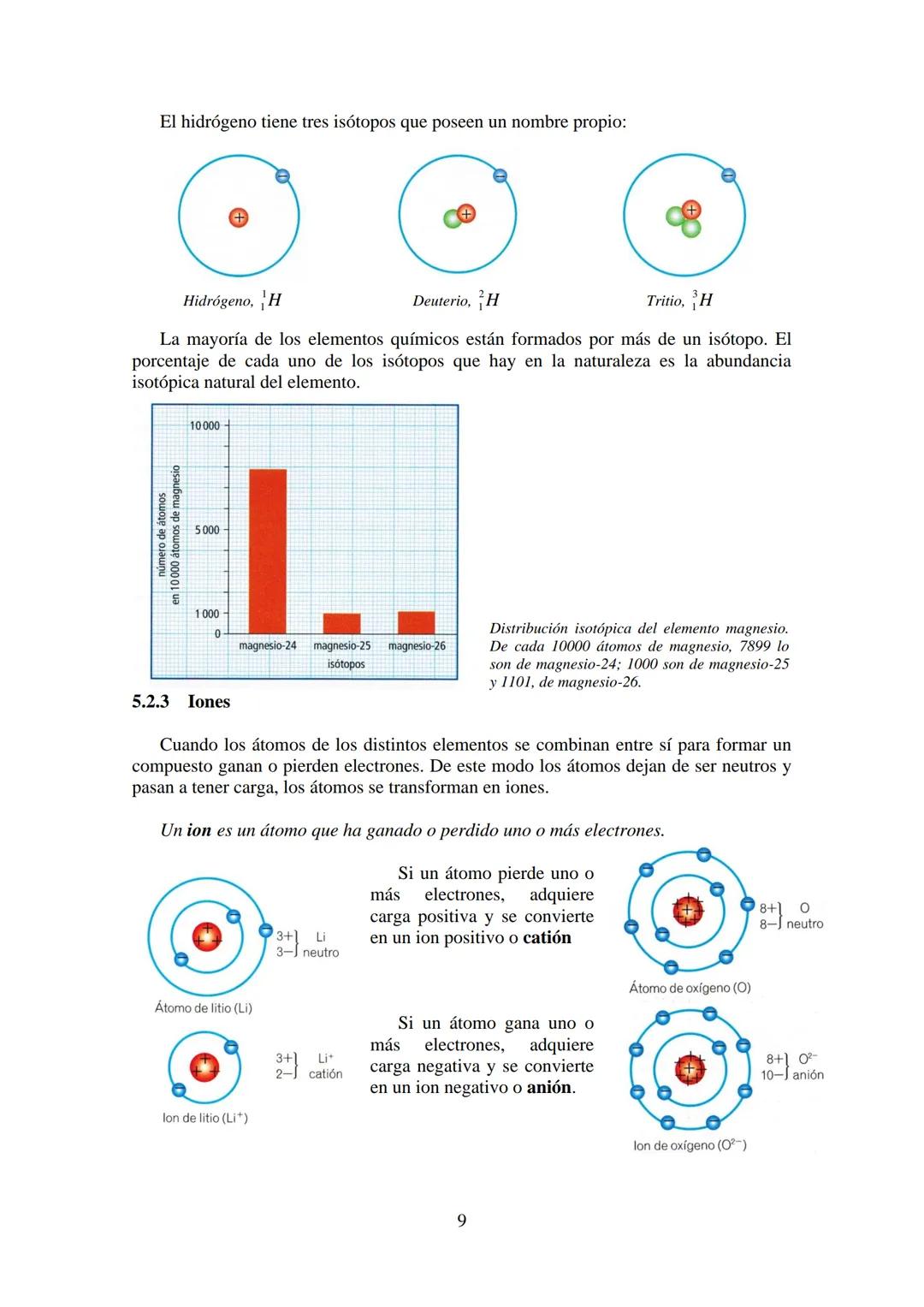
🧪 Ejemplo práctico: El hidrógeno tiene tres isótopos con nombres propios: hidrógeno normal (1 protón), deuterio y tritio .

Abundancia isotópica e iones
La mayoría de elementos naturales son mezclas de varios isótopos. La abundancia isotópica te dice qué porcentaje de cada isótopo hay en la naturaleza. Por ejemplo, de cada 10.000 átomos de magnesio, 7.899 son magnesio-24.
Cuando los átomos se combinan para formar compuestos, pueden ganar o perder electrones. Entonces dejan de ser neutros y se convierten en iones.
Si un átomo pierde electrones, queda con más protones que electrones, así que tiene carga positiva. Se llama catión (como Li⁺). Si gana electrones, tiene más electrones que protones y queda con carga negativa. Se llama anión (como O²⁻).
Los protones nunca cambian en los procesos químicos normales, solo los electrones. Por eso el número atómico siempre identifica al elemento, tenga la carga que tenga.
⚡ Truco para recordar: CATión = CArga posiTiva (perdió electrones), ANión = cArga Negativa (ganó electrones).
El modelo atómico de Bohr
El modelo de Rutherford tenía problemas serios. Según la física clásica, los electrones girando alrededor del núcleo deberían perder energía continuamente y acabar cayendo al núcleo. Además, no explicaba por qué los átomos emiten solo ciertas energías específicas cuando se calientan.
Niels Bohr en 1913 propuso un modelo revolucionario que rompía con la física tradicional. Su idea fundamental: los electrones solo pueden moverse en órbitas específicas, como si fueran escalones de una escalera energética.
En estas órbitas permitidas, el electrón no emite energía aunque esté girando (algo imposible según la física clásica). Cada órbita tiene una energía fija: cuanto más cerca del núcleo, menor energía.
Cuando un electrón salta de una órbita a otra, absorbe o emite exactamente la diferencia de energía entre ambas órbitas. Esto explicaba perfectamente los espectros atómicos observados experimentalmente.
🎯 La clave: Bohr introdujo la idea de que a escala atómica las reglas son diferentes. Esta idea fue fundamental para el desarrollo de la mecánica cuántica.

Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: partículas atómicas
9El átomo
El átomo
Tabla Periódica Frases
Frases de algunas columnas para ayudar a memorizar la tabla periódica
Propiedades periódicas
Apuntes propiedades periódicas 1bach, las actividades son de emestrada.
Enlaces químicos, uniones intermoleculares, reacciones químicas e industria química.
Apunets sobre los enlaces químicos y sus tipos, las uniones intermoleculares, reacciones químicas con sus procesos y factores e información y estaciones en la industria química.
Identificación de Átomos: Número Atómico
El número atómico y el número másico son clave para diferenciar átomos de distintos elementos. Ejemplo con el sodio.
Tabla periódica (solo los símbolos químicos y sus nombres 🕺🏼🕺🏼🕺🏼
Faltan algún ya que esos son los que pidió mi profesor espero ayudar 😰😰😰
El enlace químico
Profundizamos en el enlace químico
La jerga química: formulación inorgánica
LA JERGA QUÍMICA: FORMULACIÓN INORGÁNICA
Peroxidos
Formulación
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
La Teoría Atómica de Dalton y las Partículas Fundamentales del Átomo
¿Te lías con "que" y "de que"? ¿Te parece imposible entender cómo funciona la materia a nivel atómico? Tranquilo, que no es tan complicado como parece. Aquí tienes todo lo que necesitas saber sobre gramática española y teoría atómica de... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Uso correcto de "que" y "de que" + Teoría atómica de Dalton
El truco infalible para "que" vs "de que": convierte la frase en pregunta. Si la pregunta lleva "de", tu frase también. Por ejemplo: "Estoy seguro de que llueve" → ¿De qué estoy seguro? Pero "Me dijo que llueve" → ¿Qué me dijo?
Los antiguos griegos ya debatían sobre la teoría atomista. Leucipo y Demócrito creían que todo estaba hecho de átomos (partículas súper pequeñas), pero Platón y Aristóteles pensaban que la materia era continua y se podía dividir infinitamente.
En 1808, John Dalton retomó la idea atomista con tres postulados clave: la materia está hecha de átomos indivisibles, todos los átomos de un elemento son iguales, y los compuestos se forman combinando átomos diferentes en proporciones fijas.
💡 Dato curioso: El agua siempre tiene 2 átomos de hidrógeno y 1 de oxígeno, da igual si viene del Ártico o del Caribe.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Clasificación de la materia según Dalton
Los elementos son sustancias con átomos idénticos (como el oxígeno). Los compuestos tienen átomos diferentes combinados (como el agua). Las mezclas son combinaciones de sustancias diferentes (como el aire).
La teoría de Dalton explica por qué existen tantos compuestos químicos. Es como formar palabras con letras: con unas pocas letras puedes crear miles de palabras diferentes. Con pocos elementos químicos, la naturaleza crea infinidad de compuestos.
Dos elementos pueden combinarse de formas diferentes. El carbono y el oxígeno forman dos compuestos distintos: CO (monóxido de carbono, súper tóxico) y CO₂ (dióxido de carbono, el de las bebidas con gas).
Dalton creó símbolos especiales para cada elemento, pero ahora usamos los de la tabla periódica que conoces.
⚗️ Para el examen: Recuerda que un elemento = átomos iguales, un compuesto = átomos diferentes en proporciones fijas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Naturaleza eléctrica de la materia
¿Has notado que se te pega el pelo al quitarte un jersey? ¿O que al frotar un globo se pega a la pared? Todo esto pasa por la carga eléctrica, una propiedad fundamental de la materia.
Existen dos tipos de fenómenos eléctricos: atracción y repulsión. Los científicos explican esto con dos tipos de carga eléctrica: positiva y negativa. La regla es simple: cargas iguales se repelen, cargas diferentes se atraen.
Normalmente la materia es eléctricamente neutra (tiene la misma cantidad de carga positiva y negativa). Solo cuando tiene más de un tipo que del otro es cuando vemos efectos eléctricos, como los rayos en las tormentas.
La unidad de carga eléctrica es el culombio (C), aunque a escala atómica se usa la carga elemental porque el culombio es enorme.
⚡ Dato flipante: Para sumar un culombio necesitas juntar 624.000.000.000.000.000 electrones. ¡Por eso es mejor usar otras unidades!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Descubrimiento de las partículas atómicas
A finales del siglo XIX surgió una pregunta clave: si los átomos son indivisibles según Dalton, ¿cómo pueden ganar o perder carga eléctrica? La respuesta cambió la ciencia para siempre.
J.J. Thomson en 1897 descubrió el electrón usando tubos de descarga. Estos tubos tenían gas a baja presión y dos placas metálicas. Al aplicar voltaje, aparecía un rayo luminoso (los rayos catódicos) que iba del polo negativo al positivo.
Thomson demostró que estos rayos eran partículas con carga negativa presentes en todos los átomos. Como tenían masa, podían mover objetos. Como tenían carga negativa, se desviaban hacia las placas positivas.
El descubrimiento fue revolucionario: todos los átomos contienen electrones, partículas cargadas negativamente. Esto significaba que los átomos sí eran divisibles, contradiciendo a Dalton.
🔬 Experimento clave: Los rayos catódicos se comportaban igual sin importar qué gas hubiera en el tubo, demostrando que los electrones están en todos los átomos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Protones, neutrones y modelos atómicos
Como la materia es neutra, si tiene electrones (carga negativa), debe tener algo con carga positiva para compensar. Ernest Rutherford descubrió el protón: misma carga que el electrón pero positiva, y 1840 veces más masivo.
James Chadwick en 1931 completó el puzzle descubriendo el neutrón: sin carga eléctrica pero con masa similar al protón. Ya teníamos las tres partículas fundamentales del átomo.
Con estos descubrimientos, los científicos crearon modelos atómicos para explicar cómo se organizan estas partículas. Thomson propuso el modelo del "bizcocho con pasas": una gran esfera positiva con electrones incrustados, como pasas en un bizcocho.
Sin embargo, este modelo no duró mucho. Los experimentos de Rutherford demostraron que la realidad era muy diferente.
📊 Datos importantes: Protón = +1 carga, masa 1u; Electrón = -1 carga, masa 1/1840 u; Neutrón = 0 carga, masa 1u.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El revolucionario modelo de Rutherford
Rutherford diseñó un experimento genial: lanzar partículas positivas contra una lámina de oro súper fina. Según el modelo de Thomson, todas deberían pasar sin desviarse mucho. Pero la realidad fue otra.
La mayoría de partículas atravesaban la lámina, pero algunas (1 de cada 10.000) rebotaban completamente. Era como si una pelota de ping-pong rebotara contra una hoja de papel. ¡Imposible con el modelo de Thomson!
Rutherford concluyó que casi toda la masa del átomo estaba concentrada en un punto minúsculo: el núcleo atómico. El resto del átomo estaba prácticamente vacío, con electrones girando alrededor del núcleo como planetas alrededor del Sol.
El modelo de Rutherford establece que los átomos tienen dos zonas: el núcleo (contiene protones y neutrones, casi toda la masa) y la corteza electrónica (donde giran los electrones a gran distancia).
🏟️ Para visualizarlo: Si el átomo fuera un estadio de fútbol, el núcleo sería como un guisante en el centro del campo. ¡El resto sería espacio vacío!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Número atómico, número másico e isótopos
Para identificar cualquier átomo necesitas dos números súper importantes. El número atómico (Z) es el número de protones que tiene un átomo. Cada elemento químico se caracteriza por tener siempre el mismo Z.
El número másico (A) es la suma de protones y neutrones en el núcleo. Para calcular los neutrones usas la fórmula: N = A - Z.
Cualquier átomo se representa como ᴬzX. Por ejemplo, el ¹⁶₈O tiene 8 protones, 8 electrones (en átomos neutros) y 8 neutrones (16-8=8).
Los isótopos son átomos del mismo elemento (mismo Z) pero con diferente número de neutrones (diferente A). El cloro-35 y el cloro-37 son isótopos: ambos tienen 17 protones pero diferentes neutrones.
🧪 Ejemplo práctico: El hidrógeno tiene tres isótopos con nombres propios: hidrógeno normal (1 protón), deuterio y tritio .

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Abundancia isotópica e iones
La mayoría de elementos naturales son mezclas de varios isótopos. La abundancia isotópica te dice qué porcentaje de cada isótopo hay en la naturaleza. Por ejemplo, de cada 10.000 átomos de magnesio, 7.899 son magnesio-24.
Cuando los átomos se combinan para formar compuestos, pueden ganar o perder electrones. Entonces dejan de ser neutros y se convierten en iones.
Si un átomo pierde electrones, queda con más protones que electrones, así que tiene carga positiva. Se llama catión (como Li⁺). Si gana electrones, tiene más electrones que protones y queda con carga negativa. Se llama anión (como O²⁻).
Los protones nunca cambian en los procesos químicos normales, solo los electrones. Por eso el número atómico siempre identifica al elemento, tenga la carga que tenga.
⚡ Truco para recordar: CATión = CArga posiTiva (perdió electrones), ANión = cArga Negativa (ganó electrones).

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El modelo atómico de Bohr
El modelo de Rutherford tenía problemas serios. Según la física clásica, los electrones girando alrededor del núcleo deberían perder energía continuamente y acabar cayendo al núcleo. Además, no explicaba por qué los átomos emiten solo ciertas energías específicas cuando se calientan.
Niels Bohr en 1913 propuso un modelo revolucionario que rompía con la física tradicional. Su idea fundamental: los electrones solo pueden moverse en órbitas específicas, como si fueran escalones de una escalera energética.
En estas órbitas permitidas, el electrón no emite energía aunque esté girando (algo imposible según la física clásica). Cada órbita tiene una energía fija: cuanto más cerca del núcleo, menor energía.
Cuando un electrón salta de una órbita a otra, absorbe o emite exactamente la diferencia de energía entre ambas órbitas. Esto explicaba perfectamente los espectros atómicos observados experimentalmente.
🎯 La clave: Bohr introdujo la idea de que a escala atómica las reglas son diferentes. Esta idea fue fundamental para el desarrollo de la mecánica cuántica.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: partículas atómicas
9El átomo
El átomo
Tabla Periódica Frases
Frases de algunas columnas para ayudar a memorizar la tabla periódica
Propiedades periódicas
Apuntes propiedades periódicas 1bach, las actividades son de emestrada.
Enlaces químicos, uniones intermoleculares, reacciones químicas e industria química.
Apunets sobre los enlaces químicos y sus tipos, las uniones intermoleculares, reacciones químicas con sus procesos y factores e información y estaciones en la industria química.
Identificación de Átomos: Número Atómico
El número atómico y el número másico son clave para diferenciar átomos de distintos elementos. Ejemplo con el sodio.
Tabla periódica (solo los símbolos químicos y sus nombres 🕺🏼🕺🏼🕺🏼
Faltan algún ya que esos son los que pidió mi profesor espero ayudar 😰😰😰
El enlace químico
Profundizamos en el enlace químico
La jerga química: formulación inorgánica
LA JERGA QUÍMICA: FORMULACIÓN INORGÁNICA
Peroxidos
Formulación
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.