¿Te parece complicado nombrar compuestos químicos como el "monóxido de... Mostrar más
Guía Completa de Formulación Inorgánica



Introducción a la Formulación Inorgánica
¿Sabías que dominar la formulación inorgánica es como tener un superpoder en química? Te permite entender exactamente qué elementos forman cada compuesto y en qué proporciones.
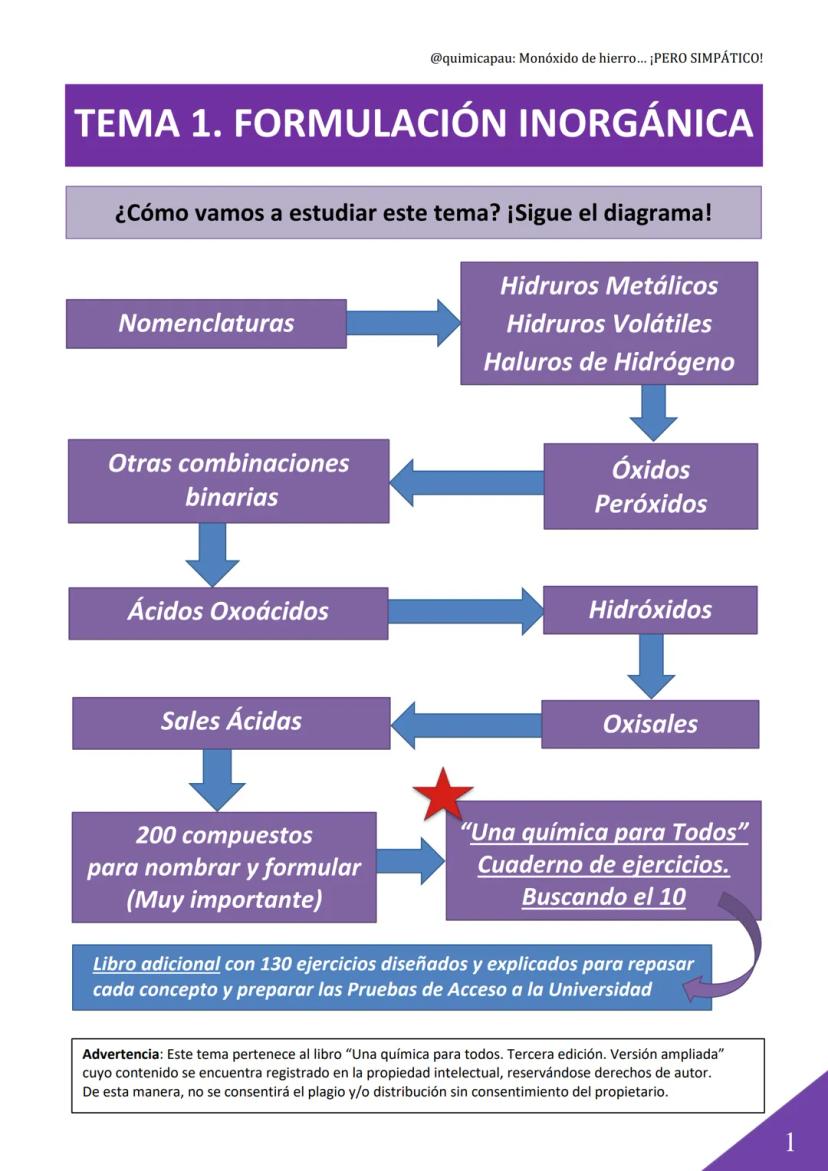
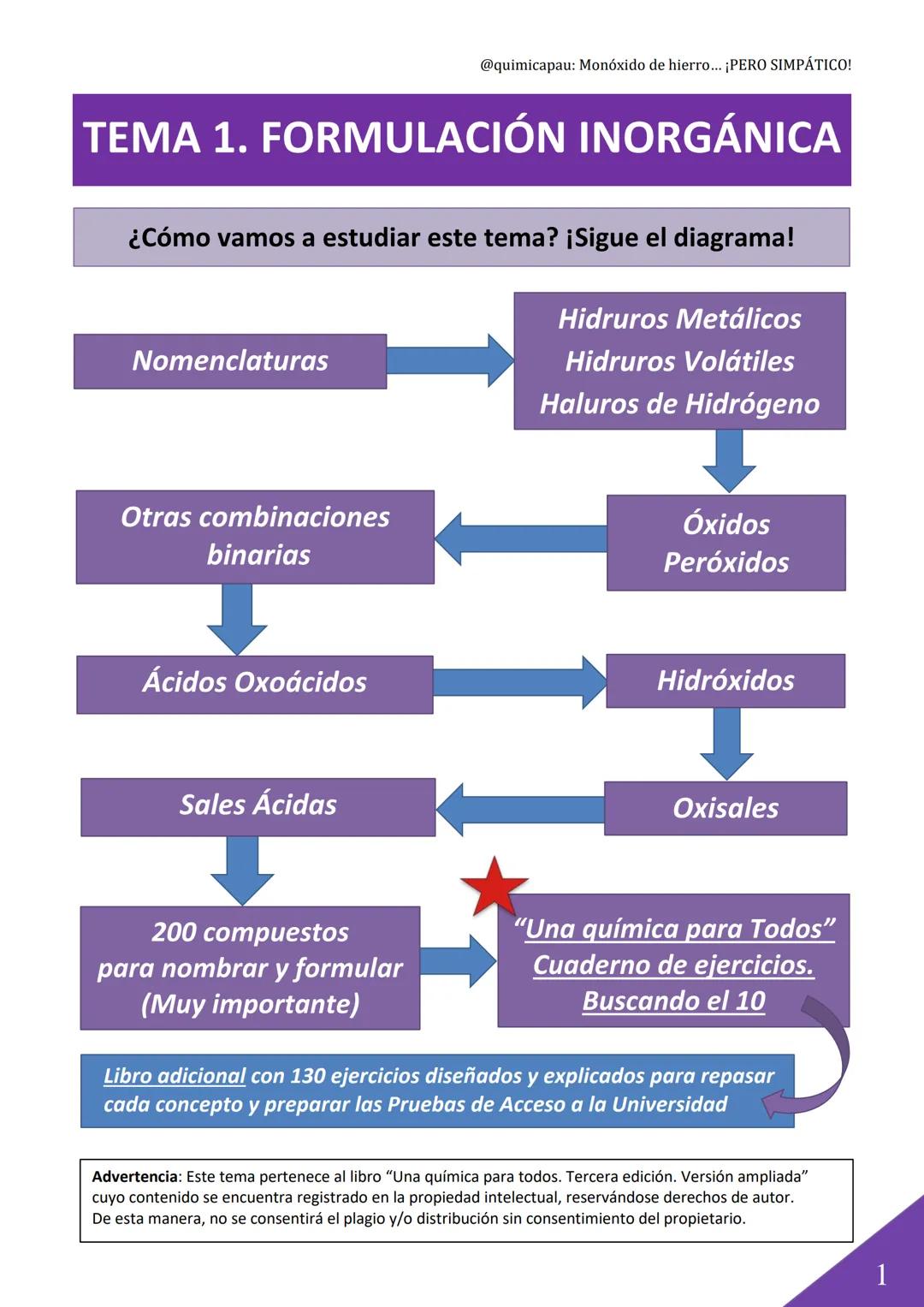
Este tema cubre todos los tipos de compuestos que necesitas conocer: desde los hidruros metálicos más sencillos hasta las oxisales más complejas. El objetivo es que puedas formular y nombrar 200 compuestos diferentes usando las tres nomenclaturas principales.
Las tres formas de nombrar compuestos son: la nomenclatura de composición , la nomenclatura con números de oxidación (usando números romanos) y la nomenclatura tradicional . Cada una tiene sus ventajas según el tipo de compuesto.
¡Truco importante! No intentes memorizar todos los nombres de golpe. Practica grupo por grupo y verás cómo cada tipo sigue un patrón lógico.

Combinaciones Binarias del Hidrógeno
Los hidruros metálicos son súper fáciles una vez que entiendes el truco. Se forman combinando un metal con hidrógeno, donde el hidrógeno siempre actúa con valencia -1.
Para formular hidruros como el hidruro de aluminio (AlH₃), simplemente cruza las valencias: el aluminio tiene valencia +3, el hidrógeno -1, así que necesitas 3 átomos de hidrógeno por cada aluminio. ¡Así de simple!
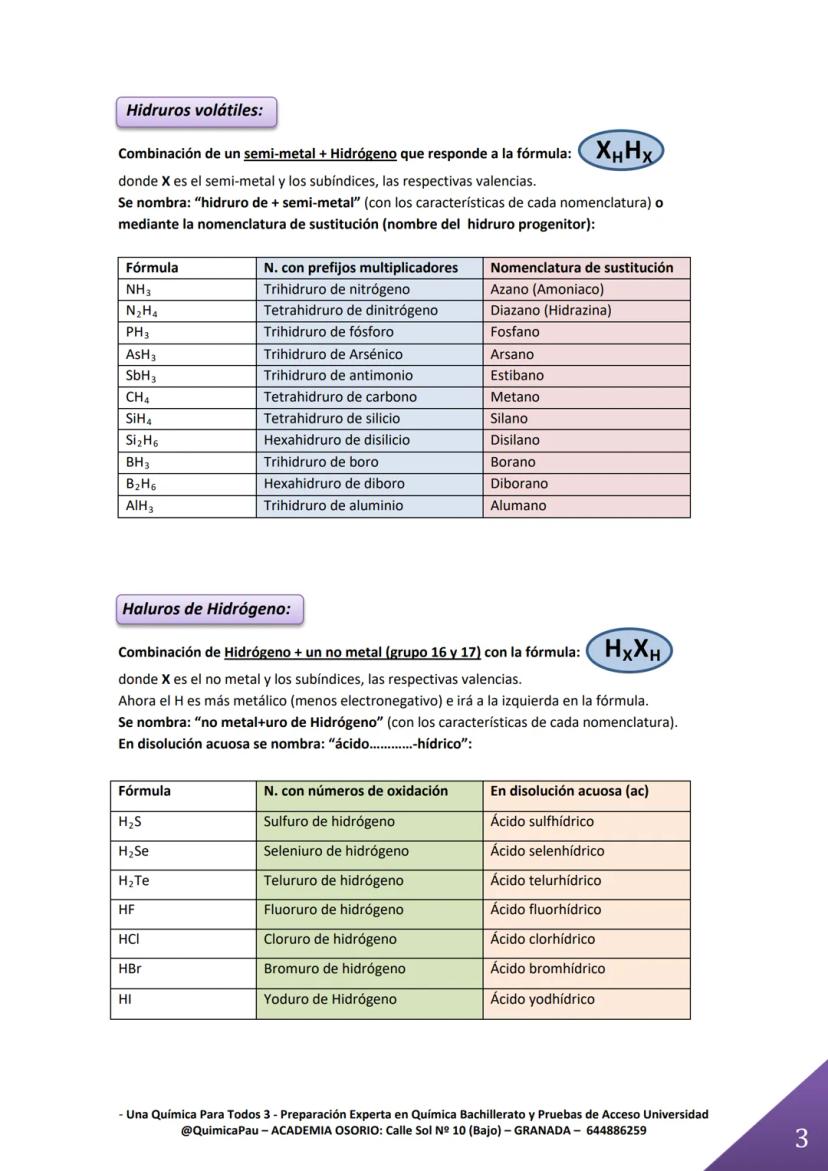
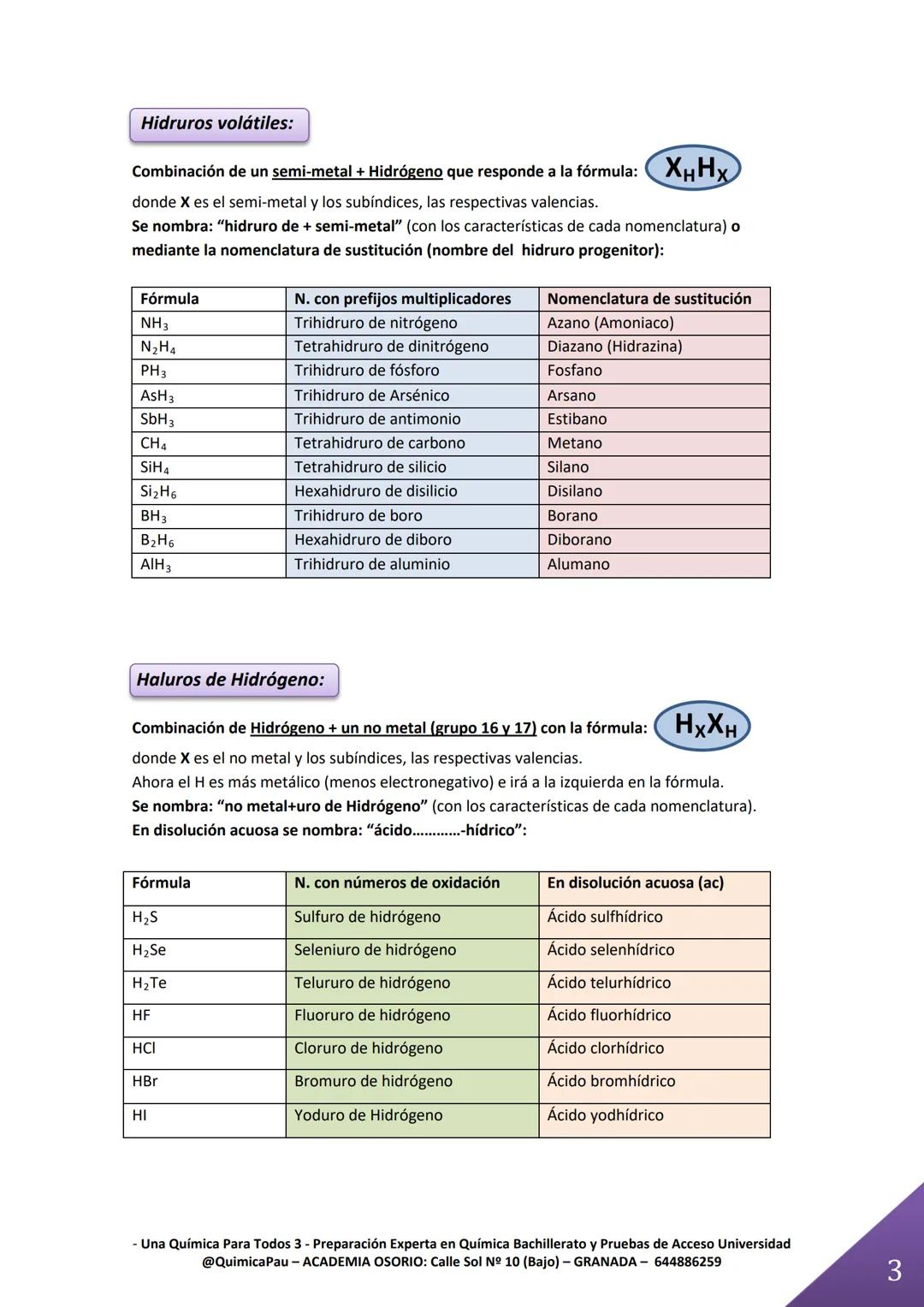
Los hidruros volátiles son diferentes porque se forman con semimetales. Aquí puedes usar nombres especiales como "amoniaco" para NH₃ o "metano" para CH₄. Estos nombres especiales se llaman nomenclatura de sustitución.
Los haluros de hidrógeno cambian completamente cuando los disuelves en agua. Por ejemplo, HCl gaseoso se llama "cloruro de hidrógeno", pero en disolución acuosa se convierte en "ácido clorhídrico".
¡Ojo! Cuando el hidrógeno se combina con elementos del grupo 16 y 17, el hidrógeno va a la izquierda en la fórmula porque es menos electronegativo.
Combinaciones Binarias del Oxígeno
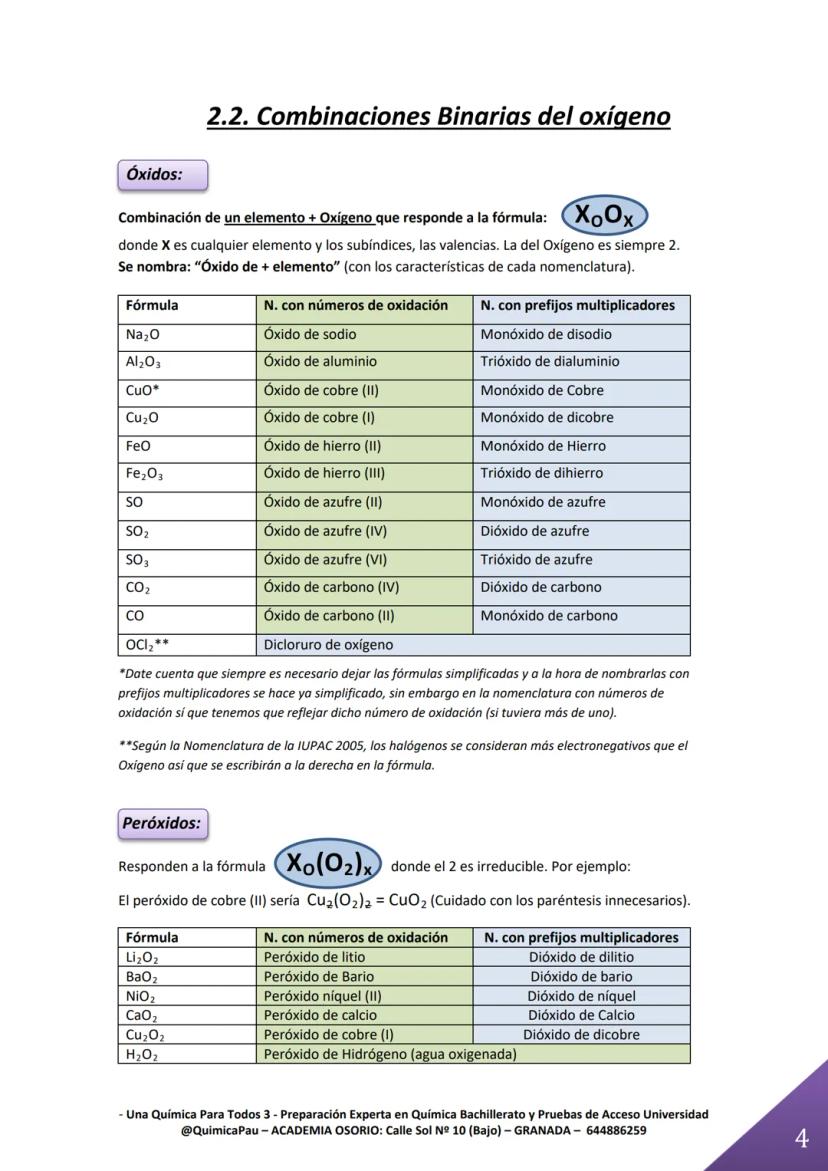
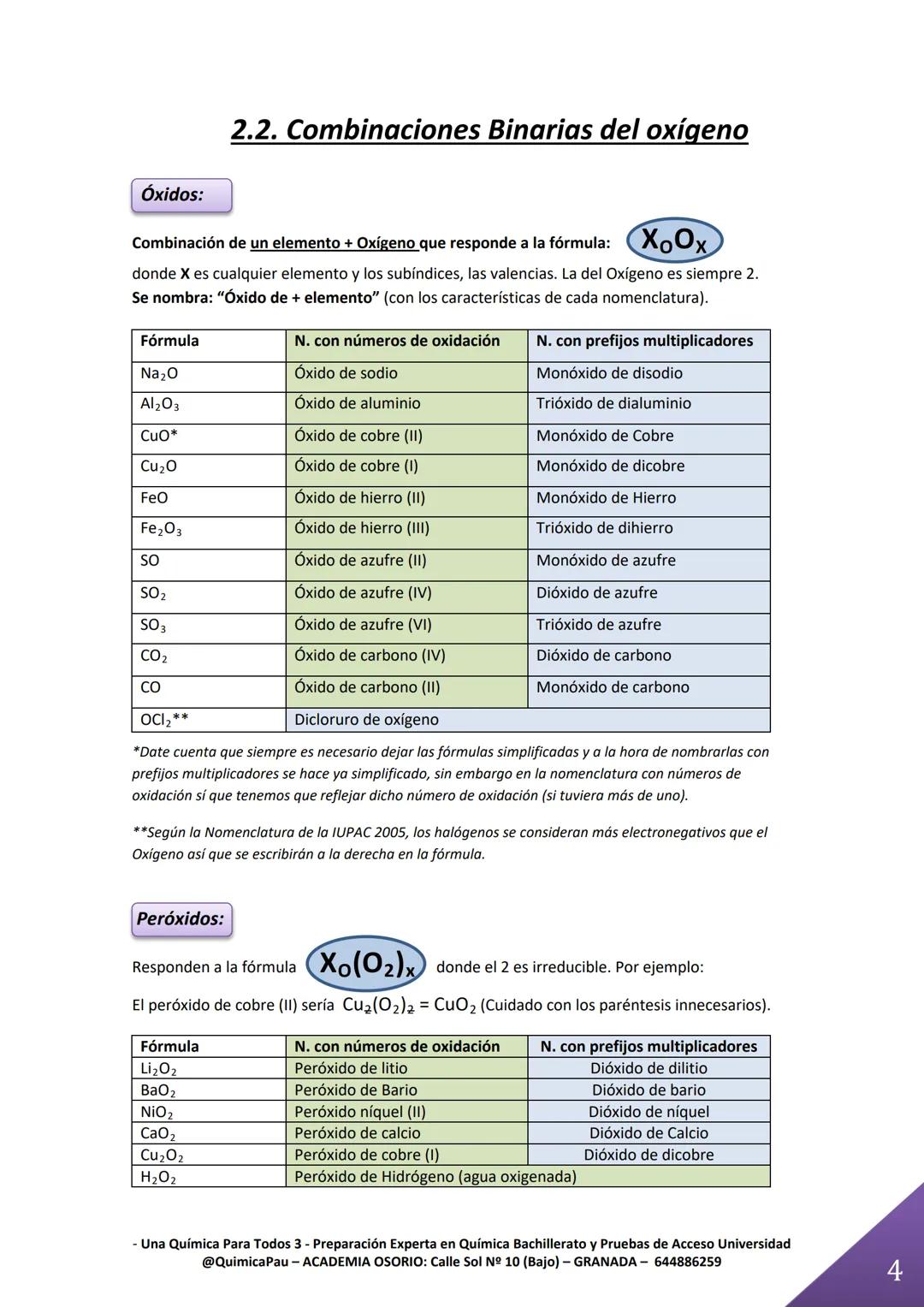
Los óxidos son como los hidruros pero con oxígeno, que siempre tiene valencia -2. Son súper importantes porque forman la base para muchos otros compuestos más complejos.
La clave está en simplificar siempre las fórmulas. Por ejemplo, Cu₂O₂ se simplifica a CuO. Pero cuidado: cuando uses prefijos multiplicadores, usa la fórmula ya simplificada, mientras que con números de oxidación debes indicar la valencia real del metal.
Los peróxidos son especiales porque contienen el grupo O₂²⁻ que no se puede separar. Por eso el peróxido de hidrógeno es H₂O₂ y no se simplifica. Reconócelos por la fórmula característica X(O₂).
Un truco genial: en algunos casos como OCl₂, el cloro va a la derecha porque es más electronegativo que el oxígeno. ¡La electronegatividad manda en las fórmulas!
¡Truco de oro! Para saber si es un óxido normal o un peróxido, fíjate en si puedes simplificar la fórmula. Si no puedes, probablemente sea un peróxido.
Otras Combinaciones Binarias
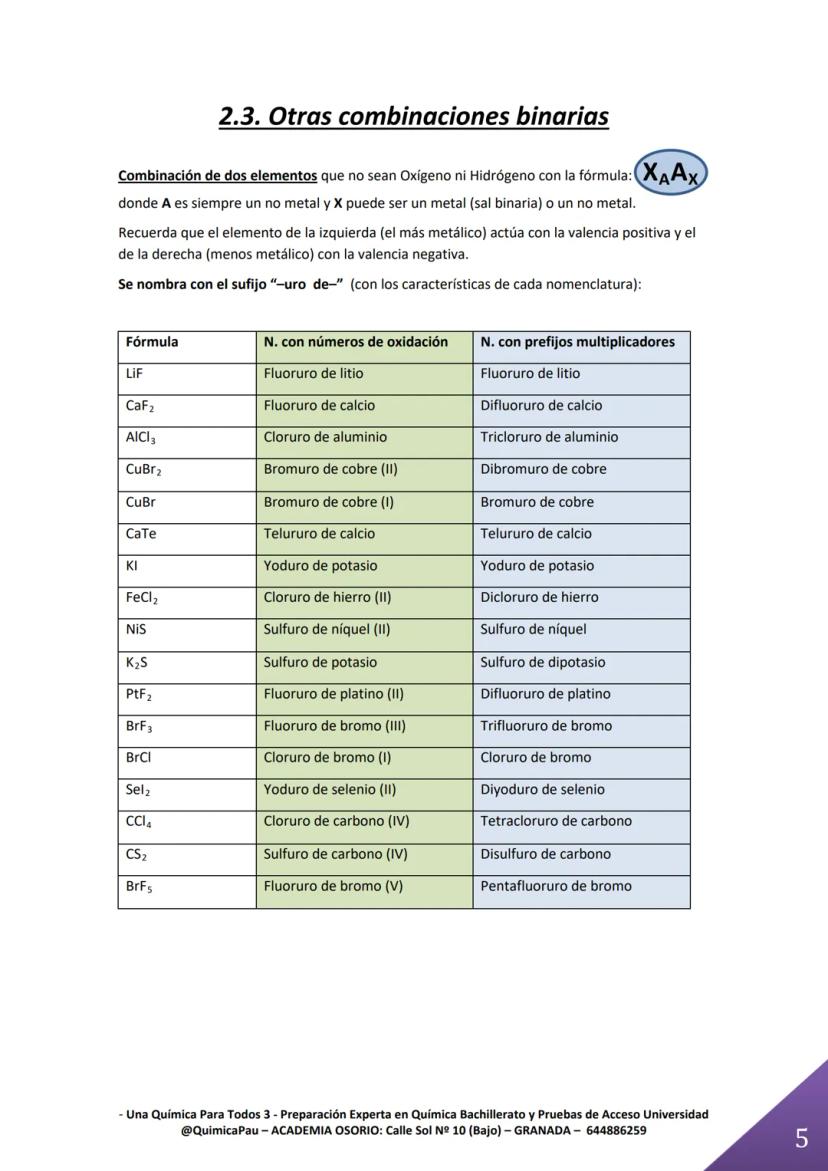
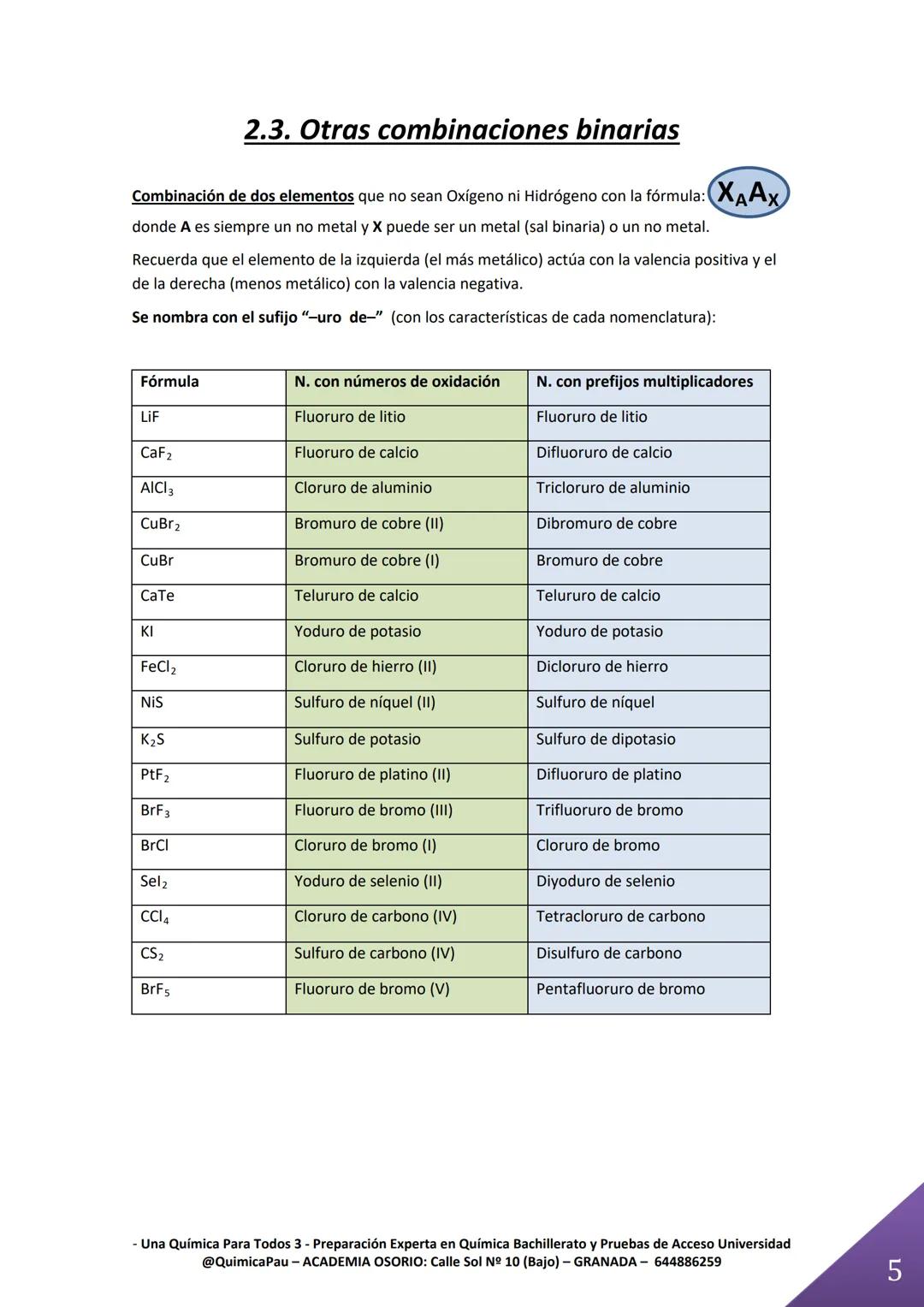
Estas combinaciones binarias son como las "sales básicas" de la química. Se forman cuando combinas dos elementos que no son oxígeno ni hidrógeno, y siempre terminan en "-uro".
El elemento más metálico (menos electronegativo) va a la izquierda con valencia positiva, mientras que el no metal va a la derecha con valencia negativa. Por ejemplo, en CaBr₂, el calcio es más metálico que el bromo.
Aquí brillan los prefijos multiplicadores: tetracloruro de carbono (CCl₄), pentafluoruro de bromo (BrF₅). Estos prefijos te dicen exactamente cuántos átomos de cada elemento hay.
También puedes usar números de oxidación para indicar con qué valencia actúa cada elemento. Por ejemplo, CuBr puede ser bromuro de cobre (I) si el cobre actúa con valencia +1.
¡Dato curioso! Algunos compuestos como el tetracloruro de carbono tienen nombres tan conocidos que se usan en el día a día. ¡La química está en todas partes!
Ácidos Oxoácidos
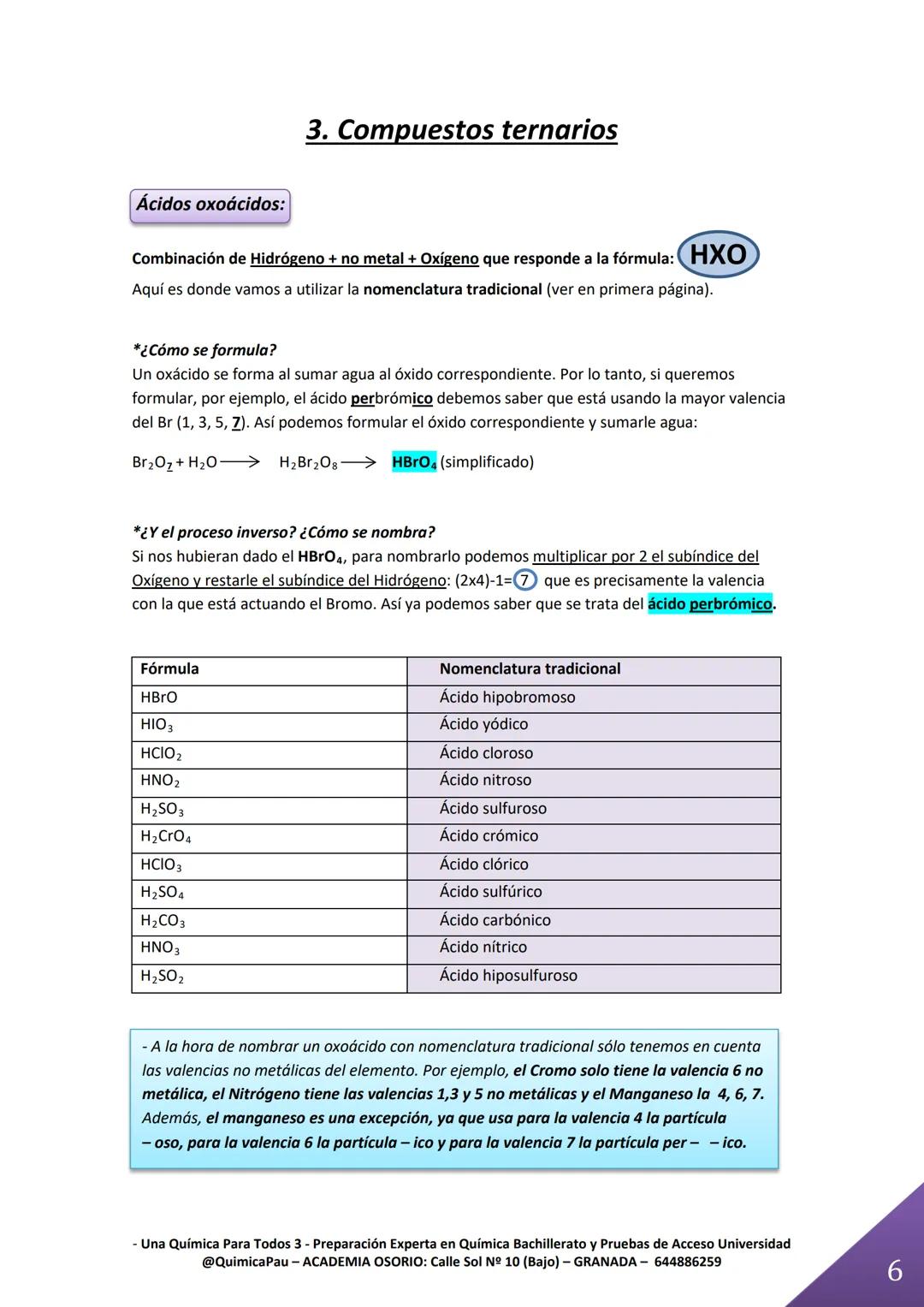
Los ácidos oxoácidos suenan complicados, pero siguen un patrón súper lógico. Se forman cuando añades agua a un óxido, y aquí es donde la nomenclatura tradicional con -oso e -ico cobra sentido.
El truco matemático es genial: para nombrar un ácido como HBrO₄, multiplica por 2 el subíndice del oxígeno y réstale el del hidrógeno: (2×4)-1=7. Como el bromo actúa con valencia 7 (su valencia máxima), es ácido "per-brómico".
Para formular el proceso es al revés: si quieres el ácido perbrómico, sabes que el bromo usa valencia 7, entonces formas Br₂O₇ + H₂O = H₂Br₂O₈, que simplificado es HBrO₄.
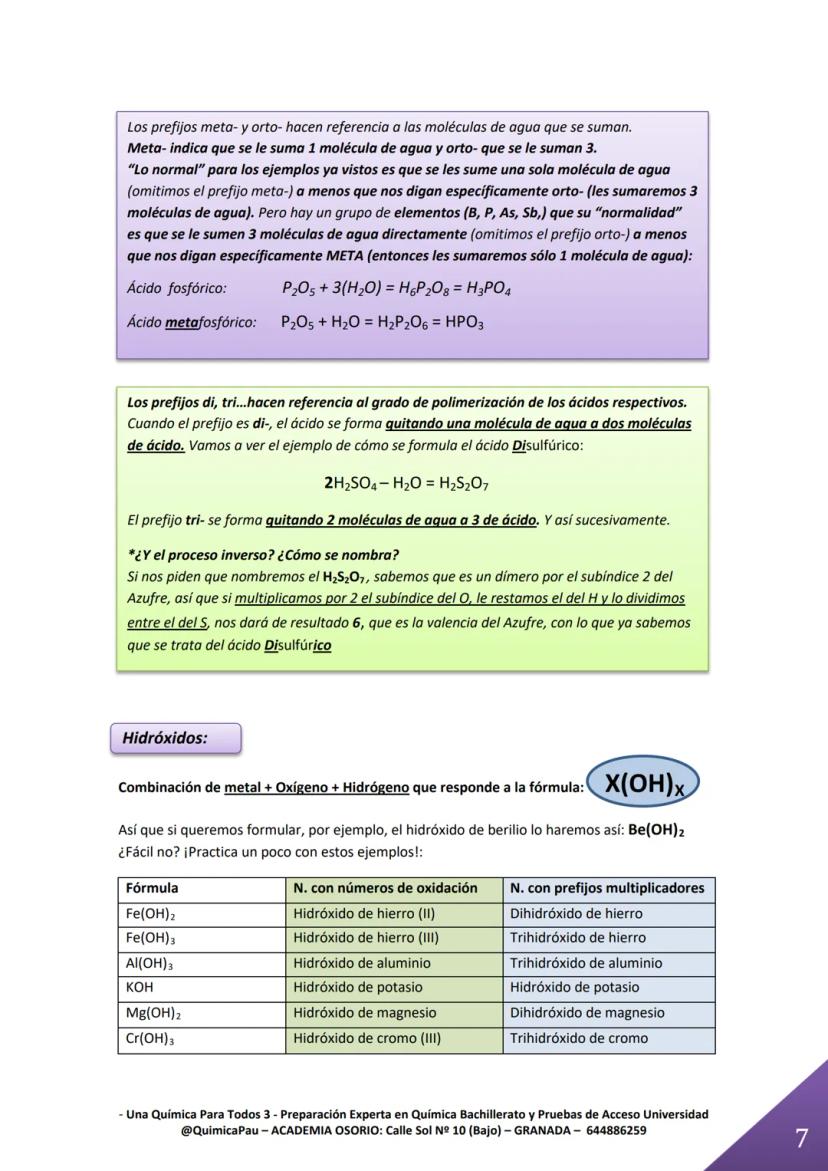
Los elementos como fósforo, boro y arsénico son especiales: normalmente se les suman 3 moléculas de agua en lugar de 1. Solo cuando dices "meta-" les sumas una sola molécula.
¡Truco matemático! Valencia del elemento = (2 × subíndice del O) - subíndice del H. ¡Con esta fórmula nunca fallarás!
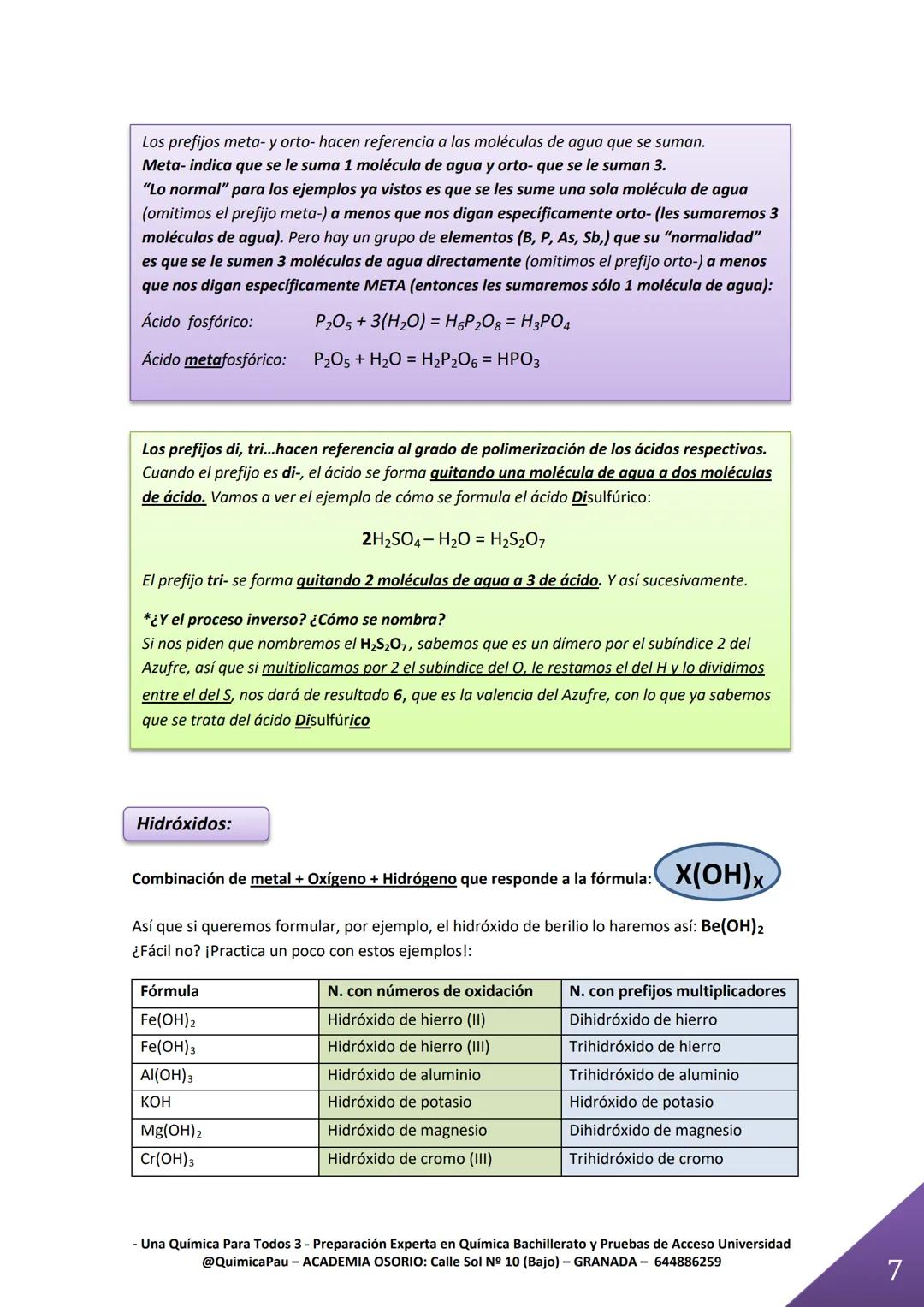
Hidróxidos y Oxisales
Los hidróxidos son facilísimos: solo tienes que poner el metal seguido del grupo OH entre paréntesis. Para el hidróxido de berilio: Be(OH)₂. ¡Pan comido!
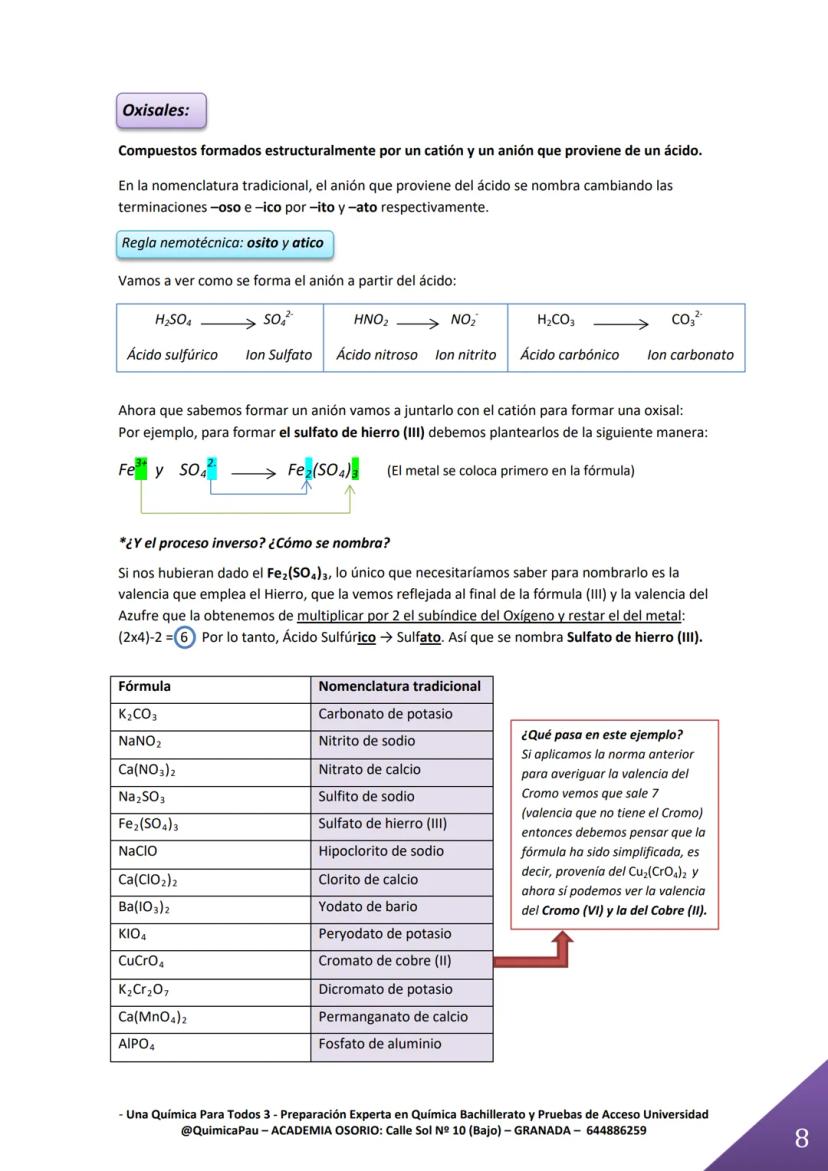
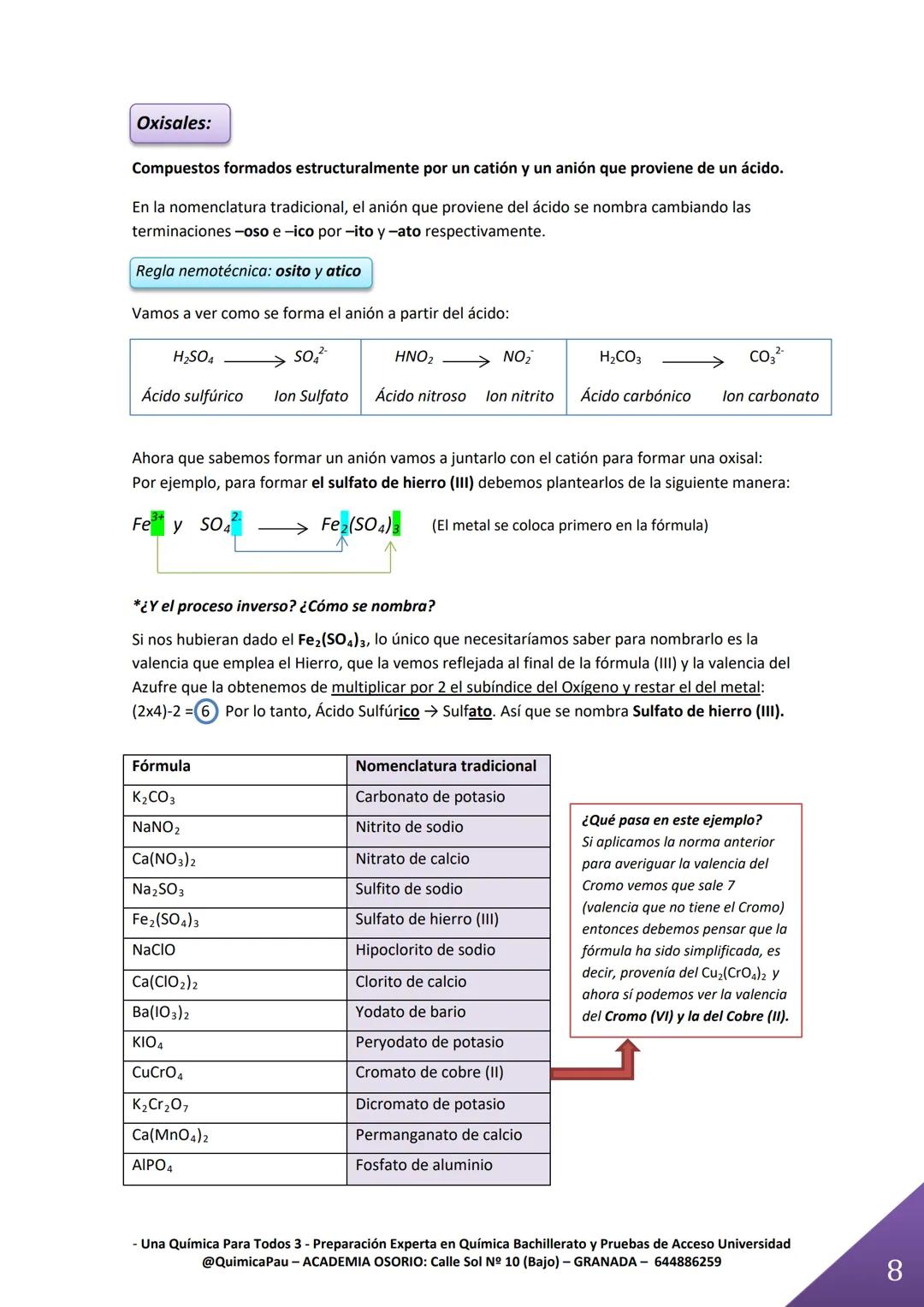
Las oxisales son donde realmente brilla tu conocimiento. Se forman combinando un catión metálico con un anión que viene de un ácido oxoácido. La regla nemotécnica "osito y atico" es tu mejor amiga: -oso se convierte en -ito, -ico se convierte en -ato.
Para formar una oxisal como el sulfato de hierro (III), identifica los iones: Fe³⁺ y SO₄²⁻. Luego balancea las cargas: Fe₂(SO₄)₃. El metal siempre va primero en la fórmula.
El truco para nombrar es calcular la valencia del no metal: (2 × subíndice del O) - valencia del metal. Si sale 6 para el azufre, viene del ácido sulfúrico, así que será un "sulfato".
¡Cuidado especial! Si al calcular la valencia te sale un número raro, probablemente la fórmula esté simplificada. Piensa en la fórmula original.
Sales Ácidas
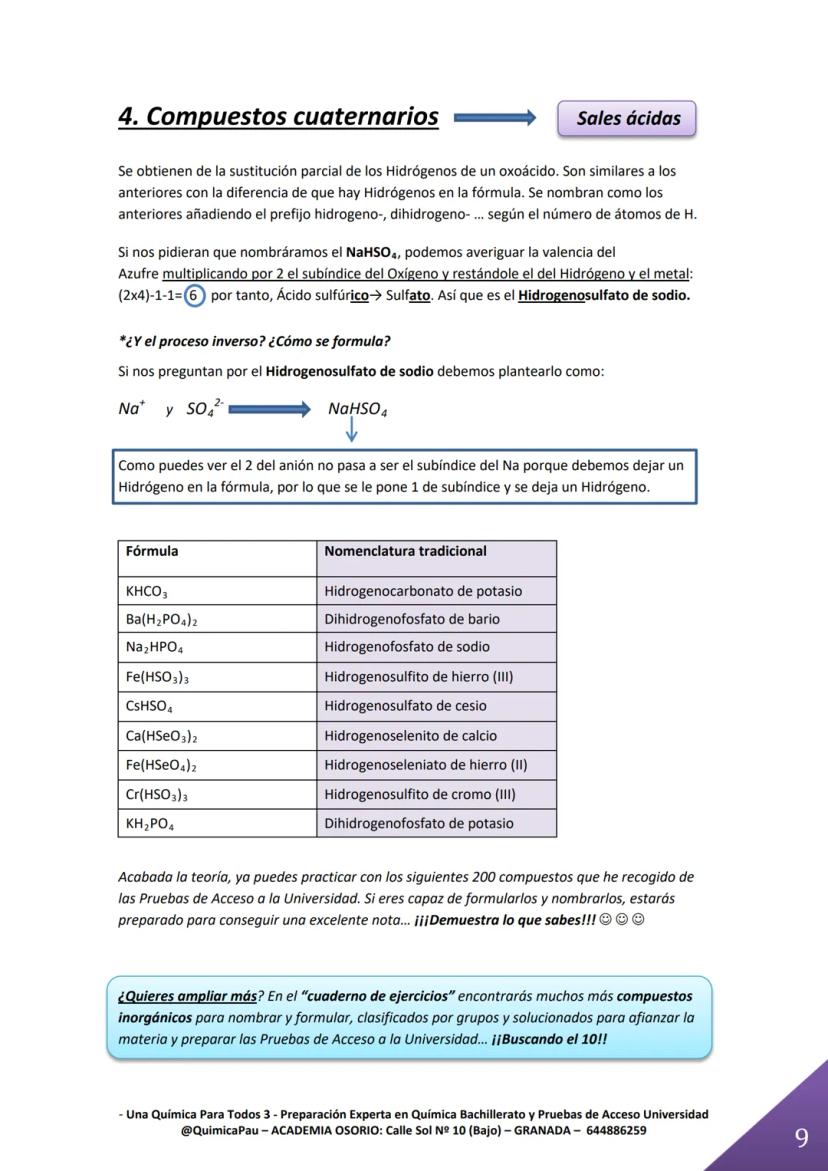
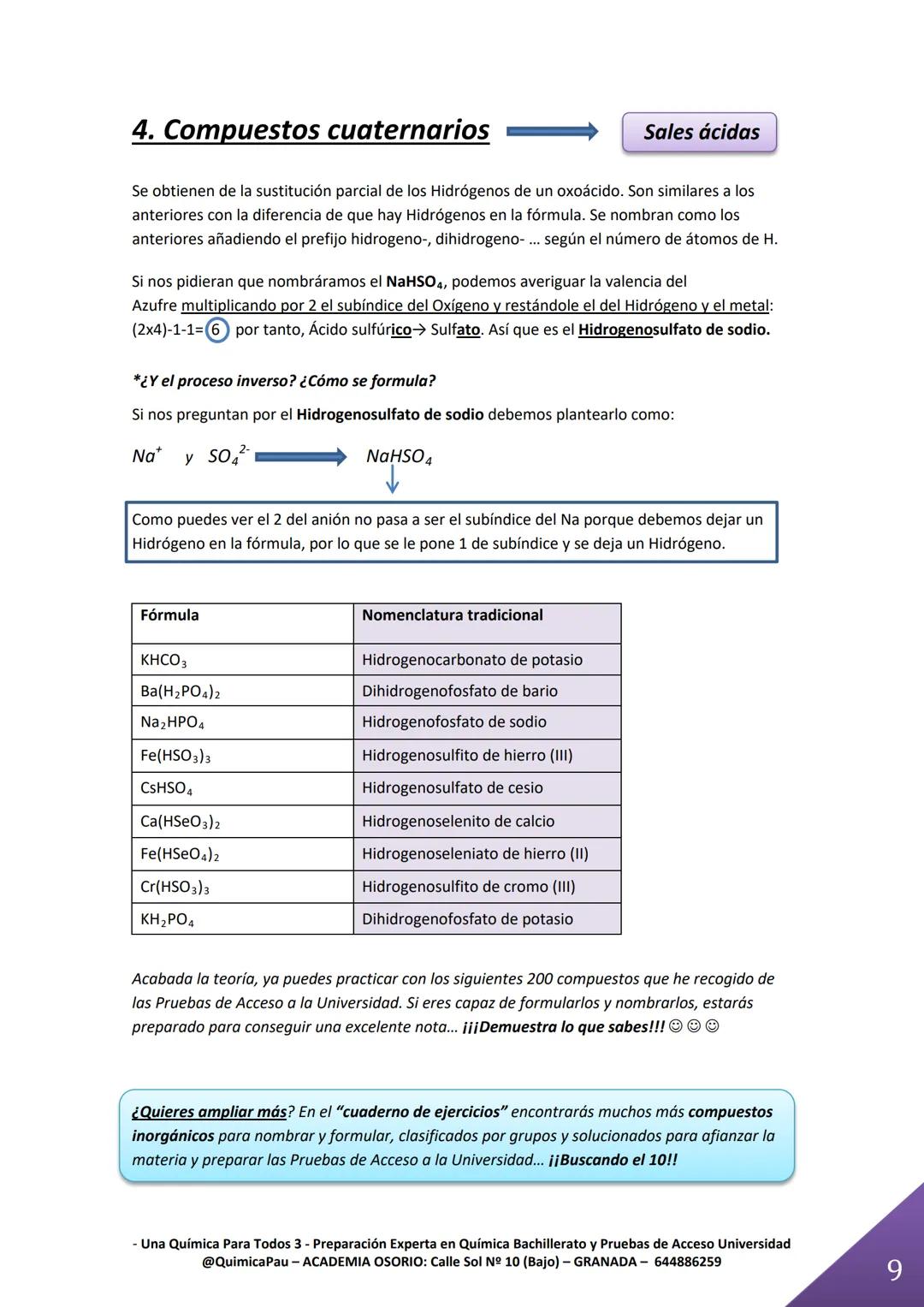
Las sales ácidas son como las oxisales normales, pero conservan algunos hidrógenos del ácido original. Son súper fáciles de reconocer porque tienen hidrógeno en la fórmula además del metal y el anión.
Para nombrarlas, añades el prefijo "hidrogeno-", "dihidrogeno-", etc., según cuántos hidrógenos conserve. El NaHSO₄ es el hidrogenosulfato de sodio.
El truco para calcular la valencia sigue siendo el mismo: (2 × subíndice del O) - hidrógenos - valencia del metal. En NaHSO₄: (2×4)-1-1=6, así que viene del ácido sulfúrico.
Para formular es al revés: si quieres hidrogenosulfato de sodio, tomas el anión SO₄²⁻, le dejas un hidrógeno (queda HSO₄⁻) y lo combinas con Na⁺ para dar NaHSO₄.
¡Dato útil! Las sales ácidas son muy comunes en la vida real. El bicarbonato de sodio (NaHCO₃) que usas para cocinar es una sal ácida.

Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: colección de fórmulas de física
9Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Formulario Física 2ºBachillerato completo
Todo acerca de 2ºbachillerato de física, toda la formulación. Completo.
Formulario física 2 Bach
Todas las fórmulas que utilizarás en física y en evau divididas por temas en tan solo tres folios
Formulación orgánica teoría y ejercicios
1bachillerato
Formulación y nomenclatura orgánica
Formulación orgánica
Formulación óxidos e hidruros
Formulación de óxidos e hidruros
Ejercicios Formulación Inorgánica
Ejercicios en blanco para practicar formulación inorgánica.
Formulación inorganica 4 eso
Apuntes formulación inorganica simples
FORMULACIÓN II
Hidrocarburos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Guía Completa de Formulación Inorgánica
¿Te parece complicado nombrar compuestos químicos como el "monóxido de hierro"? ¡Tranquilo! La formulación inorgánica es como aprender un código secreto que, una vez que lo dominas, te permite descifrar cualquier compuesto químico. Con práctica y los trucos correctos, podrás... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Introducción a la Formulación Inorgánica
¿Sabías que dominar la formulación inorgánica es como tener un superpoder en química? Te permite entender exactamente qué elementos forman cada compuesto y en qué proporciones.
Este tema cubre todos los tipos de compuestos que necesitas conocer: desde los hidruros metálicos más sencillos hasta las oxisales más complejas. El objetivo es que puedas formular y nombrar 200 compuestos diferentes usando las tres nomenclaturas principales.
Las tres formas de nombrar compuestos son: la nomenclatura de composición , la nomenclatura con números de oxidación (usando números romanos) y la nomenclatura tradicional . Cada una tiene sus ventajas según el tipo de compuesto.
¡Truco importante! No intentes memorizar todos los nombres de golpe. Practica grupo por grupo y verás cómo cada tipo sigue un patrón lógico.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Combinaciones Binarias del Hidrógeno
Los hidruros metálicos son súper fáciles una vez que entiendes el truco. Se forman combinando un metal con hidrógeno, donde el hidrógeno siempre actúa con valencia -1.
Para formular hidruros como el hidruro de aluminio (AlH₃), simplemente cruza las valencias: el aluminio tiene valencia +3, el hidrógeno -1, así que necesitas 3 átomos de hidrógeno por cada aluminio. ¡Así de simple!
Los hidruros volátiles son diferentes porque se forman con semimetales. Aquí puedes usar nombres especiales como "amoniaco" para NH₃ o "metano" para CH₄. Estos nombres especiales se llaman nomenclatura de sustitución.
Los haluros de hidrógeno cambian completamente cuando los disuelves en agua. Por ejemplo, HCl gaseoso se llama "cloruro de hidrógeno", pero en disolución acuosa se convierte en "ácido clorhídrico".
¡Ojo! Cuando el hidrógeno se combina con elementos del grupo 16 y 17, el hidrógeno va a la izquierda en la fórmula porque es menos electronegativo.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Combinaciones Binarias del Oxígeno
Los óxidos son como los hidruros pero con oxígeno, que siempre tiene valencia -2. Son súper importantes porque forman la base para muchos otros compuestos más complejos.
La clave está en simplificar siempre las fórmulas. Por ejemplo, Cu₂O₂ se simplifica a CuO. Pero cuidado: cuando uses prefijos multiplicadores, usa la fórmula ya simplificada, mientras que con números de oxidación debes indicar la valencia real del metal.
Los peróxidos son especiales porque contienen el grupo O₂²⁻ que no se puede separar. Por eso el peróxido de hidrógeno es H₂O₂ y no se simplifica. Reconócelos por la fórmula característica X(O₂).
Un truco genial: en algunos casos como OCl₂, el cloro va a la derecha porque es más electronegativo que el oxígeno. ¡La electronegatividad manda en las fórmulas!
¡Truco de oro! Para saber si es un óxido normal o un peróxido, fíjate en si puedes simplificar la fórmula. Si no puedes, probablemente sea un peróxido.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Otras Combinaciones Binarias
Estas combinaciones binarias son como las "sales básicas" de la química. Se forman cuando combinas dos elementos que no son oxígeno ni hidrógeno, y siempre terminan en "-uro".
El elemento más metálico (menos electronegativo) va a la izquierda con valencia positiva, mientras que el no metal va a la derecha con valencia negativa. Por ejemplo, en CaBr₂, el calcio es más metálico que el bromo.
Aquí brillan los prefijos multiplicadores: tetracloruro de carbono (CCl₄), pentafluoruro de bromo (BrF₅). Estos prefijos te dicen exactamente cuántos átomos de cada elemento hay.
También puedes usar números de oxidación para indicar con qué valencia actúa cada elemento. Por ejemplo, CuBr puede ser bromuro de cobre (I) si el cobre actúa con valencia +1.
¡Dato curioso! Algunos compuestos como el tetracloruro de carbono tienen nombres tan conocidos que se usan en el día a día. ¡La química está en todas partes!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Ácidos Oxoácidos
Los ácidos oxoácidos suenan complicados, pero siguen un patrón súper lógico. Se forman cuando añades agua a un óxido, y aquí es donde la nomenclatura tradicional con -oso e -ico cobra sentido.
El truco matemático es genial: para nombrar un ácido como HBrO₄, multiplica por 2 el subíndice del oxígeno y réstale el del hidrógeno: (2×4)-1=7. Como el bromo actúa con valencia 7 (su valencia máxima), es ácido "per-brómico".
Para formular el proceso es al revés: si quieres el ácido perbrómico, sabes que el bromo usa valencia 7, entonces formas Br₂O₇ + H₂O = H₂Br₂O₈, que simplificado es HBrO₄.
Los elementos como fósforo, boro y arsénico son especiales: normalmente se les suman 3 moléculas de agua en lugar de 1. Solo cuando dices "meta-" les sumas una sola molécula.
¡Truco matemático! Valencia del elemento = (2 × subíndice del O) - subíndice del H. ¡Con esta fórmula nunca fallarás!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Hidróxidos y Oxisales
Los hidróxidos son facilísimos: solo tienes que poner el metal seguido del grupo OH entre paréntesis. Para el hidróxido de berilio: Be(OH)₂. ¡Pan comido!
Las oxisales son donde realmente brilla tu conocimiento. Se forman combinando un catión metálico con un anión que viene de un ácido oxoácido. La regla nemotécnica "osito y atico" es tu mejor amiga: -oso se convierte en -ito, -ico se convierte en -ato.
Para formar una oxisal como el sulfato de hierro (III), identifica los iones: Fe³⁺ y SO₄²⁻. Luego balancea las cargas: Fe₂(SO₄)₃. El metal siempre va primero en la fórmula.
El truco para nombrar es calcular la valencia del no metal: (2 × subíndice del O) - valencia del metal. Si sale 6 para el azufre, viene del ácido sulfúrico, así que será un "sulfato".
¡Cuidado especial! Si al calcular la valencia te sale un número raro, probablemente la fórmula esté simplificada. Piensa en la fórmula original.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sales Ácidas
Las sales ácidas son como las oxisales normales, pero conservan algunos hidrógenos del ácido original. Son súper fáciles de reconocer porque tienen hidrógeno en la fórmula además del metal y el anión.
Para nombrarlas, añades el prefijo "hidrogeno-", "dihidrogeno-", etc., según cuántos hidrógenos conserve. El NaHSO₄ es el hidrogenosulfato de sodio.
El truco para calcular la valencia sigue siendo el mismo: (2 × subíndice del O) - hidrógenos - valencia del metal. En NaHSO₄: (2×4)-1-1=6, así que viene del ácido sulfúrico.
Para formular es al revés: si quieres hidrogenosulfato de sodio, tomas el anión SO₄²⁻, le dejas un hidrógeno (queda HSO₄⁻) y lo combinas con Na⁺ para dar NaHSO₄.
¡Dato útil! Las sales ácidas son muy comunes en la vida real. El bicarbonato de sodio (NaHCO₃) que usas para cocinar es una sal ácida.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: colección de fórmulas de física
9Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Formulario Física 2ºBachillerato completo
Todo acerca de 2ºbachillerato de física, toda la formulación. Completo.
Formulario física 2 Bach
Todas las fórmulas que utilizarás en física y en evau divididas por temas en tan solo tres folios
Formulación orgánica teoría y ejercicios
1bachillerato
Formulación y nomenclatura orgánica
Formulación orgánica
Formulación óxidos e hidruros
Formulación de óxidos e hidruros
Ejercicios Formulación Inorgánica
Ejercicios en blanco para practicar formulación inorgánica.
Formulación inorganica 4 eso
Apuntes formulación inorganica simples
FORMULACIÓN II
Hidrocarburos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.