¡Vamos a descifrar el código de la formulación inorgánica! La... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
4,066
•
Actualizado Mar 22, 2026
•
lidia sánchez
@lidiasnchhz
¡Vamos a descifrar el código de la formulación inorgánica! La... Mostrar más








Las nomenclaturas son como diferentes formas de "llamar" al mismo compuesto. Tienes cuatro opciones: sistemática , de Stock (números romanos), de carga , y tradicional (solo para algunos casos específicos).
Los hidruros son compuestos que llevan hidrógeno. Con metales, el hidrógeno siempre tiene carga -1, así que FeH₂ se llama "dihidruro de hierro". Con no metales es más complicado porque el hidrógeno puede tener carga +1 o -1 según el elemento.
¡Ojo con las excepciones! Algunos hidruros tienen nombres especiales que tienes que memorizar: NH₃ es amoniaco, CH₄ es metano, y PH₃ es fosfano.
La clave está en fijarse primero en qué tipo de elemento acompaña al hidrógeno. ¿Es un metal? Entonces el hidrógeno va con -1. ¿Es un no metal? Ahí tienes que mirar en qué grupo de la tabla periódica está.

Los óxidos son súper fáciles una vez que entiendes el patrón: cualquier elemento + oxígeno con carga -2. El truco está en simplificar las fórmulas cuando sea posible. Por ejemplo, Sr₂O₂ se convierte en SrO.
Para nombrarlos, usas los prefijos o indicas el número de oxidación del elemento. PtO₂ puede ser "dióxido de platino" o "óxido de platino (IV)". Si el elemento solo tiene una valencia posible, no hace falta poner números.
Los peróxidos son un caso especial donde tienes el grupo O₂²⁻ (ion peróxido). El más famoso es H₂O₂, que conoces como agua oxigenada.
Dato curioso: Los peróxidos siempre mantienen esa estructura O₂²⁻, no se simplifican como los óxidos normales.

Las sales binarias son compuestos de dos elementos sin oxígeno. Cuando combines un metal con un no metal, siempre nombras primero el no metal y después el metal.
Au₂S₃ se lee como "trisulfuro de dioro" o "sulfuro de oro (III)". El no metal (azufre) va primero y lleva la terminación -uro, mientras que el metal (oro) va después con su número de oxidación.
Si tienes dos no metales, el más electronegativo va primero en el nombre. BrCl₇ es "heptacloruro de bromo" porque el cloro es más electronegativo que el bromo.
Grupos especiales: Memoriza el cianuro (CN⁻) y el amonio (NH₄⁺), que aparecen constantemente en exámenes.
También puedes encontrar casos como HCN (cianuro de hidrógeno) que tiene nombre especial: ácido cianhídrico.

Los hidróxidos contienen el grupo OH⁻ (hidroxilo). Son compuestos básicos muy comunes que encuentras en productos de limpieza y laboratorio.
La fórmula general es muy sencilla: metal + OH⁻. Ca(OH)₂ es "hidróxido de calcio", NaOH es "hidróxido de sodio". Si el metal tiene varias valencias, indicas cuál estás usando: Fe(OH)₃ es "hidróxido de hierro (III)".
El grupo OH⁻ siempre tiene carga -1, así que necesitas equilibrar las cargas. El calcio tiene carga +2, por eso necesitas dos grupos OH⁻ para formar Ca(OH)₂.
En el lab: El NaOH (sosa cáustica) y el Ca(OH)₂ (cal apagada) son hidróxidos que ves en la vida real.
Algunos hidróxidos como Mg(OH)₂ se usan en medicinas (como antiácido), mientras que otros como KOH son importantes en la industria.

Los oxoácidos son ácidos que contienen hidrógeno, un no metal y oxígeno. Aquí viene la parte que más cuesta, pero tiene truco: las terminaciones -oso/-ico se convierten en -ito/-ato cuando formas sales.
Para el grupo 17 (halógenos), tienes cuatro valencias posibles: +1 (hipo...oso), +3 (...oso), +5 (...ico), y +7 (per...ico). HClO es ácido hipocloroso, HClO₄ es ácido perclórico.
El grupo 16 (azufre y compañía) usa las valencias +2, +4 y +6. H₂SO₃ es ácido sulfuroso, H₂SO₄ es ácido sulfúrico. Lo del "hipo" solo aparece con valencia +2.
Excepción importante: El yodo con valencia +7 puede formar HIO₄ (ácido metaperyódico) o H₅IO₆ (ácido ortoperyódico).
Los grupos 15, 14, 13 y 7 también siguen patrones similares, pero cada uno tiene sus excepciones. El fósforo, por ejemplo, puede formar ácidos meta-, piro- y orto- según cuántas moléculas de agua reaccionen.

El grupo 15 (nitrógeno, fósforo...) usa valencias +1, +3 y +5. HNO₂ es ácido nitroso, HNO₃ es ácido nítrico. El fósforo es especial porque forma ácidos meta-, piro- y orto- dependiendo de cuánta agua interviene en la reacción.
Los grupos 14 y 13 son más sencillos. El carbono forma H₂CO₃ (ácido carbónico), el boro forma HBO₂ (ácido metabórico) y H₃BO₃ (ácido ortobórico).
El manganeso (grupo 7) tiene tres valencias importantes: +4, +6 y +7. HMnO₄ es el famoso ácido permangánico (permanganato de potasio), que usas en laboratorio como oxidante.
Truco para recordar: Los prefijos meta- significan "menos agua", orto- significa "más agua", y piro- es intermedio.
El cromo forma H₂CrO₄ (ácido crómico) y H₂Cr₂O₇ (ácido dicrómico). Este último es como si juntaras dos moléculas del primero perdiendo una molécula de agua.

Las oxisales se forman cuando los oxoácidos pierden sus hidrógenos y se combinan con metales. Los cationes son iones con carga positiva (metales que pierden electrones), y los aniones son iones con carga negativa.
Los cationes más comunes son Au³⁺, Mg²⁺, Al³⁺, y grupos especiales como NH₄⁺ (amonio) y H₃O⁺ (oxonio). Los aniones simples llevan terminación -uro: Br⁻ (bromuro), Se²⁻ (seleniuro).
Los aniones de oxoácidos cambian las terminaciones: -oso se convierte en -ito, -ico se convierte en -ato. HClO₃ (ácido clórico) forma ClO₃⁻ (ion clorato).
Iones complejos: H₃PO₄ puede perder uno, dos o tres hidrógenos, formando H₂PO₄⁻, HPO₄²⁻ o PO₄³⁻.
Cuando un oxoácido pierde parcialmente sus hidrógenos, usas el prefijo "hidrogeno-" para indicar cuántos quedan. HSO₃⁻ es ion hidrogenosulfito.
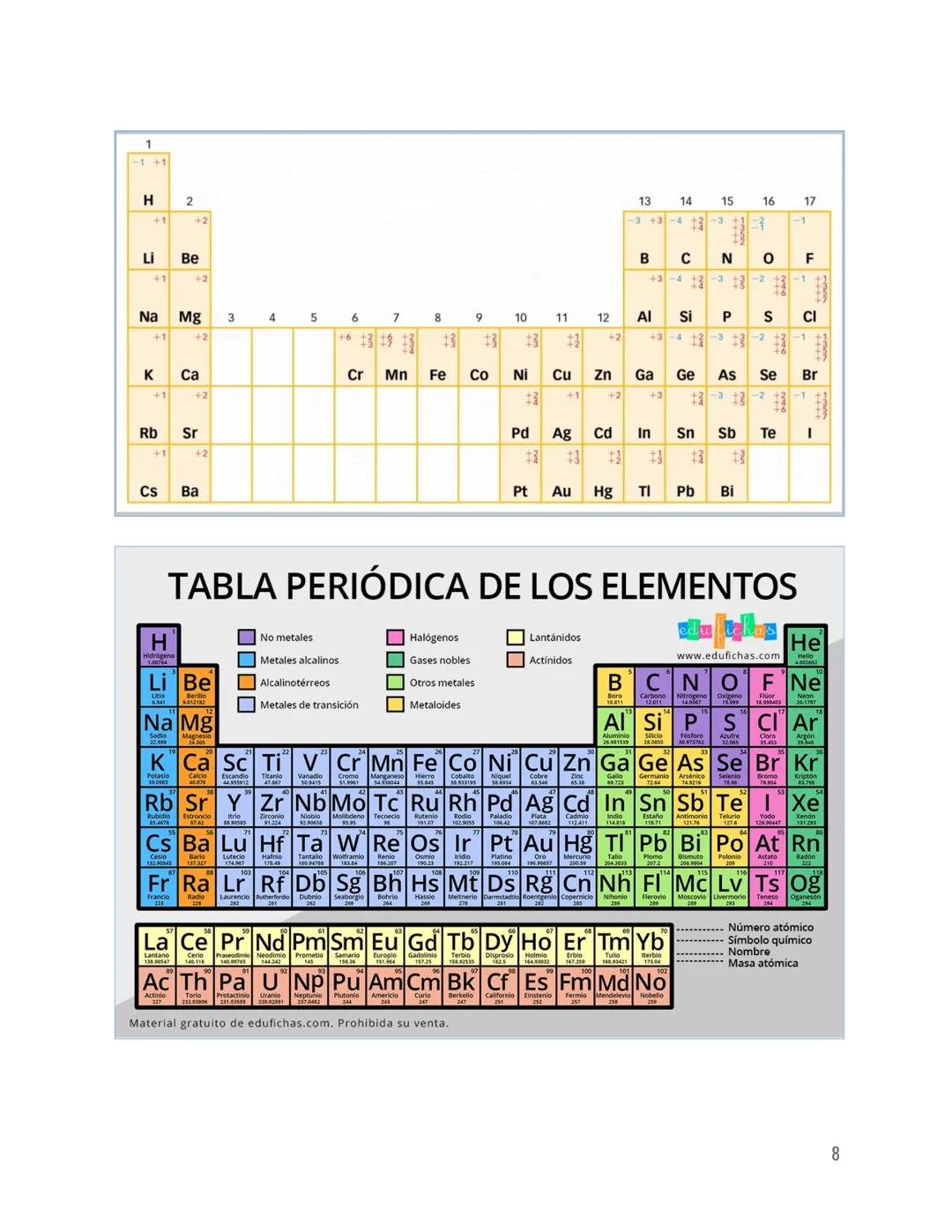
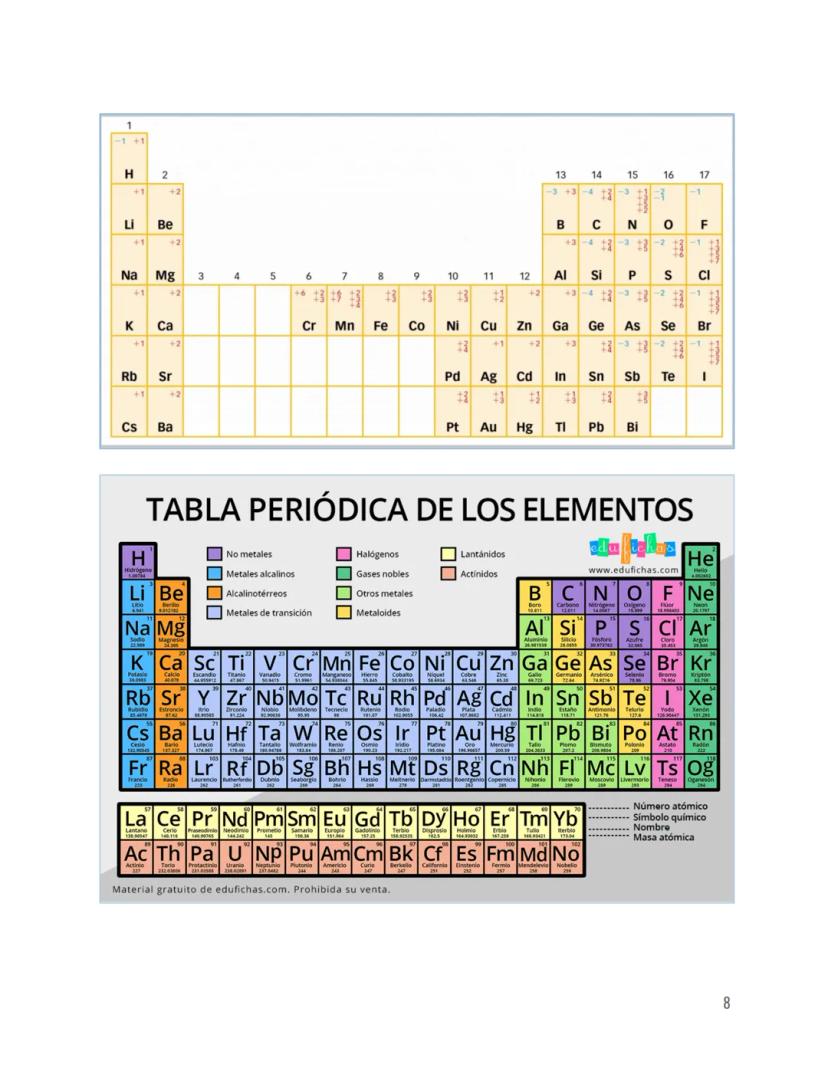
La tabla periódica es tu mejor amiga para la formulación. Los elementos están organizados por grupos (columnas) que comparten propiedades químicas similares.
Los metales alcalinos (grupo 1) siempre tienen valencia +1, los alcalinotérreos (grupo 2) tienen +2. Los halógenos (grupo 17) como Cl, Br, I pueden tener valencias -1, +1, +3, +5, +7.
Los metales de transición son los más complicados porque tienen múltiples valencias. El hierro puede ser +2 o +3, el cobre +1 o +2. Por eso necesitas indicar cuál estás usando con números romanos.
Consejo de oro: Memoriza las valencias más comunes de cada grupo. Te ahorrará muchísimo tiempo en exámenes.
Los metaloides como el boro o el silicio pueden comportarse como metales o no metales según el compuesto. Los gases nobles casi nunca forman compuestos, así que no te preocupes por ellos.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
lidia sánchez
@lidiasnchhz
¡Vamos a descifrar el código de la formulación inorgánica! La química puede parecer un idioma extraño al principio, pero una vez que pillas los patrones básicos, te darás cuenta de que todo tiene lógica. Aquí tienes todo lo que necesitas... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las nomenclaturas son como diferentes formas de "llamar" al mismo compuesto. Tienes cuatro opciones: sistemática , de Stock (números romanos), de carga , y tradicional (solo para algunos casos específicos).
Los hidruros son compuestos que llevan hidrógeno. Con metales, el hidrógeno siempre tiene carga -1, así que FeH₂ se llama "dihidruro de hierro". Con no metales es más complicado porque el hidrógeno puede tener carga +1 o -1 según el elemento.
¡Ojo con las excepciones! Algunos hidruros tienen nombres especiales que tienes que memorizar: NH₃ es amoniaco, CH₄ es metano, y PH₃ es fosfano.
La clave está en fijarse primero en qué tipo de elemento acompaña al hidrógeno. ¿Es un metal? Entonces el hidrógeno va con -1. ¿Es un no metal? Ahí tienes que mirar en qué grupo de la tabla periódica está.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los óxidos son súper fáciles una vez que entiendes el patrón: cualquier elemento + oxígeno con carga -2. El truco está en simplificar las fórmulas cuando sea posible. Por ejemplo, Sr₂O₂ se convierte en SrO.
Para nombrarlos, usas los prefijos o indicas el número de oxidación del elemento. PtO₂ puede ser "dióxido de platino" o "óxido de platino (IV)". Si el elemento solo tiene una valencia posible, no hace falta poner números.
Los peróxidos son un caso especial donde tienes el grupo O₂²⁻ (ion peróxido). El más famoso es H₂O₂, que conoces como agua oxigenada.
Dato curioso: Los peróxidos siempre mantienen esa estructura O₂²⁻, no se simplifican como los óxidos normales.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las sales binarias son compuestos de dos elementos sin oxígeno. Cuando combines un metal con un no metal, siempre nombras primero el no metal y después el metal.
Au₂S₃ se lee como "trisulfuro de dioro" o "sulfuro de oro (III)". El no metal (azufre) va primero y lleva la terminación -uro, mientras que el metal (oro) va después con su número de oxidación.
Si tienes dos no metales, el más electronegativo va primero en el nombre. BrCl₇ es "heptacloruro de bromo" porque el cloro es más electronegativo que el bromo.
Grupos especiales: Memoriza el cianuro (CN⁻) y el amonio (NH₄⁺), que aparecen constantemente en exámenes.
También puedes encontrar casos como HCN (cianuro de hidrógeno) que tiene nombre especial: ácido cianhídrico.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los hidróxidos contienen el grupo OH⁻ (hidroxilo). Son compuestos básicos muy comunes que encuentras en productos de limpieza y laboratorio.
La fórmula general es muy sencilla: metal + OH⁻. Ca(OH)₂ es "hidróxido de calcio", NaOH es "hidróxido de sodio". Si el metal tiene varias valencias, indicas cuál estás usando: Fe(OH)₃ es "hidróxido de hierro (III)".
El grupo OH⁻ siempre tiene carga -1, así que necesitas equilibrar las cargas. El calcio tiene carga +2, por eso necesitas dos grupos OH⁻ para formar Ca(OH)₂.
En el lab: El NaOH (sosa cáustica) y el Ca(OH)₂ (cal apagada) son hidróxidos que ves en la vida real.
Algunos hidróxidos como Mg(OH)₂ se usan en medicinas (como antiácido), mientras que otros como KOH son importantes en la industria.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los oxoácidos son ácidos que contienen hidrógeno, un no metal y oxígeno. Aquí viene la parte que más cuesta, pero tiene truco: las terminaciones -oso/-ico se convierten en -ito/-ato cuando formas sales.
Para el grupo 17 (halógenos), tienes cuatro valencias posibles: +1 (hipo...oso), +3 (...oso), +5 (...ico), y +7 (per...ico). HClO es ácido hipocloroso, HClO₄ es ácido perclórico.
El grupo 16 (azufre y compañía) usa las valencias +2, +4 y +6. H₂SO₃ es ácido sulfuroso, H₂SO₄ es ácido sulfúrico. Lo del "hipo" solo aparece con valencia +2.
Excepción importante: El yodo con valencia +7 puede formar HIO₄ (ácido metaperyódico) o H₅IO₆ (ácido ortoperyódico).
Los grupos 15, 14, 13 y 7 también siguen patrones similares, pero cada uno tiene sus excepciones. El fósforo, por ejemplo, puede formar ácidos meta-, piro- y orto- según cuántas moléculas de agua reaccionen.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El grupo 15 (nitrógeno, fósforo...) usa valencias +1, +3 y +5. HNO₂ es ácido nitroso, HNO₃ es ácido nítrico. El fósforo es especial porque forma ácidos meta-, piro- y orto- dependiendo de cuánta agua interviene en la reacción.
Los grupos 14 y 13 son más sencillos. El carbono forma H₂CO₃ (ácido carbónico), el boro forma HBO₂ (ácido metabórico) y H₃BO₃ (ácido ortobórico).
El manganeso (grupo 7) tiene tres valencias importantes: +4, +6 y +7. HMnO₄ es el famoso ácido permangánico (permanganato de potasio), que usas en laboratorio como oxidante.
Truco para recordar: Los prefijos meta- significan "menos agua", orto- significa "más agua", y piro- es intermedio.
El cromo forma H₂CrO₄ (ácido crómico) y H₂Cr₂O₇ (ácido dicrómico). Este último es como si juntaras dos moléculas del primero perdiendo una molécula de agua.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las oxisales se forman cuando los oxoácidos pierden sus hidrógenos y se combinan con metales. Los cationes son iones con carga positiva (metales que pierden electrones), y los aniones son iones con carga negativa.
Los cationes más comunes son Au³⁺, Mg²⁺, Al³⁺, y grupos especiales como NH₄⁺ (amonio) y H₃O⁺ (oxonio). Los aniones simples llevan terminación -uro: Br⁻ (bromuro), Se²⁻ (seleniuro).
Los aniones de oxoácidos cambian las terminaciones: -oso se convierte en -ito, -ico se convierte en -ato. HClO₃ (ácido clórico) forma ClO₃⁻ (ion clorato).
Iones complejos: H₃PO₄ puede perder uno, dos o tres hidrógenos, formando H₂PO₄⁻, HPO₄²⁻ o PO₄³⁻.
Cuando un oxoácido pierde parcialmente sus hidrógenos, usas el prefijo "hidrogeno-" para indicar cuántos quedan. HSO₃⁻ es ion hidrogenosulfito.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La tabla periódica es tu mejor amiga para la formulación. Los elementos están organizados por grupos (columnas) que comparten propiedades químicas similares.
Los metales alcalinos (grupo 1) siempre tienen valencia +1, los alcalinotérreos (grupo 2) tienen +2. Los halógenos (grupo 17) como Cl, Br, I pueden tener valencias -1, +1, +3, +5, +7.
Los metales de transición son los más complicados porque tienen múltiples valencias. El hierro puede ser +2 o +3, el cobre +1 o +2. Por eso necesitas indicar cuál estás usando con números romanos.
Consejo de oro: Memoriza las valencias más comunes de cada grupo. Te ahorrará muchísimo tiempo en exámenes.
Los metaloides como el boro o el silicio pueden comportarse como metales o no metales según el compuesto. Los gases nobles casi nunca forman compuestos, así que no te preocupes por ellos.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
81
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
Formulación de Química Inorgánica para 1° de Bachillerato y 4° de ESO
Enlace ionico i covalente
Formjlacion inorgánica de 1batx
cuadernillo de formulación inorganica completo y con ejemplos
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS