La estructura atómicaes fundamental para entender toda la química... Mostrar más
Estructura Atómica y Enlace Químico: Guía Completa de Estudio







Estructura atómica, sistema periódico y enlace químico
¡Empezamos el tema más importante de química! Todo lo que estudiarás este año tiene que ver con cómo están hechos los átomos y cómo se unen entre ellos.
Este tema te dará las bases para entender por qué los elementos se comportan como lo hacen. También descubrirás cómo se forman los diferentes tipos de enlaces químicos.
¿Sabías que...? Los conceptos de este tema aparecen en casi todas las preguntas de selectividad de química.

Los primeros pasos: Demócrito vs Aristóteles
La historia del átomo empezó hace más de 2000 años con una gran discusión. Demócrito pensaba que si cortabas cualquier cosa en trozos cada vez más pequeños, al final llegarías a una partícula que ya no se podría dividir más: el átomo.
Pero Aristóteles no estaba de acuerdo y propuso que todo estaba hecho de cuatro elementos: tierra, agua, aire y fuego. Su idea fue tan influyente que durante casi 2000 años nadie se atrevió a contradecirle.
Curiosidad: La palabra "átomo" viene del griego y significa "que no se puede dividir".
La evolución de los modelos atómicos
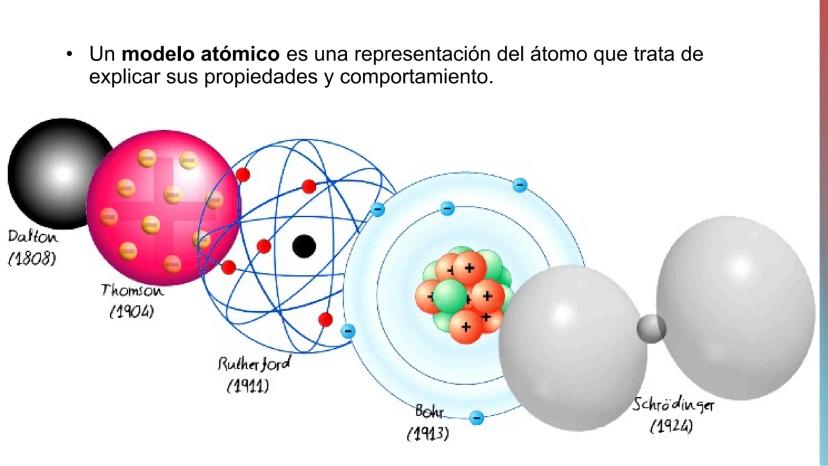
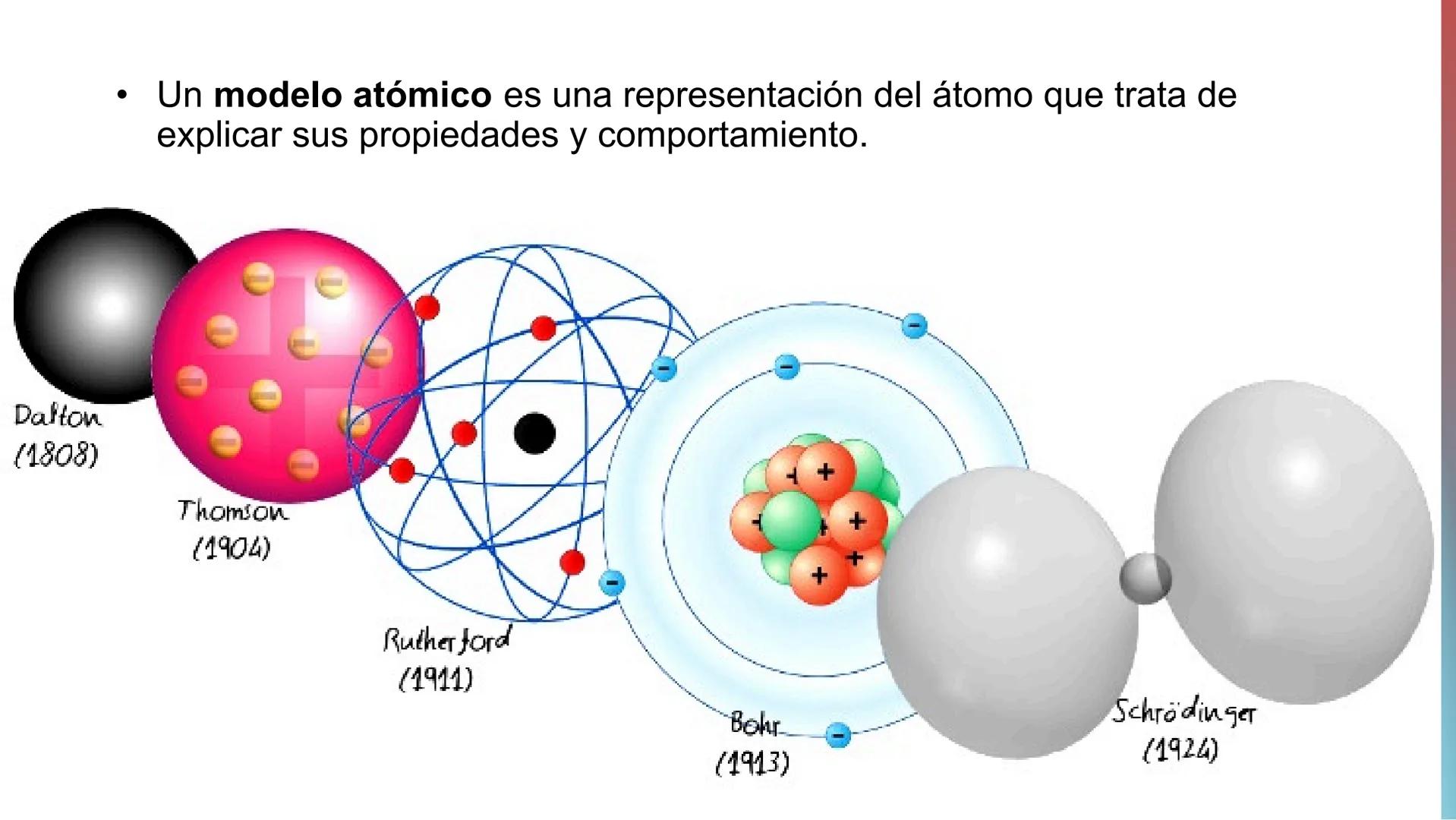
Un modelo atómico es como un dibujo que nos ayuda a imaginar cómo es un átomo y por qué se comporta de cierta manera. A lo largo de la historia, los científicos han ido mejorando estos modelos.
Los principales modelos que debes conocer son: Dalton (1808), Thomson (1904), Rutherford (1911), Bohr (1913) y Schrödinger (1924). Cada uno aportó algo nuevo y corrigió errores del anterior.
Es como si cada científico hubiera añadido una pieza al puzzle hasta conseguir la imagen que tenemos hoy del átomo.
Para el examen: Tienes que saber las características principales de cada modelo y sus limitaciones.

Modelo atómico de Dalton
Dalton fue el primero en retomar las ideas de Demócrito de forma científica en el siglo XIX. Sus ideas principales eran bastante lógicas para su época.
Según Dalton, la materia está formada por partículas pequeñas e indivisibles. Los átomos del mismo elemento son idénticos en masa y propiedades. Los compuestos se forman cuando se unen átomos en proporciones sencillas.
También propuso que en las reacciones químicas los átomos solo se reorganizan, pero nunca desaparecen ni se transforman en otros elementos. Esta idea sigue siendo válida hoy en día.
Dato clave: El modelo de Dalton explica perfectamente las leyes químicas básicas que estudiarás.

Modelo atómico de Thomson
Thomson descubrió algo que Dalton no sabía: los átomos no son indivisibles. En 1898 propuso que el átomo era como un "pudin de pasas": una esfera de carga positiva con electrones incrustados por toda su superficie.
Este modelo explicaba por qué los átomos son neutros (las cargas positivas y negativas se compensan). También se conoce como el modelo del "pudin de pasas" porque los electrones parecían pasas metidas en un pudin.
Aunque después se demostró que estaba equivocado, Thomson fue el primero en descubrir que había partículas más pequeñas que el átomo.
Recuerda: Thomson descubrió el electrón, la primera partícula subatómica conocida.
El descubrimiento del electrón
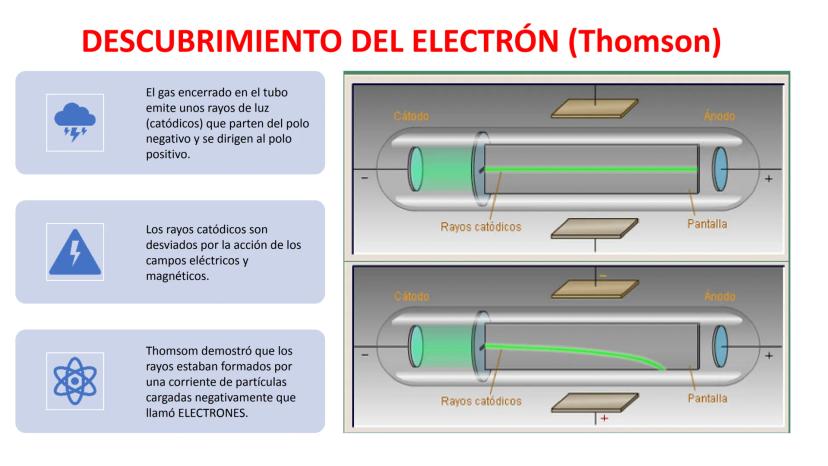
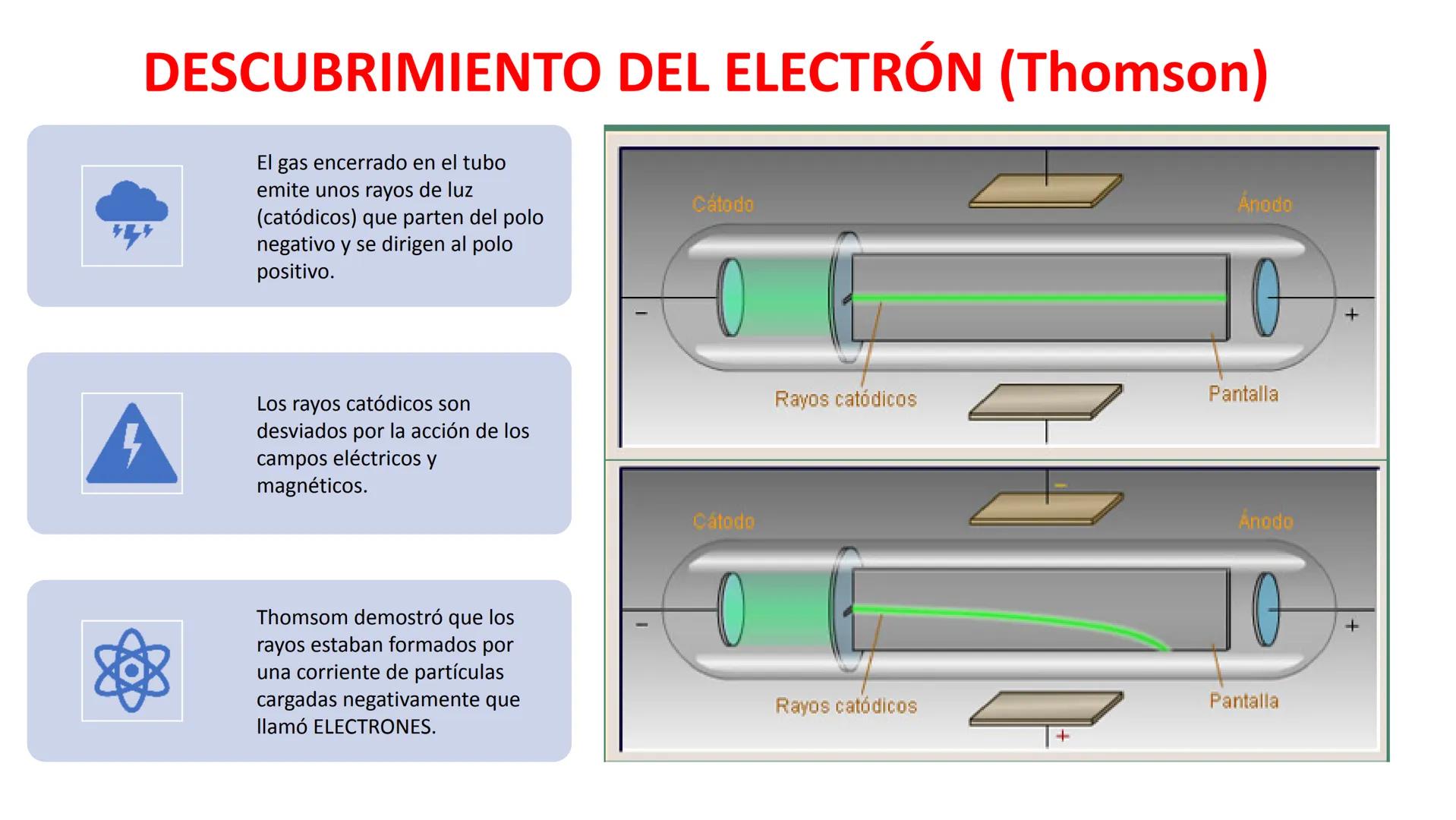
Thomson hizo un experimento genial con tubos de rayos catódicos. Cuando aplicaba electricidad a un gas encerrado en un tubo, aparecían unos rayos luminosos que iban del polo negativo al positivo.
Lo más interesante era que estos rayos catódicos se desviaban cuando Thomson ponía cerca campos eléctricos o magnéticos. Esto le demostró que los rayos estaban formados por partículas con carga negativa.
A estas partículas las llamó electrones. Así descubrió que los átomos no eran indivisibles como pensaba Dalton, sino que tenían partes más pequeñas.
Experimento clave: Los tubos de rayos catódicos fueron el primer paso para entender la estructura interna del átomo.
Modelo atómico de Rutherford
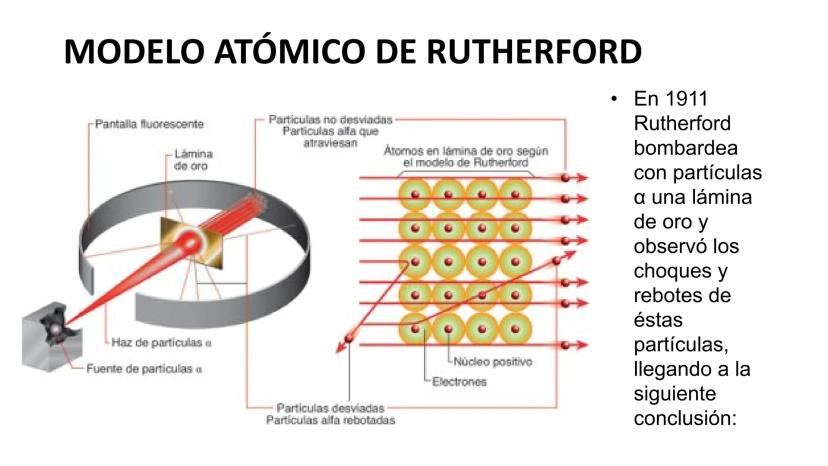
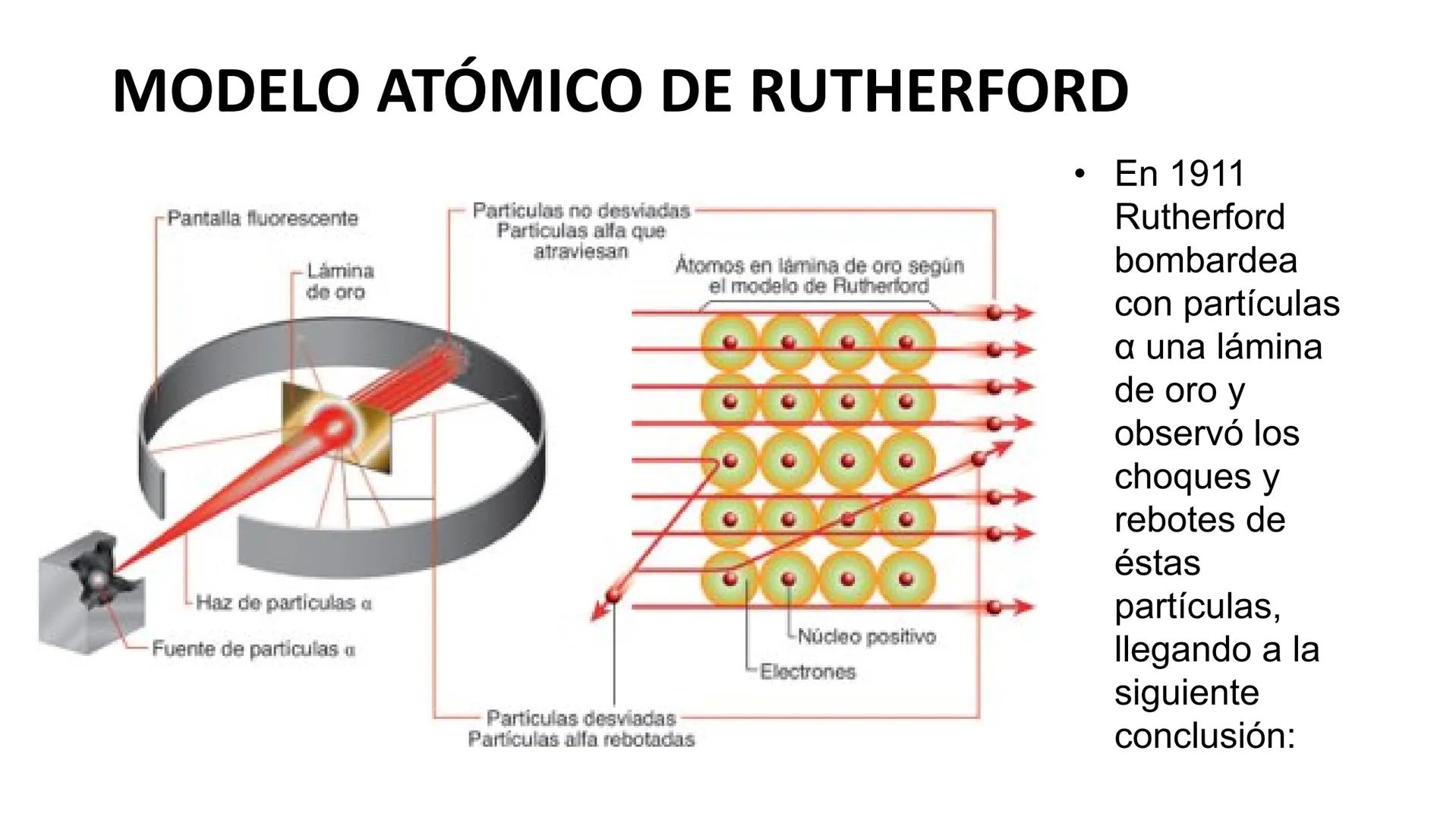
Rutherford hizo uno de los experimentos más famosos de la historia de la química. Bombardeó una lámina de oro muy fina con partículas alfa (partículas con carga positiva) y observó qué pasaba.
Lo que vio le sorprendió mucho: la mayoría de partículas atravesaban la lámina sin problemas, algunas se desviaban ligeramente y unas pocas rebotaban completamente. Esto no encajaba con el modelo de Thomson.
Su experimento demostró que el átomo tenía un núcleo muy pequeño y denso en el centro, con carga positiva, y que el resto era espacio prácticamente vacío.
Analogía útil: Si el núcleo fuera una canica, el átomo completo sería como un estadio de fútbol.
Conclusiones del experimento de Rutherford
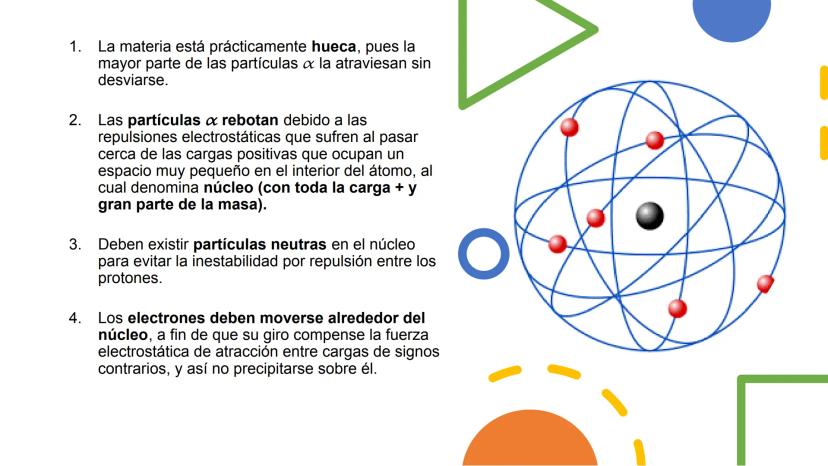
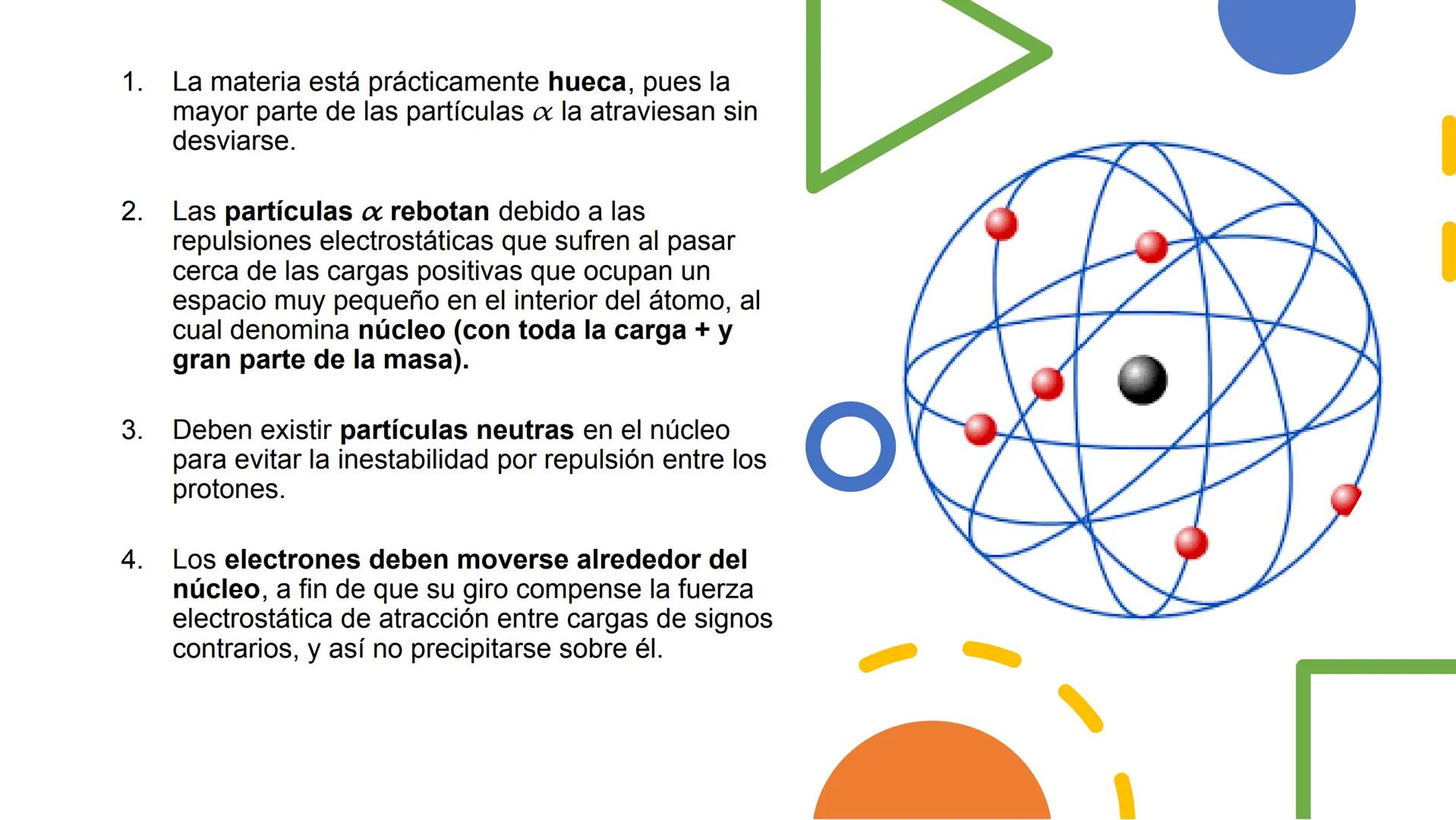
Las observaciones de Rutherford le llevaron a conclusiones revolucionarias. Primero, que la materia está prácticamente hueca, porque la mayoría de partículas alfa pasaban sin problemas.
Segundo, que debe existir un núcleo muy pequeño con toda la carga positiva y la mayor parte de la masa, porque algunas partículas rebotaban. Tercero, que debían existir partículas neutras en el núcleo para explicar toda la masa.
Por último, propuso que los electrones giran alrededor del núcleo, como los planetas alrededor del Sol. Esto evitaría que cayeran sobre el núcleo debido a la atracción eléctrica.
Idea clave: Rutherford descubrió que el átomo tiene una estructura parecida al sistema solar.

Fallos del modelo de Rutherford
Aunque el modelo de Rutherford era mucho mejor que los anteriores, tenía algunos problemas importantes que no podía explicar. El primero era la estabilidad del núcleo: si los protones tienen carga positiva, ¿por qué no se repelen y destrozan el núcleo?
El segundo problema era que la masa del núcleo no coincidía con la masa de los protones que contenía. Faltaba algo para explicar toda esa masa extra.
Estos fallos llevaron a otros científicos a seguir investigando y mejorando el modelo atómico.
Para entender: Cada modelo atómico resolvía algunos problemas pero creaba otros nuevos.

El descubrimiento del neutrón
En 1932, Chadwick resolvió uno de los misterios del átomo. Bombardeando átomos de berilio con partículas alfa, descubrió una nueva partícula sin carga eléctrica y con masa similar al protón: el neutrón.
Este descubrimiento explicó los dos problemas del modelo de Rutherford. Los neutrones aportan la masa que faltaba en el núcleo y ayudan a mantener unidos a los protones, evitando que se repelan.
Ahora ya conocemos las tres partículas subatómicas básicas: electrones (en la corteza), protones y neutrones (en el núcleo). Esta es la base de la estructura atómica actual.
Dato importante: Los neutrones actúan como el "pegamento" que mantiene unido el núcleo atómico.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: modelo atómico
9Formulación Inorgánica Química 1°BACH
Guía con lo necesario para formular y trucos
mol,moleculas,atomos
como calcular los moles moleculas sus gramos etc
Modelos atomicos
Apuntes de modelos atómicos
El átomo
Explicación de los modelos atómicos, número atómico y másico, tabla periódica, propiedades periódicas de los elementos, electrones desapareados, enlaces y diagrama de Lewis.
Estructura de lewis
Os gusta?
Modelos atómicos de Dalton, THomson, Rutherford y Bohr
Presentación
Átomo
Incluye las propiedades del átomo y los tipos de enlaces
Los átomos
esquema/resumen los átomos
Estructura anatómica
Estructura anatómica modelos atómicos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Estructura Atómica y Enlace Químico: Guía Completa de Estudio
La estructura atómicaes fundamental para entender toda la química que estudiarás este año. Desde las primeras ideas de los antiguos griegos hasta los modelos modernos, verás cómo los científicos han ido descubriendo poco a poco qué hay dentro de... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Estructura atómica, sistema periódico y enlace químico
¡Empezamos el tema más importante de química! Todo lo que estudiarás este año tiene que ver con cómo están hechos los átomos y cómo se unen entre ellos.
Este tema te dará las bases para entender por qué los elementos se comportan como lo hacen. También descubrirás cómo se forman los diferentes tipos de enlaces químicos.
¿Sabías que...? Los conceptos de este tema aparecen en casi todas las preguntas de selectividad de química.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Los primeros pasos: Demócrito vs Aristóteles
La historia del átomo empezó hace más de 2000 años con una gran discusión. Demócrito pensaba que si cortabas cualquier cosa en trozos cada vez más pequeños, al final llegarías a una partícula que ya no se podría dividir más: el átomo.
Pero Aristóteles no estaba de acuerdo y propuso que todo estaba hecho de cuatro elementos: tierra, agua, aire y fuego. Su idea fue tan influyente que durante casi 2000 años nadie se atrevió a contradecirle.
Curiosidad: La palabra "átomo" viene del griego y significa "que no se puede dividir".

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La evolución de los modelos atómicos
Un modelo atómico es como un dibujo que nos ayuda a imaginar cómo es un átomo y por qué se comporta de cierta manera. A lo largo de la historia, los científicos han ido mejorando estos modelos.
Los principales modelos que debes conocer son: Dalton (1808), Thomson (1904), Rutherford (1911), Bohr (1913) y Schrödinger (1924). Cada uno aportó algo nuevo y corrigió errores del anterior.
Es como si cada científico hubiera añadido una pieza al puzzle hasta conseguir la imagen que tenemos hoy del átomo.
Para el examen: Tienes que saber las características principales de cada modelo y sus limitaciones.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Modelo atómico de Dalton
Dalton fue el primero en retomar las ideas de Demócrito de forma científica en el siglo XIX. Sus ideas principales eran bastante lógicas para su época.
Según Dalton, la materia está formada por partículas pequeñas e indivisibles. Los átomos del mismo elemento son idénticos en masa y propiedades. Los compuestos se forman cuando se unen átomos en proporciones sencillas.
También propuso que en las reacciones químicas los átomos solo se reorganizan, pero nunca desaparecen ni se transforman en otros elementos. Esta idea sigue siendo válida hoy en día.
Dato clave: El modelo de Dalton explica perfectamente las leyes químicas básicas que estudiarás.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Modelo atómico de Thomson
Thomson descubrió algo que Dalton no sabía: los átomos no son indivisibles. En 1898 propuso que el átomo era como un "pudin de pasas": una esfera de carga positiva con electrones incrustados por toda su superficie.
Este modelo explicaba por qué los átomos son neutros (las cargas positivas y negativas se compensan). También se conoce como el modelo del "pudin de pasas" porque los electrones parecían pasas metidas en un pudin.
Aunque después se demostró que estaba equivocado, Thomson fue el primero en descubrir que había partículas más pequeñas que el átomo.
Recuerda: Thomson descubrió el electrón, la primera partícula subatómica conocida.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El descubrimiento del electrón
Thomson hizo un experimento genial con tubos de rayos catódicos. Cuando aplicaba electricidad a un gas encerrado en un tubo, aparecían unos rayos luminosos que iban del polo negativo al positivo.
Lo más interesante era que estos rayos catódicos se desviaban cuando Thomson ponía cerca campos eléctricos o magnéticos. Esto le demostró que los rayos estaban formados por partículas con carga negativa.
A estas partículas las llamó electrones. Así descubrió que los átomos no eran indivisibles como pensaba Dalton, sino que tenían partes más pequeñas.
Experimento clave: Los tubos de rayos catódicos fueron el primer paso para entender la estructura interna del átomo.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Modelo atómico de Rutherford
Rutherford hizo uno de los experimentos más famosos de la historia de la química. Bombardeó una lámina de oro muy fina con partículas alfa (partículas con carga positiva) y observó qué pasaba.
Lo que vio le sorprendió mucho: la mayoría de partículas atravesaban la lámina sin problemas, algunas se desviaban ligeramente y unas pocas rebotaban completamente. Esto no encajaba con el modelo de Thomson.
Su experimento demostró que el átomo tenía un núcleo muy pequeño y denso en el centro, con carga positiva, y que el resto era espacio prácticamente vacío.
Analogía útil: Si el núcleo fuera una canica, el átomo completo sería como un estadio de fútbol.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Conclusiones del experimento de Rutherford
Las observaciones de Rutherford le llevaron a conclusiones revolucionarias. Primero, que la materia está prácticamente hueca, porque la mayoría de partículas alfa pasaban sin problemas.
Segundo, que debe existir un núcleo muy pequeño con toda la carga positiva y la mayor parte de la masa, porque algunas partículas rebotaban. Tercero, que debían existir partículas neutras en el núcleo para explicar toda la masa.
Por último, propuso que los electrones giran alrededor del núcleo, como los planetas alrededor del Sol. Esto evitaría que cayeran sobre el núcleo debido a la atracción eléctrica.
Idea clave: Rutherford descubrió que el átomo tiene una estructura parecida al sistema solar.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fallos del modelo de Rutherford
Aunque el modelo de Rutherford era mucho mejor que los anteriores, tenía algunos problemas importantes que no podía explicar. El primero era la estabilidad del núcleo: si los protones tienen carga positiva, ¿por qué no se repelen y destrozan el núcleo?
El segundo problema era que la masa del núcleo no coincidía con la masa de los protones que contenía. Faltaba algo para explicar toda esa masa extra.
Estos fallos llevaron a otros científicos a seguir investigando y mejorando el modelo atómico.
Para entender: Cada modelo atómico resolvía algunos problemas pero creaba otros nuevos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El descubrimiento del neutrón
En 1932, Chadwick resolvió uno de los misterios del átomo. Bombardeando átomos de berilio con partículas alfa, descubrió una nueva partícula sin carga eléctrica y con masa similar al protón: el neutrón.
Este descubrimiento explicó los dos problemas del modelo de Rutherford. Los neutrones aportan la masa que faltaba en el núcleo y ayudan a mantener unidos a los protones, evitando que se repelan.
Ahora ya conocemos las tres partículas subatómicas básicas: electrones (en la corteza), protones y neutrones (en el núcleo). Esta es la base de la estructura atómica actual.
Dato importante: Los neutrones actúan como el "pegamento" que mantiene unido el núcleo atómico.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: modelo atómico
9Formulación Inorgánica Química 1°BACH
Guía con lo necesario para formular y trucos
mol,moleculas,atomos
como calcular los moles moleculas sus gramos etc
Modelos atomicos
Apuntes de modelos atómicos
El átomo
Explicación de los modelos atómicos, número atómico y másico, tabla periódica, propiedades periódicas de los elementos, electrones desapareados, enlaces y diagrama de Lewis.
Estructura de lewis
Os gusta?
Modelos atómicos de Dalton, THomson, Rutherford y Bohr
Presentación
Átomo
Incluye las propiedades del átomo y los tipos de enlaces
Los átomos
esquema/resumen los átomos
Estructura anatómica
Estructura anatómica modelos atómicos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.