¿Te has preguntado alguna vez cómo los científicos organizaron todos... Mostrar más
El Sistema Periódico y sus Propiedades







Sistema Periódico: Propiedades que se Repiten
El sistema periódico es la base de toda la química moderna. Las propiedades periódicas son características de los elementos que se repiten de forma regular cuando los ordenamos por su número atómico.
Estas propiedades incluyen cosas como el tamaño de los átomos, cuánto les cuesta perder electrones, o qué tan reactivos son. Lo genial es que siguen patrones predecibles que te ayudan a entender el comportamiento químico sin tener que memorizar todo.
💡 Dato curioso: La palabra "periódico" significa que algo se repite en intervalos regulares, como las estaciones del año.

Los Primeros Intentos: Tríadas de Döbereiner (1817)
Antes de la tabla periódica moderna, los científicos ya notaban que algunos elementos se comportaban de manera similar. Döbereiner fue el primero en organizarlos en grupos de tres llamados tríadas.
Su descubrimiento fue brillante: si tomabas tres elementos con propiedades parecidas y calculabas la media de sus pesos atómicos, ¡el resultado coincidía con el peso del elemento del medio! Por ejemplo, con litio (7), sodio (23) y potasio (39): (7+39)/2 = 23.
Las tríadas incluían metales reactivos como Li-Na-K, no metales como S-Se-Te, y halógenos como Cl-Br-I. Cada grupo tenía propiedades químicas muy similares, lo que sugería que había un patrón oculto en la naturaleza.
💡 Recuerda: Las tríadas fueron el primer indicio de que los elementos no eran completamente aleatorios.
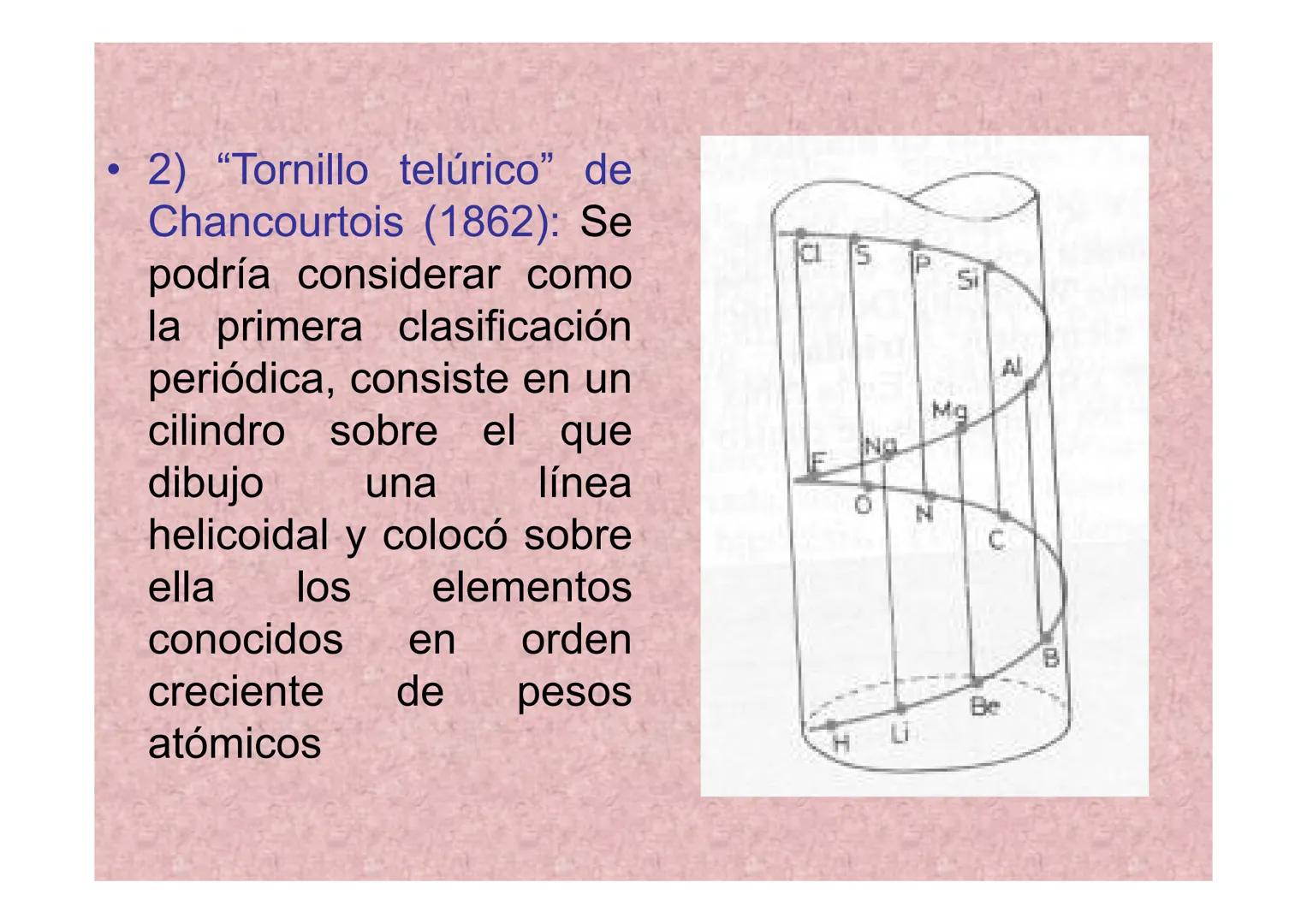
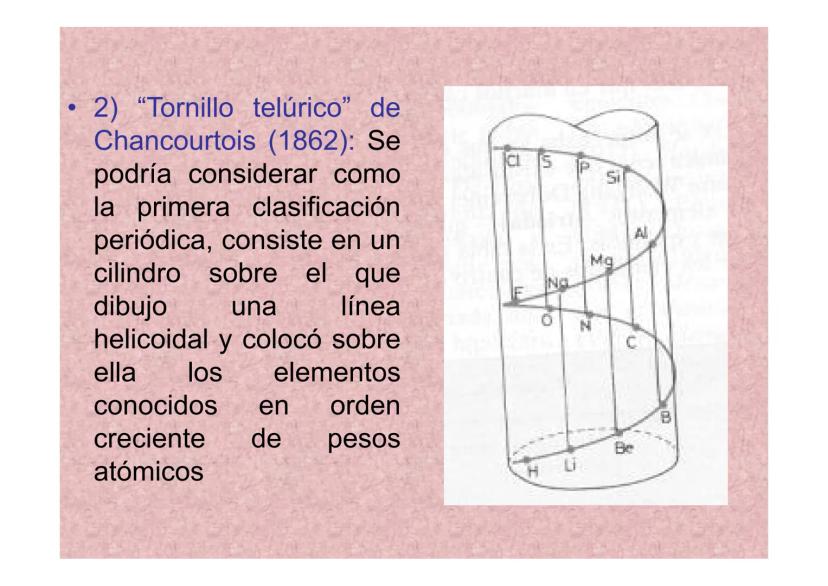
El Tornillo Telúrico de Chancourtois (1862)
Chancourtois tuvo una idea revolucionaria: crear la primera clasificación realmente periódica. Imaginó un cilindro con una línea en espiral donde colocó los elementos ordenados por peso atómico creciente.
Su "tornillo telúrico" mostraba que cada 16 unidades de peso atómico, las propiedades se repetían. Los elementos con características similares quedaban alineados verticalmente en el cilindro.
Aunque su trabajo fue ignorado en su época (¡lo publicó en una revista de geología!), fue el primero en demostrar que las propiedades de los elementos son verdaderamente periódicas.
💡 Piénsalo así: Era como enrollar una cinta con todos los elementos - los similares quedaban uno encima del otro.

La Ley de las Octavas de Newlands (1863)
Newlands propuso algo parecido a las escalas musicales: la ley de las octavas. Observó que si ordenabas los elementos por peso atómico, cada octavo elemento tenía propiedades similares al primero.
Su tabla mostraba patrones claros: hidrógeno se parecía al litio, berilio al sodio, boro al magnesio, etc. Era como si los elementos "cantaran" la misma melodía cada ocho notas.
Lamentablemente, sus contemporáneos se burlaron de él y lo ridiculizaron. ¡Incluso le preguntaron si había intentado ordenar los elementos alfabéticamente! Pero 23 años después, la Royal Society le dio la razón con la prestigiosa Davy Medal.
💡 Lección importante: A veces las ideas revolucionarias necesitan tiempo para ser aceptadas.
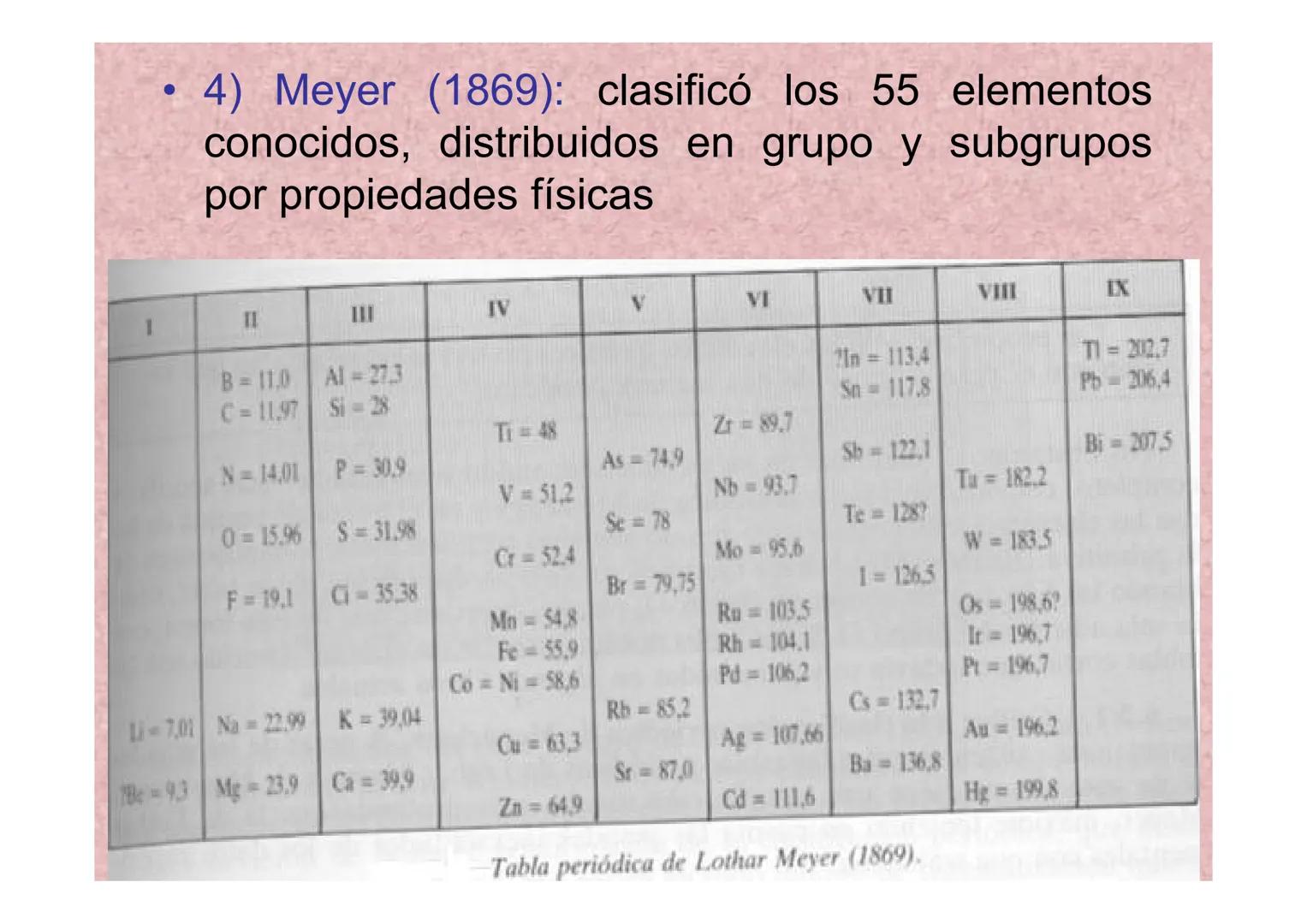
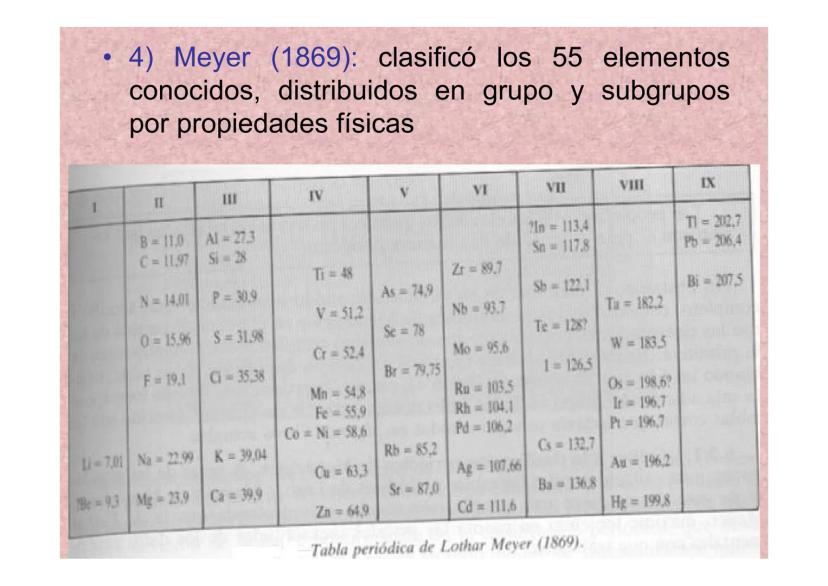
Meyer (1869): Clasificación por Propiedades Físicas
Meyer fue más sistemático y clasificó los 55 elementos conocidos usando principalmente propiedades físicas. Su tabla era más completa y precisa que las anteriores.
Organizó los elementos en grupos y subgrupos, creando una estructura similar a la tabla periódica actual. Su trabajo incluía pesos atómicos más exactos y mostraba patrones claros en las propiedades.
Lo interesante es que Meyer trabajó de forma independiente a Mendeleiev, llegando a conclusiones muy similares. Esto demostró que los patrones periódicos eran reales y no casualidades.
💡 Dato importante: Cuando dos científicos llegan a la misma conclusión por separado, es una fuerte evidencia de que están en lo cierto.
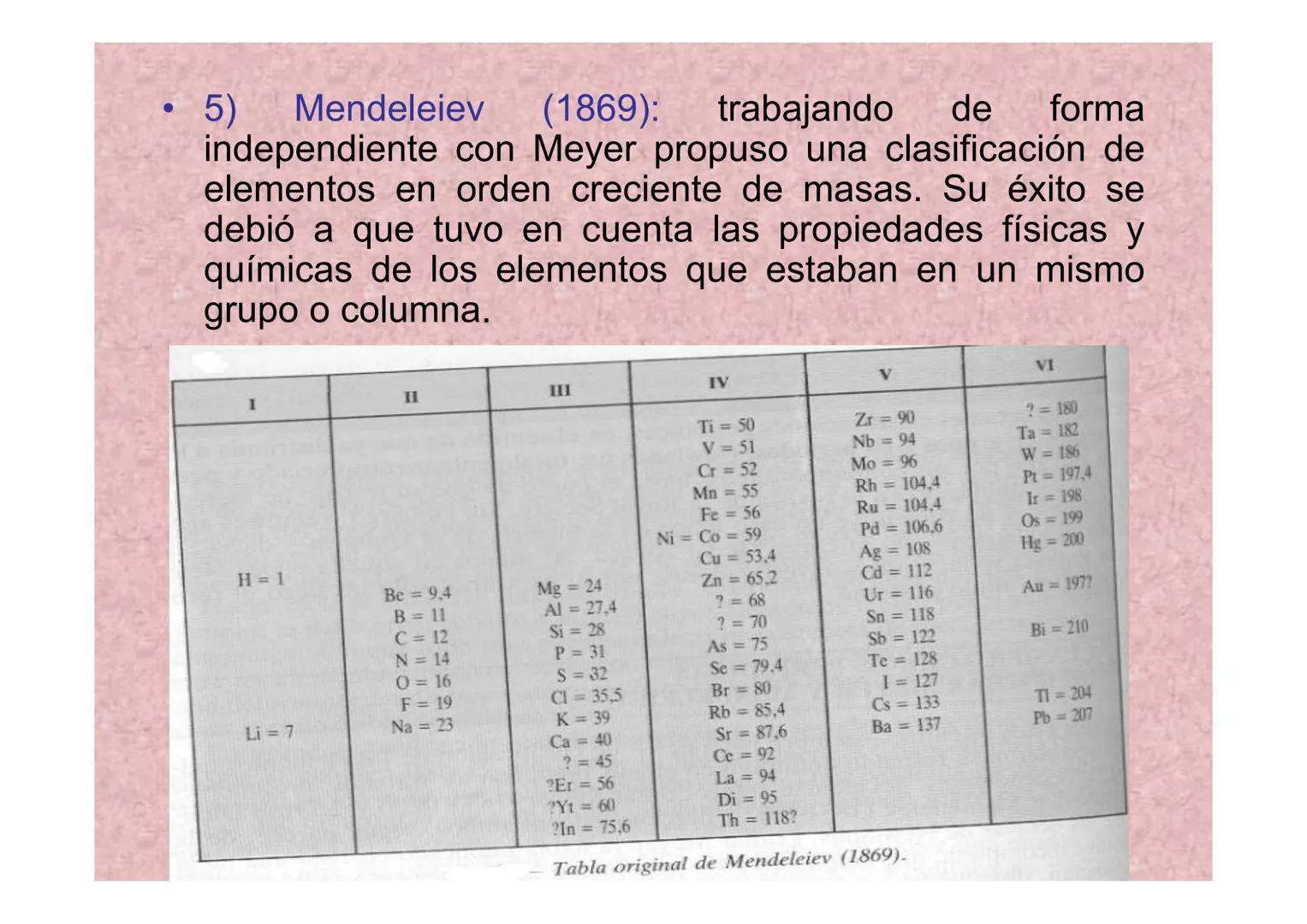
Mendeleiev (1869): El Genio de las Predicciones
Mendeleiev revolucionó la química con su tabla periódica. Su genialidad no solo fue ordenar los elementos, sino predecir las propiedades de elementos aún no descubiertos.
Dejó espacios vacíos donde sabía que debían existir elementos y les puso nombres temporales como "eka-silicio" o "eka-aluminio". Cuando se descubrieron el germanio y el galio, ¡sus propiedades coincidían perfectamente con sus predicciones!
Su tabla consideraba tanto propiedades físicas como químicas, y tuvo el valor de cambiar el orden cuando las propiedades no encajaban con los pesos atómicos. Esto fue clave para el éxito de su sistema.
💡 El secreto del éxito: Mendeleiev se atrevió a hacer predicciones verificables, la esencia del método científico.
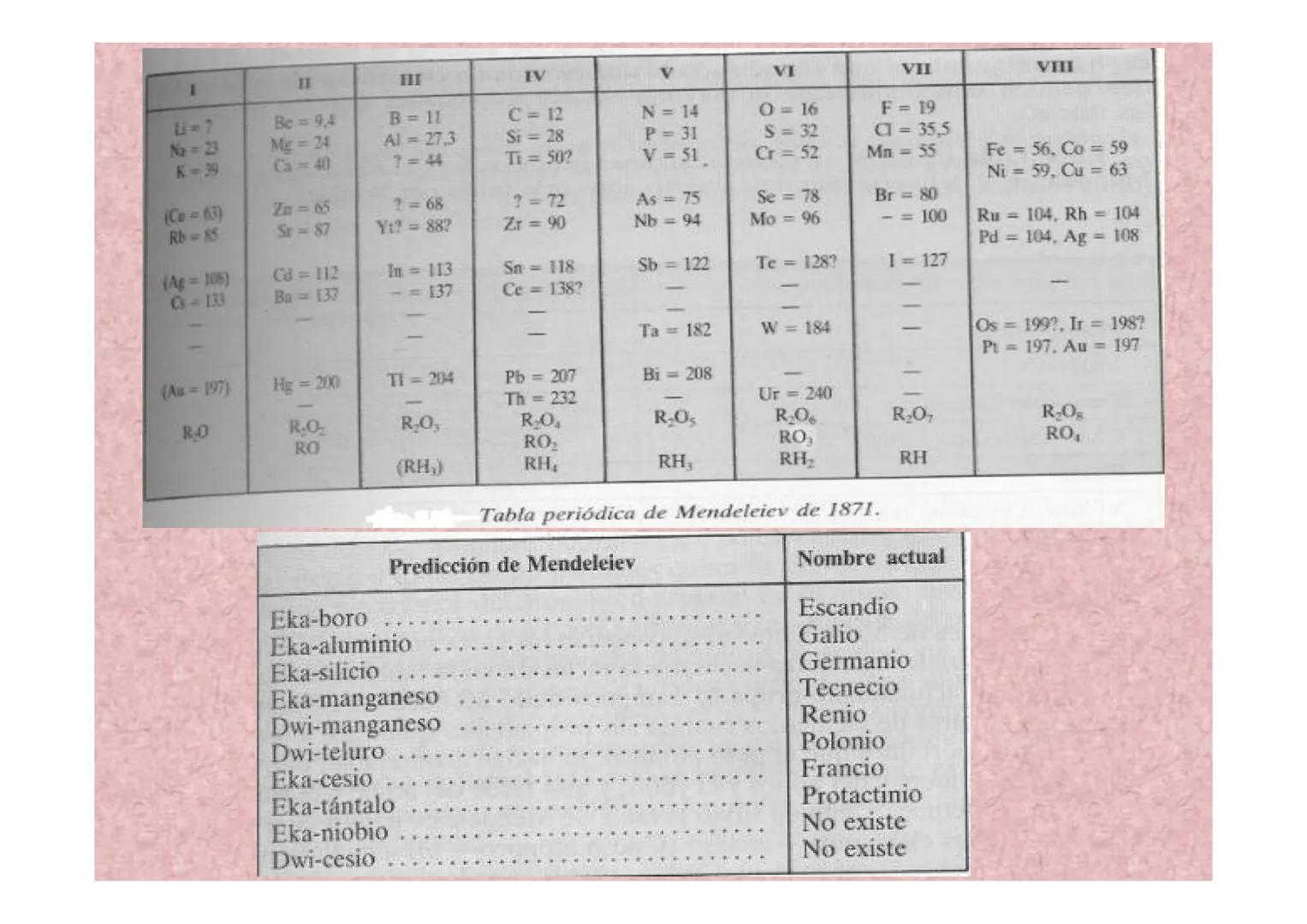
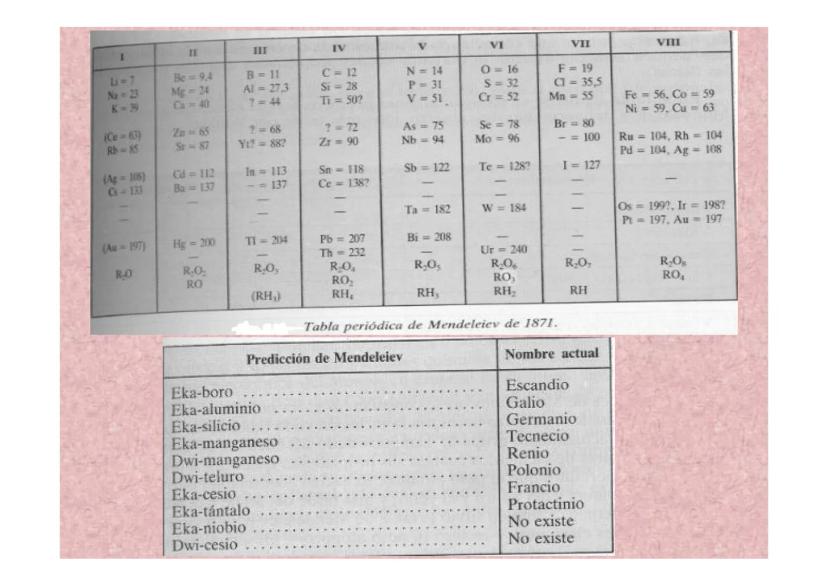
La Tabla Mejorada de 1871 y Predicciones Exitosas
En 1871, Mendeleiev perfeccionó su tabla y hizo predicciones aún más detalladas. Predijo elementos como el escandio, galio, germanio, tecnecio y renio, describiendo sus propiedades con increíble precisión.
Su sistema de nomenclatura era genial: "eka" significaba "uno después" en sánscrito, y "dwi" significaba "dos después". Así, eka-silicio era el elemento que vendría después del silicio en su tabla.
La tabla de 1871 incluía las fórmulas de los óxidos (RO, R₂O₃, etc.) que cada grupo formaba, mostrando patrones químicos claros. Esto ayudaba a entender por qué ciertos elementos se comportaban de manera similar.
💡 Impresionante: Mendeleiev predijo correctamente el peso atómico, densidad, color y propiedades químicas de elementos que no se descubrirían hasta décadas después.
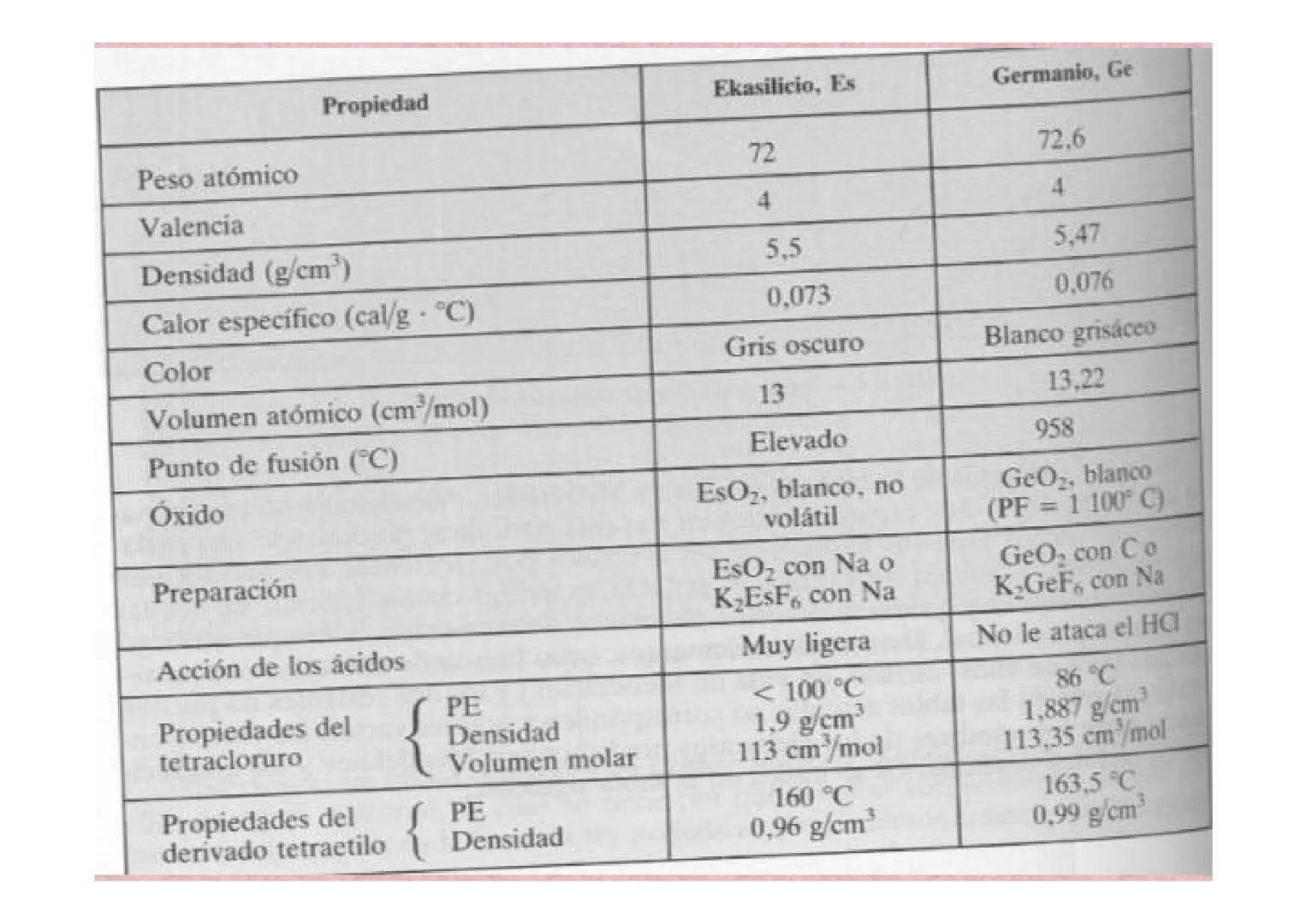
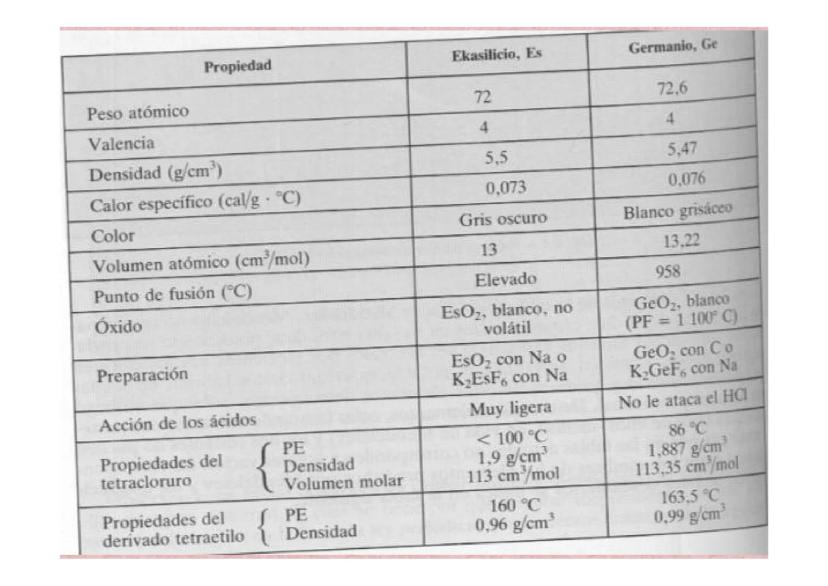
La Predicción Perfecta: Ekasilicio vs Germanio
La predicción más famosa de Mendeleiev fue el "ekasilicio", que resultó ser el germanio descubierto en 1886. La precisión de sus predicciones fue asombrosa y convenció a toda la comunidad científica.
Predijo que tendría peso atómico 72 (real: 72.6), densidad 5.5 g/cm³ (real: 5.47), y que sería de color gris oscuro. ¡Incluso acertó en las propiedades de sus compuestos como el tetracloruro!
Esta predicción exitosa demostró que la tabla periódica no era solo una herramienta de clasificación, sino una ventana para entender la estructura fundamental de la materia.
💡 Mensaje clave: Cuando una teoría puede predecir lo desconocido con precisión, sabes que has descubierto algo fundamental sobre la naturaleza.

Distribución Electrónica: La Base Moderna
La distribución electrónica explica cómo se organizan los electrones alrededor del núcleo atómico. Se escribe como nxᵉ, donde n es el nivel energético, x el tipo de orbital (s, p, d, f) y e el número de electrones.
La capa de valencia es la más externa y la más importante porque determina cómo se comporta químicamente el átomo. Es como la "personalidad química" del elemento - define con qué otros elementos puede combinarse.
Para escribir configuraciones electrónicas correctamente, necesitas seguir principios específicos que explican por qué los electrones se distribuyen de cierta manera y no de otra.
💡 Piénsalo así: Es como asignar asientos en un teatro - hay reglas sobre dónde puede sentarse cada electrón.

Principio de Exclusión de Pauli
El principio de exclusión de Pauli es fundamental: en un átomo no puede haber dos electrones con los cuatro números cuánticos iguales. Esto significa que cada orbital puede contener máximo 2 electrones.
Las matemáticas son simples pero poderosas: en cada nivel n pueden haber máximo n² orbitales y 2n² electrones. Por ejemplo, en el nivel 2: máximo 4 orbitales y 8 electrones.
Este principio explica por qué los átomos tienen el tamaño que tienen y por qué la tabla periódica tiene la estructura que conocemos. Sin él, todos los electrones se amontonarían en el orbital más bajo.
💡 Regla de oro: Dos electrones por orbital como máximo, y deben tener spines opuestos (como dos personas durmiendo en una cama doble).
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: niveles de energía
9Formulación
Formulación química
SÍMBOLOS Y VALENCIAS
Valencias
La estructura del átomo
Esquema del tema estructura del átomo para selectividad (temario 1º Bachillerato)
CONFIGURACIÓN ELECTRÓNICA
Apuntes de la configuración electrónica de física y química.
Química inorgánica
Estudia todos los tipos de compuestos dentro de la química inorgánica, cómo se nombran, las valencias, etc.
NÚMEROS CUÁNTICOS
Teoría y ejercicio
Estructura atómica y tabla periódica
Resúmenes
RADIO ATÓMICO, EI, AE, ELECTRONEGATIVIDAD…
Radio atómico, ionico, especies isoelectronicas…
El átomo y el sistema periódico. Propiedades periódicas.
Contiene 6 de las propiedades periódicas, los números cuánticos, la configuración electrónica (reglas del principio se Aufbau),etc.
Contenidos más populares de Física i Química
9Formulario Dinámica y Cinemática
Aquí un esquema de todas las formulas, válido sobre todo para bachillerato y 4ESO. También incluyo un ejercicio de dinámica resuelto bastante completo
Resumen Dinamica fisica 1 bach
Resumen Dinamica fisica 1 bachillerato
Tabla periódica
Aprende sobre la tabla periódica.
DINÁMICA
teoría + ejercicios resueltos
Cinemática y dinámica
- Magnitudes del movimiento, MRU, MRUA, Caída libre/tiro vertical
Mcu y mcua
Movimiento circular uniforme y movimiento circular uniforme acelerado
fuerzas
apuntes sobre fuerzas
Fuerzas
física y química
MRU Y MRUA
movimiento rectilíneo uniforme y movimiento rectilíneo uniformemente acelerado
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
El Sistema Periódico y sus Propiedades
¿Te has preguntado alguna vez cómo los científicos organizaron todos los elementos químicos de manera tan ordenada? La tabla periódica que usas hoy no apareció de la noche a la mañana - fue el resultado de décadas de trabajo e... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sistema Periódico: Propiedades que se Repiten
El sistema periódico es la base de toda la química moderna. Las propiedades periódicas son características de los elementos que se repiten de forma regular cuando los ordenamos por su número atómico.
Estas propiedades incluyen cosas como el tamaño de los átomos, cuánto les cuesta perder electrones, o qué tan reactivos son. Lo genial es que siguen patrones predecibles que te ayudan a entender el comportamiento químico sin tener que memorizar todo.
💡 Dato curioso: La palabra "periódico" significa que algo se repite en intervalos regulares, como las estaciones del año.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Los Primeros Intentos: Tríadas de Döbereiner (1817)
Antes de la tabla periódica moderna, los científicos ya notaban que algunos elementos se comportaban de manera similar. Döbereiner fue el primero en organizarlos en grupos de tres llamados tríadas.
Su descubrimiento fue brillante: si tomabas tres elementos con propiedades parecidas y calculabas la media de sus pesos atómicos, ¡el resultado coincidía con el peso del elemento del medio! Por ejemplo, con litio (7), sodio (23) y potasio (39): (7+39)/2 = 23.
Las tríadas incluían metales reactivos como Li-Na-K, no metales como S-Se-Te, y halógenos como Cl-Br-I. Cada grupo tenía propiedades químicas muy similares, lo que sugería que había un patrón oculto en la naturaleza.
💡 Recuerda: Las tríadas fueron el primer indicio de que los elementos no eran completamente aleatorios.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El Tornillo Telúrico de Chancourtois (1862)
Chancourtois tuvo una idea revolucionaria: crear la primera clasificación realmente periódica. Imaginó un cilindro con una línea en espiral donde colocó los elementos ordenados por peso atómico creciente.
Su "tornillo telúrico" mostraba que cada 16 unidades de peso atómico, las propiedades se repetían. Los elementos con características similares quedaban alineados verticalmente en el cilindro.
Aunque su trabajo fue ignorado en su época (¡lo publicó en una revista de geología!), fue el primero en demostrar que las propiedades de los elementos son verdaderamente periódicas.
💡 Piénsalo así: Era como enrollar una cinta con todos los elementos - los similares quedaban uno encima del otro.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La Ley de las Octavas de Newlands (1863)
Newlands propuso algo parecido a las escalas musicales: la ley de las octavas. Observó que si ordenabas los elementos por peso atómico, cada octavo elemento tenía propiedades similares al primero.
Su tabla mostraba patrones claros: hidrógeno se parecía al litio, berilio al sodio, boro al magnesio, etc. Era como si los elementos "cantaran" la misma melodía cada ocho notas.
Lamentablemente, sus contemporáneos se burlaron de él y lo ridiculizaron. ¡Incluso le preguntaron si había intentado ordenar los elementos alfabéticamente! Pero 23 años después, la Royal Society le dio la razón con la prestigiosa Davy Medal.
💡 Lección importante: A veces las ideas revolucionarias necesitan tiempo para ser aceptadas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Meyer (1869): Clasificación por Propiedades Físicas
Meyer fue más sistemático y clasificó los 55 elementos conocidos usando principalmente propiedades físicas. Su tabla era más completa y precisa que las anteriores.
Organizó los elementos en grupos y subgrupos, creando una estructura similar a la tabla periódica actual. Su trabajo incluía pesos atómicos más exactos y mostraba patrones claros en las propiedades.
Lo interesante es que Meyer trabajó de forma independiente a Mendeleiev, llegando a conclusiones muy similares. Esto demostró que los patrones periódicos eran reales y no casualidades.
💡 Dato importante: Cuando dos científicos llegan a la misma conclusión por separado, es una fuerte evidencia de que están en lo cierto.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Mendeleiev (1869): El Genio de las Predicciones
Mendeleiev revolucionó la química con su tabla periódica. Su genialidad no solo fue ordenar los elementos, sino predecir las propiedades de elementos aún no descubiertos.
Dejó espacios vacíos donde sabía que debían existir elementos y les puso nombres temporales como "eka-silicio" o "eka-aluminio". Cuando se descubrieron el germanio y el galio, ¡sus propiedades coincidían perfectamente con sus predicciones!
Su tabla consideraba tanto propiedades físicas como químicas, y tuvo el valor de cambiar el orden cuando las propiedades no encajaban con los pesos atómicos. Esto fue clave para el éxito de su sistema.
💡 El secreto del éxito: Mendeleiev se atrevió a hacer predicciones verificables, la esencia del método científico.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La Tabla Mejorada de 1871 y Predicciones Exitosas
En 1871, Mendeleiev perfeccionó su tabla y hizo predicciones aún más detalladas. Predijo elementos como el escandio, galio, germanio, tecnecio y renio, describiendo sus propiedades con increíble precisión.
Su sistema de nomenclatura era genial: "eka" significaba "uno después" en sánscrito, y "dwi" significaba "dos después". Así, eka-silicio era el elemento que vendría después del silicio en su tabla.
La tabla de 1871 incluía las fórmulas de los óxidos (RO, R₂O₃, etc.) que cada grupo formaba, mostrando patrones químicos claros. Esto ayudaba a entender por qué ciertos elementos se comportaban de manera similar.
💡 Impresionante: Mendeleiev predijo correctamente el peso atómico, densidad, color y propiedades químicas de elementos que no se descubrirían hasta décadas después.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La Predicción Perfecta: Ekasilicio vs Germanio
La predicción más famosa de Mendeleiev fue el "ekasilicio", que resultó ser el germanio descubierto en 1886. La precisión de sus predicciones fue asombrosa y convenció a toda la comunidad científica.
Predijo que tendría peso atómico 72 (real: 72.6), densidad 5.5 g/cm³ (real: 5.47), y que sería de color gris oscuro. ¡Incluso acertó en las propiedades de sus compuestos como el tetracloruro!
Esta predicción exitosa demostró que la tabla periódica no era solo una herramienta de clasificación, sino una ventana para entender la estructura fundamental de la materia.
💡 Mensaje clave: Cuando una teoría puede predecir lo desconocido con precisión, sabes que has descubierto algo fundamental sobre la naturaleza.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Distribución Electrónica: La Base Moderna
La distribución electrónica explica cómo se organizan los electrones alrededor del núcleo atómico. Se escribe como nxᵉ, donde n es el nivel energético, x el tipo de orbital (s, p, d, f) y e el número de electrones.
La capa de valencia es la más externa y la más importante porque determina cómo se comporta químicamente el átomo. Es como la "personalidad química" del elemento - define con qué otros elementos puede combinarse.
Para escribir configuraciones electrónicas correctamente, necesitas seguir principios específicos que explican por qué los electrones se distribuyen de cierta manera y no de otra.
💡 Piénsalo así: Es como asignar asientos en un teatro - hay reglas sobre dónde puede sentarse cada electrón.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Principio de Exclusión de Pauli
El principio de exclusión de Pauli es fundamental: en un átomo no puede haber dos electrones con los cuatro números cuánticos iguales. Esto significa que cada orbital puede contener máximo 2 electrones.
Las matemáticas son simples pero poderosas: en cada nivel n pueden haber máximo n² orbitales y 2n² electrones. Por ejemplo, en el nivel 2: máximo 4 orbitales y 8 electrones.
Este principio explica por qué los átomos tienen el tamaño que tienen y por qué la tabla periódica tiene la estructura que conocemos. Sin él, todos los electrones se amontonarían en el orbital más bajo.
💡 Regla de oro: Dos electrones por orbital como máximo, y deben tener spines opuestos (como dos personas durmiendo en una cama doble).
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: niveles de energía
9Formulación
Formulación química
SÍMBOLOS Y VALENCIAS
Valencias
La estructura del átomo
Esquema del tema estructura del átomo para selectividad (temario 1º Bachillerato)
CONFIGURACIÓN ELECTRÓNICA
Apuntes de la configuración electrónica de física y química.
Química inorgánica
Estudia todos los tipos de compuestos dentro de la química inorgánica, cómo se nombran, las valencias, etc.
NÚMEROS CUÁNTICOS
Teoría y ejercicio
Estructura atómica y tabla periódica
Resúmenes
RADIO ATÓMICO, EI, AE, ELECTRONEGATIVIDAD…
Radio atómico, ionico, especies isoelectronicas…
El átomo y el sistema periódico. Propiedades periódicas.
Contiene 6 de las propiedades periódicas, los números cuánticos, la configuración electrónica (reglas del principio se Aufbau),etc.
Contenidos más populares de Física i Química
9Formulario Dinámica y Cinemática
Aquí un esquema de todas las formulas, válido sobre todo para bachillerato y 4ESO. También incluyo un ejercicio de dinámica resuelto bastante completo
Resumen Dinamica fisica 1 bach
Resumen Dinamica fisica 1 bachillerato
Tabla periódica
Aprende sobre la tabla periódica.
DINÁMICA
teoría + ejercicios resueltos
Cinemática y dinámica
- Magnitudes del movimiento, MRU, MRUA, Caída libre/tiro vertical
Mcu y mcua
Movimiento circular uniforme y movimiento circular uniforme acelerado
fuerzas
apuntes sobre fuerzas
Fuerzas
física y química
MRU Y MRUA
movimiento rectilíneo uniforme y movimiento rectilíneo uniformemente acelerado
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.