¿Sabías que tu cuerpo es básicamente una fábrica química súper... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
1,324
•
Actualizado May 15, 2026
•
Alicia Cereto Jiménez
@aliciaceretojim
¿Sabías que tu cuerpo es básicamente una fábrica química súper... Mostrar más








La vida tal como la conoces está construida con átomos que se unen como piezas de LEGO para formar estructuras más complejas. Estos átomos no se juntan al azar - siguen reglas químicas específicas que determinan cómo funciona todo en tu cuerpo.
Los enlaces químicos son como diferentes tipos de pegamento: algunos son súper fuertes y mantienen unidas las moléculas por dentro, mientras que otros son más débiles pero permiten que las moléculas interactúen entre ellas. Esta diferencia es clave para entender cómo funciona la biología.
💡 Piénsalo así: Los enlaces fuertes son como los clavos que mantienen una casa en pie, los débiles son como el velcro que te permite abrir y cerrar tu mochila fácilmente.

Estos son los enlaces que mantienen unidos los átomos dentro de cada molécula. Son como matrimonios químicos: duraderos y estables.
El enlace covalente es el más común en biología. Aquí los átomos "comparten" electrones como roommates compartiendo gastos. Puede ser polar (uno atrae más los electrones) o apolar (comparten por igual). Moléculas como el agua (H₂O) son polares - por eso el agua tiene propiedades tan especiales.
El enlace iónico es diferente: un átomo le "regala" electrones a otro. Uno se vuelve positivo (catión) y otro negativo (anión), y se atraen como imanes opuestos. Esto forma cristales ordenados como la sal de mesa (NaCl).
🧪 Dato curioso: La diferencia entre estos enlaces explica por qué el aceite y el agua no se mezclan, pero la sal sí se disuelve en agua.

Estos enlaces débiles son los verdaderos héroes de la biología. Permiten que las moléculas interactúen, se separen y vuelvan a unirse - exactamente lo que necesitas para procesos como la digestión o la respiración.
Las fuerzas electrostáticas atraen cargas opuestas, como cuando un enzima se une temporalmente a su sustrato. Las fuerzas de solvatación explican por qué la sal se disuelve en agua - cada ion se rodea de moléculas de agua como fans rodeando a una estrella.
Las interacciones hidrofóbicas son fascinantes: las moléculas que "odian" el agua se juntan entre ellas para evitarla. Esto forma las membranas de tus células. Las fuerzas de Van der Waals son súper débiles individualmente, pero juntas son poderosas - como una multitud de hormigas moviendo algo pesado.
Los enlaces de hidrógeno son especiales: determinan por qué el agua es líquida a temperatura ambiente y por qué el ADN tiene su forma característica.
🔬 Aplicación práctica: Estos enlaces débiles explican cómo funcionan los jabones, por qué sudas para refrescarte, y cómo las proteínas cambian de forma.

No todos los elementos químicos son igual de importantes para la vida. Hay una "lista VIP" de elementos que tu cuerpo usa constantemente.
Los bioelementos primarios (C, H, O, N, P, S) forman el 98% de tu peso corporal. Son como los ingredientes principales de una receta - sin ellos no hay vida posible. El carbono es la estrella: puede formar cuatro enlaces y crear cadenas largas y complejas.
Los bioelementos secundarios (Ca, Mg, Na, K, Cl) son el 2% restante pero súper importantes. El calcio endurece tus huesos, el sodio y potasio hacen que tus neuronas funcionen, y el magnesio es parte de la clorofila de las plantas.
Los oligoelementos aparecen en cantidades mínimas pero son esenciales. El hierro transporta oxígeno en tu sangre, el zinc fortalece tu sistema inmune, y el cobre ayuda en la producción de energía.
⚡ Dato impactante: Aunque el hierro representa menos del 0.01% de tu peso, sin él te asfixiarías porque no podrías transportar oxígeno.

El carbono es el elemento perfecto para formar la base de la vida. Puede crear cuatro enlaces súper estables, formar cadenas largas, anillos y estructuras 3D complejas. Además, abunda en la Tierra y se une igual de bien al oxígeno y al hidrógeno.
Las biomoléculas se dividen en dos grupos principales. Las inorgánicas (agua y sales minerales) también están en la materia no viva. Las orgánicas (glúcidos, lípidos, proteínas y ácidos nucleicos) son exclusivas de los seres vivos y todas tienen esqueletos de carbono.
El agua es la molécula más abundante de tu cuerpo - ¡representas un 75% de agua! Aparece como agua estructural (parte de las células), circulante (transporta nutrientes), y metabólica (forma parte de moléculas y no se puede perder).
La estructura del agua es simple pero genial: un oxígeno conectado a dos hidrógenos. Como el oxígeno atrae más los electrones, la molécula se comporta como un imán pequeño (dipolo), lo que le da propiedades únicas.
💧 Conexión personal: Literalmente eres más agua que cualquier otra cosa. Tu cerebro es 80% agua y tus músculos 75%.
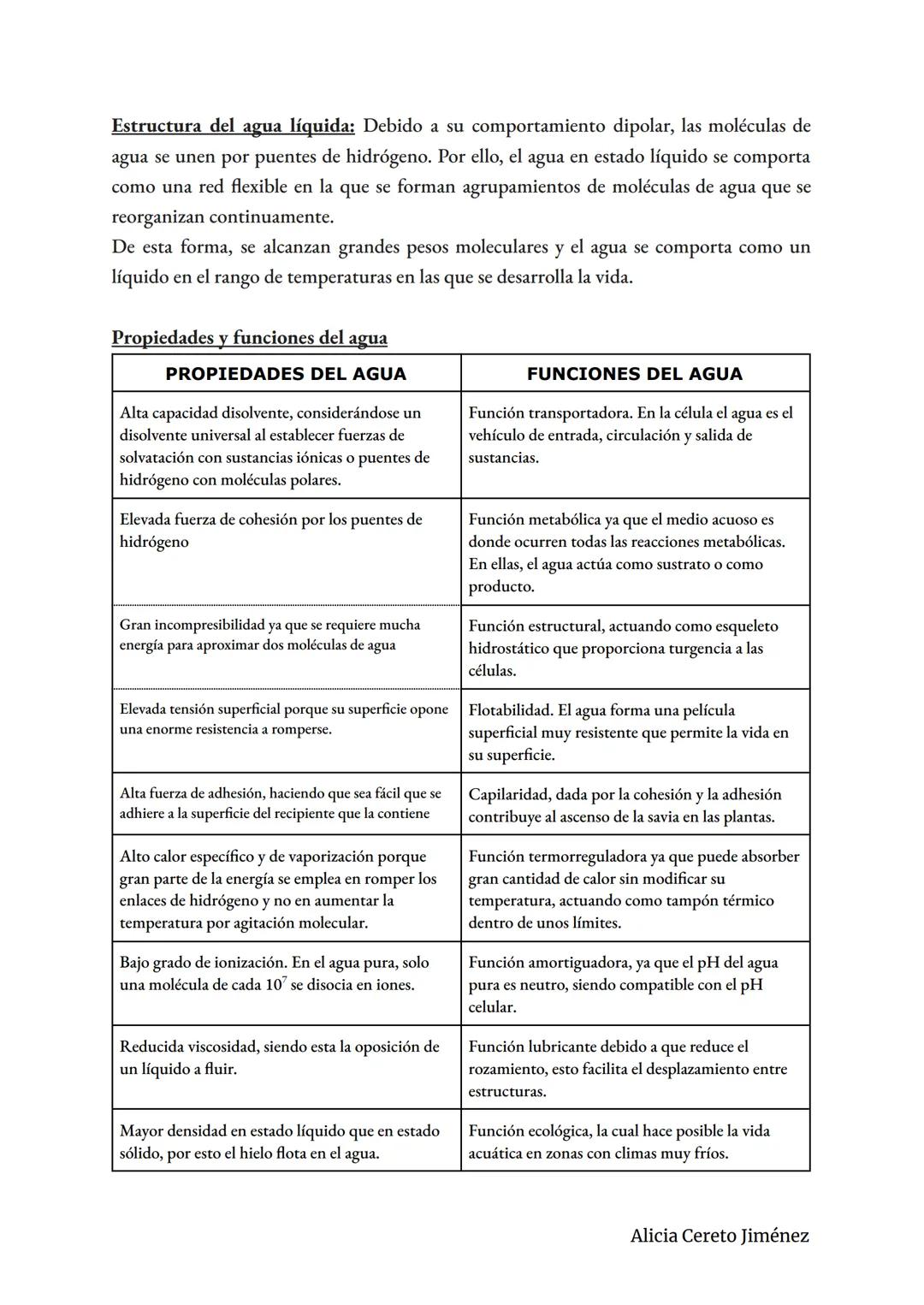
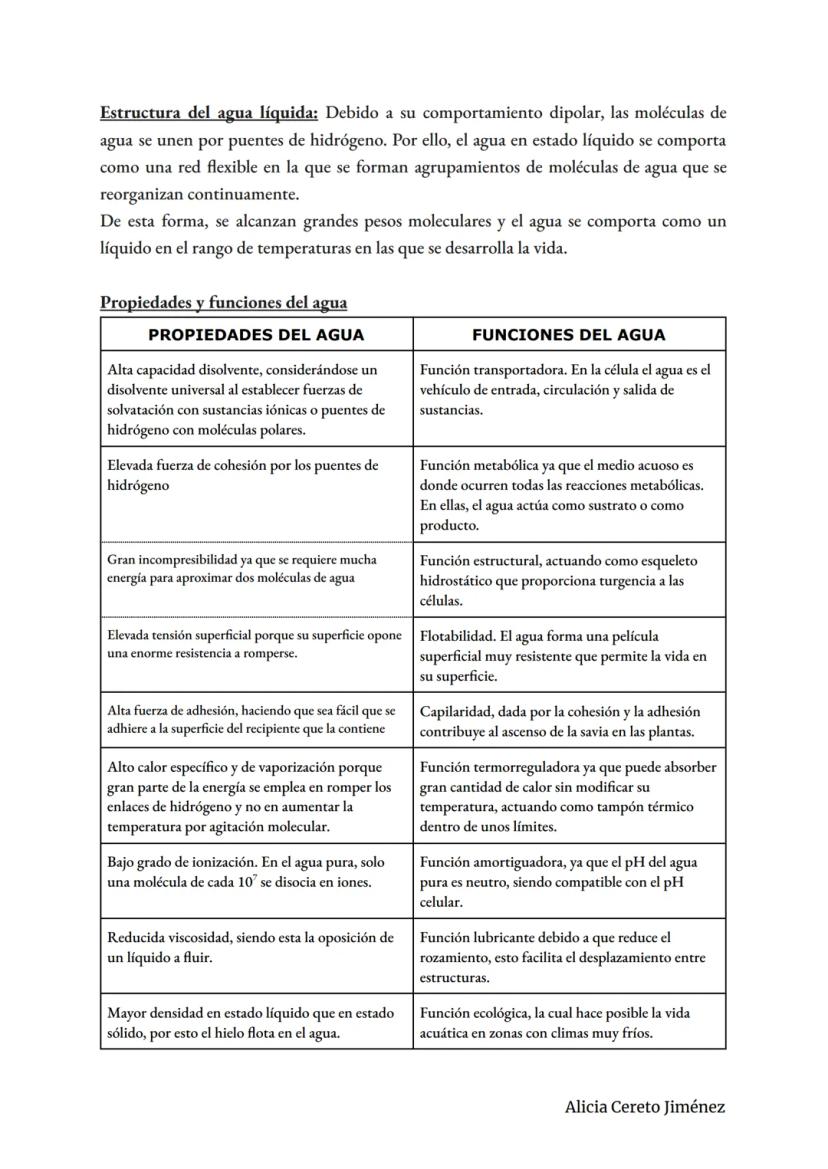
El agua líquida forma una red flexible de moléculas unidas por puentes de hidrógeno que se reorganizan constantemente. Esto le da propiedades increíbles que hacen posible la vida.
Como disolvente universal, el agua puede disolver casi todo lo que tu cuerpo necesita transportar. Su alta cohesión (las moléculas se "pegan" entre sí) y adhesión (se pega a otras superficies) permite que las plantas suban agua desde las raíces hasta las hojas.
Su función termorreguladora es clave: puede absorber muchísimo calor sin cambiar mucho de temperatura, actuando como un termostato natural. Por eso no te sobrecalientas fácilmente y el sudor te refresca tan eficazmente.
El agua también actúa como esqueleto hidrostático (da firmeza a las células), lubricante (reduce rozamiento entre tejidos), y medio de reacción para todos los procesos metabólicos. Su densidad menor en estado sólido permite que los peces sobrevivan bajo el hielo en invierno.
🌡️ Ejemplo cotidiano: Cuando tienes fiebre, tu cuerpo usa las propiedades del agua para disipar el calor excesivo a través del sudor y la respiración.

Las sales minerales pueden estar precipitadas (sólidas e insolubles) o disueltas. Las precipitadas como el fosfato cálcico forman tus huesos y dientes. Las disueltas se separan en iones y realizan funciones vitales.
Los iones disueltos actúan como cofactores enzimáticos (ayudan a las enzimas a funcionar), generan gradientes electroquímicos (permiten que tus neuronas transmitan señales), regulan el equilibrio osmótico (controlan el agua celular), y actúan como tampones para mantener el pH estable.
La ósmosis es el movimiento de agua a través de membranas semipermeables desde zonas con menos sal hacia zonas con más sal, hasta equilibrarse. Tu cuerpo usa este principio constantemente para regular el agua celular.
Si tus células se ponen en agua destilada (hipotónica) explotan por entrada excesiva de agua (citólisis). En agua muy salada (hipertónica) se deshidratan y arrugan (crenación). Las plantas han desarrollado paredes celulares rígidas para resistir estos cambios.
🧂 Aplicación real: Por eso no puedes beber agua de mar - deshidrataría tus células. Y por eso las plantas se ven "tiesas" cuando tienen suficiente agua (turgencia).

Las membranas celulares actúan como porteros súper selectivos que controlan qué entra y sale de las células. Esto es fundamental para mantener el equilibrio interno.
En la difusión, tanto agua como solutos pasan libremente a través de membranas permeables, moviéndose desde zonas concentradas hacia zonas diluidas. Es como perfume extendiéndose por una habitación.
La ósmosis es más selectiva: solo pasa agua a través de membranas semipermeables, desde donde hay menos soluto hacia donde hay más. Es el mecanismo que las plantas usan para mantenerse erguidas.
La diálisis combina ambos: pasa agua y moléculas pequeñas (como sales) pero no las grandes (como proteínas). Los riñones artificiales usan este principio para "limpiar" la sangre de pacientes con insuficiencia renal.
🏥 Conexión médica: Los sueros intravenosos están cuidadosamente preparados para ser isotónicos con tu sangre - ni muy salados ni muy diluidos, para no dañar tus glóbulos rojos.
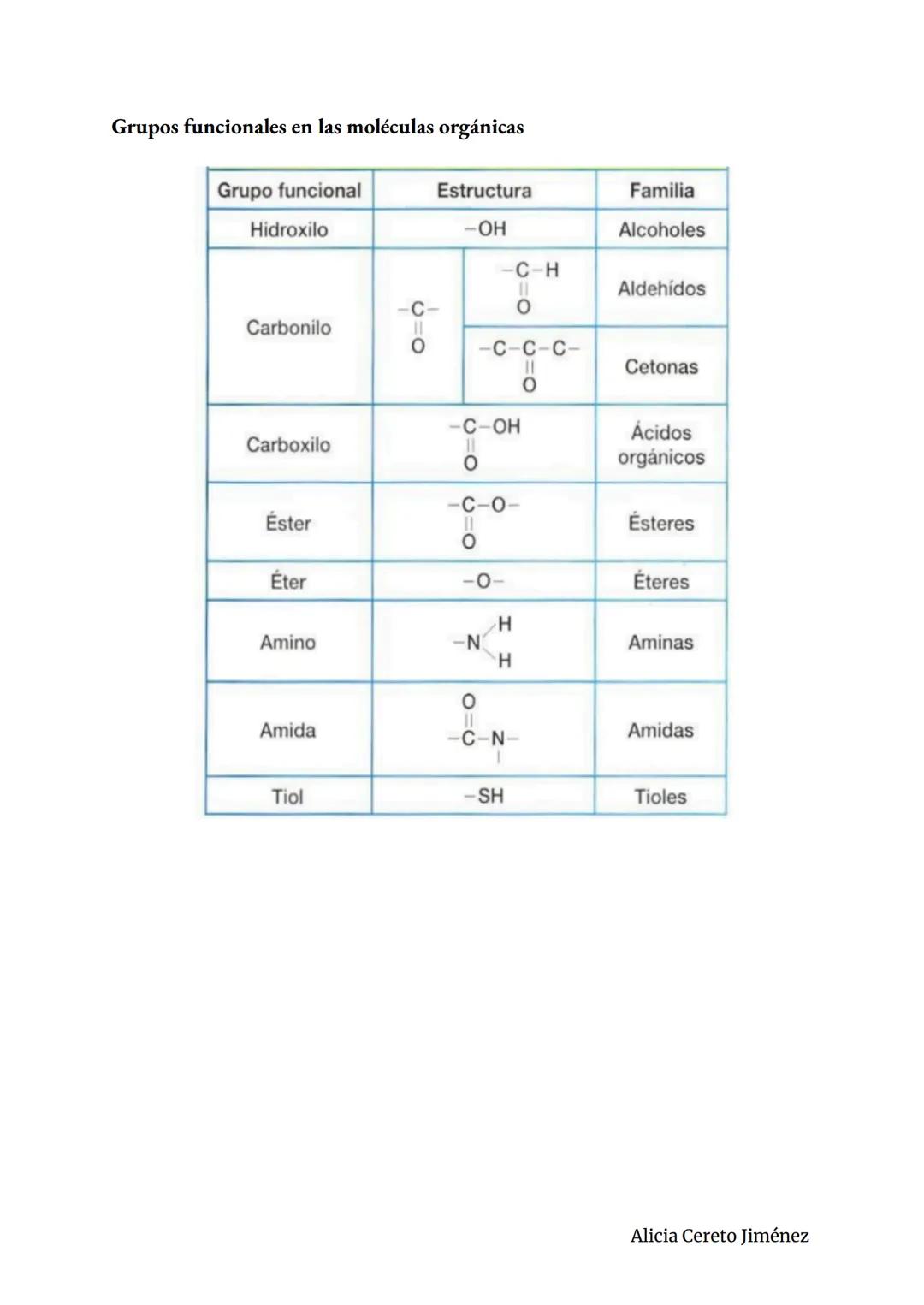
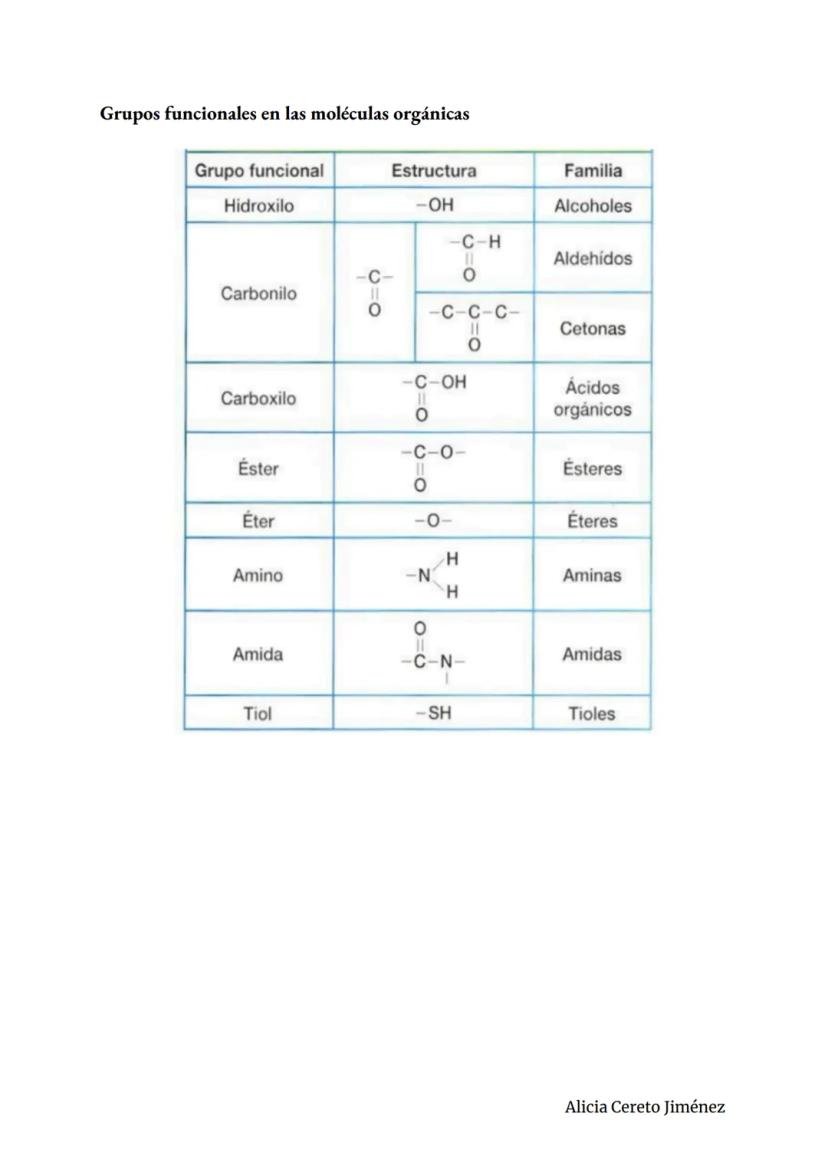
Los grupos funcionales son como "herramientas químicas" que se conectan a cadenas de carbono para darles propiedades específicas. Son los que determinan cómo se comporta cada molécula.
El grupo hidroxilo forma alcoholes y hace que las moléculas sean solubles en agua. Los grupos carbonilo forman aldehídos y cetonas, importantes en azúcares y metabolismo energético.
El grupo carboxilo hace que las moléculas sean ácidas - lo encuentras en aminoácidos y ácidos grasos. El grupo amino es básico y forma parte de proteínas y ácidos nucleicos.
Los grupos éster y éter conectan moléculas grandes, mientras que el grupo tiol forma enlaces de azufre cruciales para la estructura de proteínas. Cada uno tiene su "personalidad química" específica.
🧬 Pensamiento clave: Memorizar estos grupos te ayudará a entender cómo funcionan los carbohidratos, lípidos, proteínas y ácidos nucleicos que estudiarás próximamente.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
Alicia Cereto Jiménez
@aliciaceretojim
¿Sabías que tu cuerpo es básicamente una fábrica química súper avanzada? Todo lo que eres - desde tus músculos hasta tu ADN - está hecho de átomos que se conectan de formas específicas. Vamos a descubrir cómo funcionan estos "pegamentos"... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La vida tal como la conoces está construida con átomos que se unen como piezas de LEGO para formar estructuras más complejas. Estos átomos no se juntan al azar - siguen reglas químicas específicas que determinan cómo funciona todo en tu cuerpo.
Los enlaces químicos son como diferentes tipos de pegamento: algunos son súper fuertes y mantienen unidas las moléculas por dentro, mientras que otros son más débiles pero permiten que las moléculas interactúen entre ellas. Esta diferencia es clave para entender cómo funciona la biología.
💡 Piénsalo así: Los enlaces fuertes son como los clavos que mantienen una casa en pie, los débiles son como el velcro que te permite abrir y cerrar tu mochila fácilmente.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Estos son los enlaces que mantienen unidos los átomos dentro de cada molécula. Son como matrimonios químicos: duraderos y estables.
El enlace covalente es el más común en biología. Aquí los átomos "comparten" electrones como roommates compartiendo gastos. Puede ser polar (uno atrae más los electrones) o apolar (comparten por igual). Moléculas como el agua (H₂O) son polares - por eso el agua tiene propiedades tan especiales.
El enlace iónico es diferente: un átomo le "regala" electrones a otro. Uno se vuelve positivo (catión) y otro negativo (anión), y se atraen como imanes opuestos. Esto forma cristales ordenados como la sal de mesa (NaCl).
🧪 Dato curioso: La diferencia entre estos enlaces explica por qué el aceite y el agua no se mezclan, pero la sal sí se disuelve en agua.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Estos enlaces débiles son los verdaderos héroes de la biología. Permiten que las moléculas interactúen, se separen y vuelvan a unirse - exactamente lo que necesitas para procesos como la digestión o la respiración.
Las fuerzas electrostáticas atraen cargas opuestas, como cuando un enzima se une temporalmente a su sustrato. Las fuerzas de solvatación explican por qué la sal se disuelve en agua - cada ion se rodea de moléculas de agua como fans rodeando a una estrella.
Las interacciones hidrofóbicas son fascinantes: las moléculas que "odian" el agua se juntan entre ellas para evitarla. Esto forma las membranas de tus células. Las fuerzas de Van der Waals son súper débiles individualmente, pero juntas son poderosas - como una multitud de hormigas moviendo algo pesado.
Los enlaces de hidrógeno son especiales: determinan por qué el agua es líquida a temperatura ambiente y por qué el ADN tiene su forma característica.
🔬 Aplicación práctica: Estos enlaces débiles explican cómo funcionan los jabones, por qué sudas para refrescarte, y cómo las proteínas cambian de forma.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
No todos los elementos químicos son igual de importantes para la vida. Hay una "lista VIP" de elementos que tu cuerpo usa constantemente.
Los bioelementos primarios (C, H, O, N, P, S) forman el 98% de tu peso corporal. Son como los ingredientes principales de una receta - sin ellos no hay vida posible. El carbono es la estrella: puede formar cuatro enlaces y crear cadenas largas y complejas.
Los bioelementos secundarios (Ca, Mg, Na, K, Cl) son el 2% restante pero súper importantes. El calcio endurece tus huesos, el sodio y potasio hacen que tus neuronas funcionen, y el magnesio es parte de la clorofila de las plantas.
Los oligoelementos aparecen en cantidades mínimas pero son esenciales. El hierro transporta oxígeno en tu sangre, el zinc fortalece tu sistema inmune, y el cobre ayuda en la producción de energía.
⚡ Dato impactante: Aunque el hierro representa menos del 0.01% de tu peso, sin él te asfixiarías porque no podrías transportar oxígeno.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El carbono es el elemento perfecto para formar la base de la vida. Puede crear cuatro enlaces súper estables, formar cadenas largas, anillos y estructuras 3D complejas. Además, abunda en la Tierra y se une igual de bien al oxígeno y al hidrógeno.
Las biomoléculas se dividen en dos grupos principales. Las inorgánicas (agua y sales minerales) también están en la materia no viva. Las orgánicas (glúcidos, lípidos, proteínas y ácidos nucleicos) son exclusivas de los seres vivos y todas tienen esqueletos de carbono.
El agua es la molécula más abundante de tu cuerpo - ¡representas un 75% de agua! Aparece como agua estructural (parte de las células), circulante (transporta nutrientes), y metabólica (forma parte de moléculas y no se puede perder).
La estructura del agua es simple pero genial: un oxígeno conectado a dos hidrógenos. Como el oxígeno atrae más los electrones, la molécula se comporta como un imán pequeño (dipolo), lo que le da propiedades únicas.
💧 Conexión personal: Literalmente eres más agua que cualquier otra cosa. Tu cerebro es 80% agua y tus músculos 75%.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El agua líquida forma una red flexible de moléculas unidas por puentes de hidrógeno que se reorganizan constantemente. Esto le da propiedades increíbles que hacen posible la vida.
Como disolvente universal, el agua puede disolver casi todo lo que tu cuerpo necesita transportar. Su alta cohesión (las moléculas se "pegan" entre sí) y adhesión (se pega a otras superficies) permite que las plantas suban agua desde las raíces hasta las hojas.
Su función termorreguladora es clave: puede absorber muchísimo calor sin cambiar mucho de temperatura, actuando como un termostato natural. Por eso no te sobrecalientas fácilmente y el sudor te refresca tan eficazmente.
El agua también actúa como esqueleto hidrostático (da firmeza a las células), lubricante (reduce rozamiento entre tejidos), y medio de reacción para todos los procesos metabólicos. Su densidad menor en estado sólido permite que los peces sobrevivan bajo el hielo en invierno.
🌡️ Ejemplo cotidiano: Cuando tienes fiebre, tu cuerpo usa las propiedades del agua para disipar el calor excesivo a través del sudor y la respiración.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las sales minerales pueden estar precipitadas (sólidas e insolubles) o disueltas. Las precipitadas como el fosfato cálcico forman tus huesos y dientes. Las disueltas se separan en iones y realizan funciones vitales.
Los iones disueltos actúan como cofactores enzimáticos (ayudan a las enzimas a funcionar), generan gradientes electroquímicos (permiten que tus neuronas transmitan señales), regulan el equilibrio osmótico (controlan el agua celular), y actúan como tampones para mantener el pH estable.
La ósmosis es el movimiento de agua a través de membranas semipermeables desde zonas con menos sal hacia zonas con más sal, hasta equilibrarse. Tu cuerpo usa este principio constantemente para regular el agua celular.
Si tus células se ponen en agua destilada (hipotónica) explotan por entrada excesiva de agua (citólisis). En agua muy salada (hipertónica) se deshidratan y arrugan (crenación). Las plantas han desarrollado paredes celulares rígidas para resistir estos cambios.
🧂 Aplicación real: Por eso no puedes beber agua de mar - deshidrataría tus células. Y por eso las plantas se ven "tiesas" cuando tienen suficiente agua (turgencia).

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las membranas celulares actúan como porteros súper selectivos que controlan qué entra y sale de las células. Esto es fundamental para mantener el equilibrio interno.
En la difusión, tanto agua como solutos pasan libremente a través de membranas permeables, moviéndose desde zonas concentradas hacia zonas diluidas. Es como perfume extendiéndose por una habitación.
La ósmosis es más selectiva: solo pasa agua a través de membranas semipermeables, desde donde hay menos soluto hacia donde hay más. Es el mecanismo que las plantas usan para mantenerse erguidas.
La diálisis combina ambos: pasa agua y moléculas pequeñas (como sales) pero no las grandes (como proteínas). Los riñones artificiales usan este principio para "limpiar" la sangre de pacientes con insuficiencia renal.
🏥 Conexión médica: Los sueros intravenosos están cuidadosamente preparados para ser isotónicos con tu sangre - ni muy salados ni muy diluidos, para no dañar tus glóbulos rojos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los grupos funcionales son como "herramientas químicas" que se conectan a cadenas de carbono para darles propiedades específicas. Son los que determinan cómo se comporta cada molécula.
El grupo hidroxilo forma alcoholes y hace que las moléculas sean solubles en agua. Los grupos carbonilo forman aldehídos y cetonas, importantes en azúcares y metabolismo energético.
El grupo carboxilo hace que las moléculas sean ácidas - lo encuentras en aminoácidos y ácidos grasos. El grupo amino es básico y forma parte de proteínas y ácidos nucleicos.
Los grupos éster y éter conectan moléculas grandes, mientras que el grupo tiol forma enlaces de azufre cruciales para la estructura de proteínas. Cada uno tiene su "personalidad química" específica.
🧬 Pensamiento clave: Memorizar estos grupos te ayudará a entender cómo funcionan los carbohidratos, lípidos, proteínas y ácidos nucleicos que estudiarás próximamente.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
16
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS