Los bioelementos y biomoléculas son los componentes químicos fundamentales de... Mostrar más
Introducció a la Bioquímica: Glúcids per al Batxillerat










Bioelementos
Los bioelementos son los elementos químicos que forman parte de los seres vivos y que constituyen las biomoléculas necesarias para desarrollar los procesos vitales. No son exclusivos de los seres vivos, pues también pueden encontrarse en la materia inerte.
Los bioelementos se clasifican según su abundancia e importancia en:
- Bioelementos primarios: Son indispensables para formar biomoléculas orgánicas y constituyen el 96,2% de la materia viva. Sin ellos, no puede haber vida.
💡 Un elemento químico se considera bioelemento cuando se utiliza para dar vida. Si no cumple esta función, simplemente es un elemento químico.

Bioelementos primarios
Existen 6 bioelementos primarios, cada uno con funciones específicas:
-
Oxígeno (O): Forma grupos funcionales polares solubles en agua como -OH, -CHO, -COOH y puede formar enlaces α-glicosídicos entre biomoléculas.
-
Carbono e hidrógeno (C, H): Forman los esqueletos carbohidrogenados de las moléculas, permitiendo una gran diversidad molecular.
-
Nitrógeno (N): Presente en proteínas y ácidos nucleicos. Forma el grupo amino de los aminoácidos.
-
Fósforo (P): Presente en los ácidos nucleicos, concretamente en el grupo fosfato de los nucleótidos.
-
Azufre (S): Se encuentra en proteínas, específicamente en los aminoácidos metionina y cisteína.
Bioelementos secundarios: Aunque frecuentes, tienen menor importancia que los primarios. Constituyen el 3,9% de la materia viva y participan en muchos procesos biológicos.

Bioelementos secundarios y oligoelementos
Los 5 bioelementos secundarios incluyen:
- Calcio (Ca): Componente estructural de huesos, aportando volumen y resistencia.
- Sodio (Na): Mantiene el equilibrio hídrico y regula la cantidad de agua dentro y fuera de la célula.
- Potasio (K): Facilita la transmisión de señales nerviosas y la contracción muscular.
- Cloro (Cl): Interviene en el equilibrio de líquidos corporales y regula la presión osmótica.
- Magnesio (Mg): Forma parte de enzimas y de la clorofila, participando en reacciones como la replicación del ADN.
Oligoelementos: Elementos con presencia inferior al 0,4%, pero igualmente importantes:
- Hierro (Fe): Encargado de fabricar hemoglobina y transportar oxígeno.
- Cobre (Cu): Produce mioglobina en la sangre de invertebrados.
- Flúor (F): Presente en los dientes.

Biomoléculas
Las biomoléculas o principios inmediatos pueden clasificarse según su composición:
Simples: Formadas por átomos del mismo tipo (como el oxígeno). Compuestas: Formadas por átomos de diferentes elementos (como el agua).
Las biomoléculas compuestas se clasifican en:
Inorgánicas: Presentes tanto en materia viva como inerte
- Agua
- Sales minerales
- Dióxido de carbono
Orgánicas: Exclusivas de la materia viva
- Glúcidos
- Lípidos
- Proteínas
- Ácidos nucleicos
💡 Algunos elementos indispensables para el organismo no son bioelementos primarios porque no tienen la misma abundancia que los que forman las biomoléculas orgánicas, pero siguen siendo fundamentales para la vida.

Enlaces químicos
Los enlaces químicos pueden ser intramoleculares (fuertes y estables) o intermoleculares (débiles y dinámicos).
Enlaces intramoleculares:
- Enlace iónico: Se forma por la atracción entre un catión (+) y un anión (-).
- Se produce entre un metal y un no metal
- Los metales, poco electronegativos, pierden electrones formando cationes
- Los no metales, muy electronegativos, ganan electrones formando aniones
- Implica transferencia de electrones
- Tiene alto punto de fusión
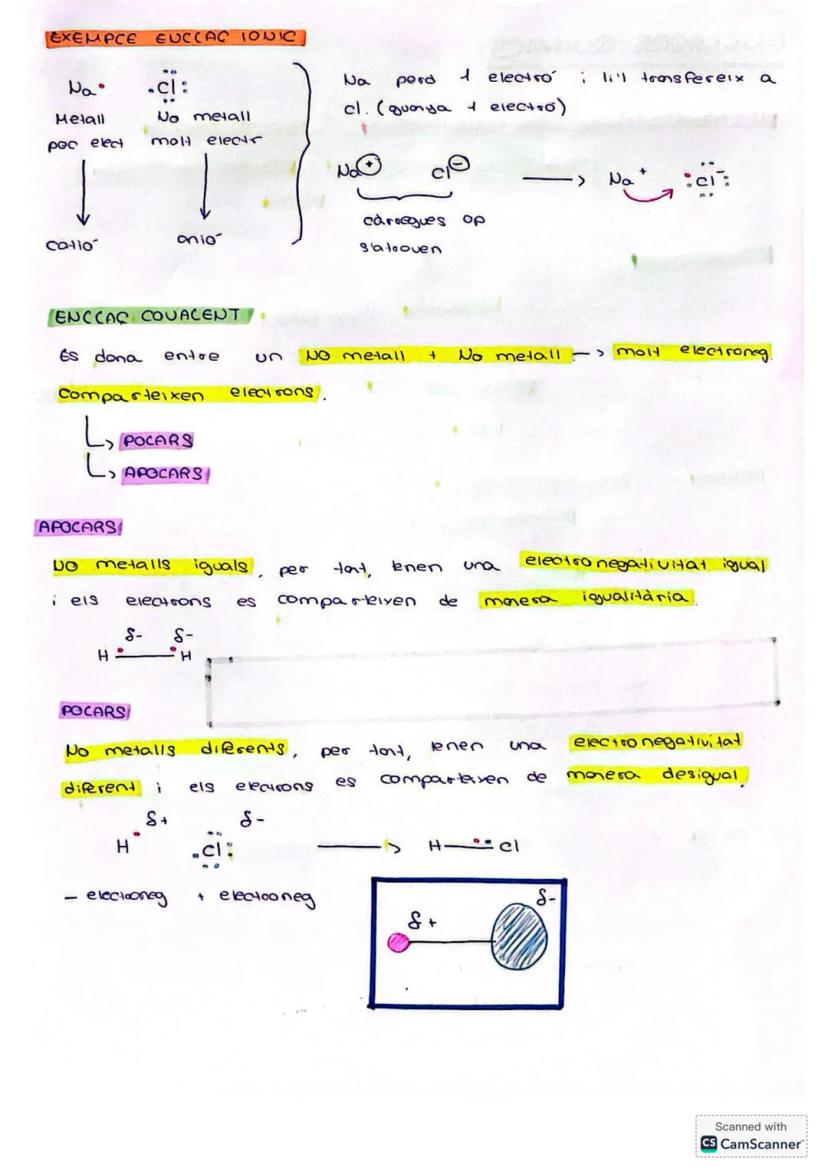
Ejemplo de enlace iónico: Na (metal poco electronegativo) + Cl (no metal muy electronegativo) → Na⁺ + Cl⁻ → NaCl
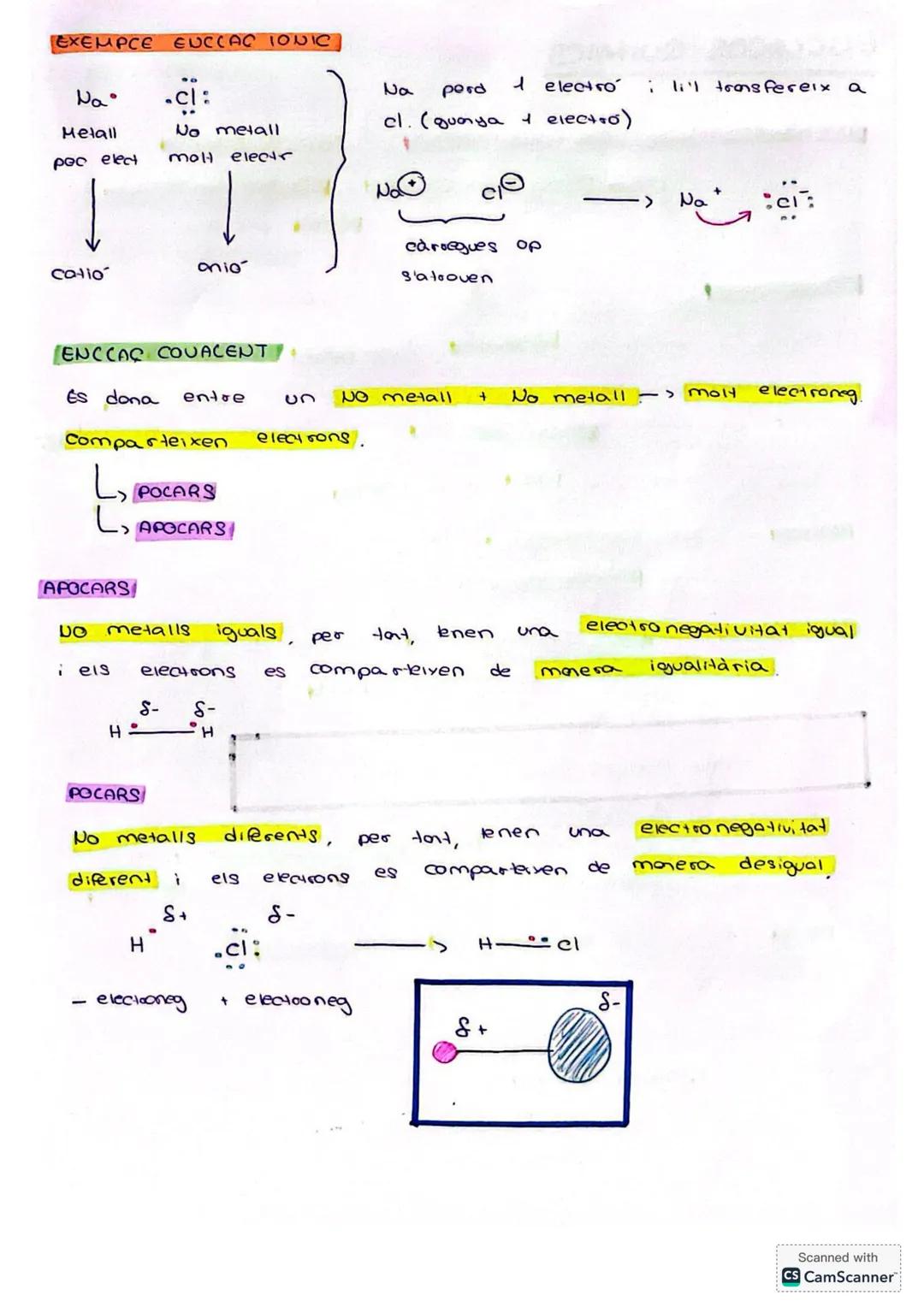
Enlace covalente
Enlace covalente: Se forma entre no metales que comparten electrones. Puede ser:
-
Apolar: Entre no metales iguales con electronegatividad idéntica, donde los electrones se comparten equitativamente.
Ejemplo: H-H
-
Polar: Entre no metales diferentes con electronegatividad distinta, donde los electrones se comparten desigualmente.
Ejemplo: H-Cl (el Cl es más electronegativo que el H)
Este tipo de enlace es fundamental en la estructura de las biomoléculas orgánicas, permitiendo la formación de las complejas cadenas de carbono que caracterizan a los seres vivos.

Enlaces químicos intermoleculares
Los enlaces intermoleculares son débiles y dinámicos, pero fundamentales para la estructura tridimensional de las biomoléculas. Existen cuatro tipos:
-
Puentes de hidrógeno: Se forman entre moléculas con enlaces covalentes polares. Son débiles y pueden romperse con facilidad, pero su número los hace importantes.
-
Fuerzas de Van der Waals: Se dan entre moléculas con enlaces covalentes polares o apolares. Permiten los estados líquido y sólido del agua.
-
Interacciones hidrofóbicas: Se producen entre moléculas con enlaces covalentes apolares.
-
Fuerzas de solvatación: Se forman entre agua y moléculas con enlaces iónicos .
Estos enlaces, aunque individualmente débiles, son cruciales para mantener la estructura tridimensional de proteínas, ácidos nucleicos y otras biomoléculas complejas.

El agua
El agua es la sustancia química más abundante en los seres vivos (75%) y se encuentra en tres formas:
- Agua circulante: La que está en la sangre o la savia
- Agua intersticial: La que se encuentra entre células
- Agua intracelular: La que está en el citosol y dentro de los orgánulos celulares
La molécula de agua es polar y tiene carga, lo que le confiere propiedades únicas.
Características fundamentales del agua:
- Elevado grado de cohesión entre moléculas: Debido a los puentes de hidrógeno, el agua es un líquido incompresible ideal para dar volumen a las células, provocar turgencia en plantas y servir de esqueleto hidrostático en invertebrados.
💡 Las características especiales del agua la convierten en una molécula indispensable para la vida, funcionando como disolvente universal, regulador térmico y componente estructural.

Propiedades del agua
-
Elevada fuerza de adhesión: Las moléculas de agua tienden a adherirse a moléculas cargadas en la superficie de un tubo, permitiendo fenómenos de capilaridad como el ascenso de la savia bruta por los vasos del xilema.
-
Elevado calor específico: Se necesita mucha energía para aumentar su temperatura, ya que hay que romper los puentes de hidrógeno. Esto permite que actúe como amortiguador térmico que evita cambios bruscos de temperatura.
-
Elevado calor de vaporización: Se requiere mucha energía para que el agua pase a estado gaseoso, lo que permite la refrigeración del organismo mediante la evaporación.
-
Elevada constante dieléctrica o disolvente universal: Su polaridad le permite disolver compuestos iónicos como las sales minerales, que se disocian en cationes y aniones rodeados por moléculas de agua.

Más propiedades del agua
El agua también disuelve compuestos covalentes polares que contienen grupos ionizados, convirtiéndola en excelente vehículo de transporte de sustancias y para las reacciones bioquímicas.
-
Elevada tensión superficial: Es la fuerza que opone el líquido para que se rompa su superficie. Permite deformaciones del citoplasma celular y los movimientos internos de la célula.
-
Baja densidad en estado sólido: El agua puede estar en los tres estados físicos. En zonas frías, esto permite la vida marina, ya que el hielo flota y forma capas en la superficie, mientras que debajo el agua permanece líquida, permitiendo la supervivencia de las especies.
-
Bajo grado de ionización: El agua es difícil de disociar en moléculas de hidróxido negativas.
💡 La extraordinaria propiedad de que el agua sólida (hielo) sea menos densa que el agua líquida ha permitido la evolución de la vida acuática en zonas frías.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: Monosacárido
9LOS GLÚCIDOS
Apuntes de los glucidos biología 2bach
TEMA 2 GLÚCIDOS
tema glúcidos de 2bach para la EBAU
Apuntes de Biología para Ebau
Tema 1: Base molecular de la vida Tema 2: Glúcidos y lípidos Fuente: García López, M. (2016). Biología 2 bachillerato. Eldevives
Glúcidos y lípidos
Tema 2: Glúcidos y lípidos
TEMA 2 BIOLOGÍA. LOS GLÚCIDOS.
En estos apuntes hay imágenes y todo lo necesario para aprobar el examen. Contenido de 2º de bachillerato.
Tema 2 glúcidos
El grupo hidroxilo de un carbono distinto del más alejado del grupo funcional crea epímeros y ciclos en monosacáridos.
Preguntas tipo EBAU Biología - Glúcidos
Recopilación de preguntas del tema de biología "Glúcidos", que han aparecido otros años en la EBAU.
apuntes tema 1 glúcidos biología
apuntes de biología del tema 1 de glúcido
Resumen de glúcidos
Monosacáridos, monosacáridos de interés, propiedades. disacáridos, polisacáridos...
Contenidos más populares de Biología
9Replicación, transcripción y traducción
Esquema del tema de flujo de información genética del bloque de Biología Molecular
Fotosíntesis
Conceptos básicos y reacciones químicas que se producen
Descubriendo la vida: Flashcards de Biología
Aprende sobre los fundamentos de la biología con esta colección de flashcards interactivos. ¡Explora los conceptos clave y amplía tus conocimientos sobre la vida en este emocionante viaje de aprendizaje!
GENÉTICA MOLECULAR
Genética molecular 2 bachillerato y PAU
Catabolismo y anabolismo
Apuntes “esquematizados” con imágenes y visual
Anabolismo y Catabolismo
amabolismo y catabolismo
Metabolismo
Apuntes de metabolismo de segundo de bachillerato (biología). También recomiendo acompañar el estudio de este tema con el esquema que he subido para entenderlo mejor.
METABOLISMO CELULAR (CATABOLISMO + ANABOLISMO)
Apuntes completos de catabolismo y anabolismo de 2 bach
las plantas 🌳🌿
el reino de las plantas
Contenidos más populares
9Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
QUIZZ VIDA DIARIA#1
QUIZZ sobre tu vida diaria, psicológico para mejorar el estudio.:] [ Cualquier pregunta, la responderé ]^^
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Introducció a la Bioquímica: Glúcids per al Batxillerat
Los bioelementos y biomoléculas son los componentes químicos fundamentales de todos los seres vivos. Aunque comparten los mismos elementos que encontramos en la materia inerte, su proporción y organización es lo que permite el desarrollo de la vida. En este... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Bioelementos
Los bioelementos son los elementos químicos que forman parte de los seres vivos y que constituyen las biomoléculas necesarias para desarrollar los procesos vitales. No son exclusivos de los seres vivos, pues también pueden encontrarse en la materia inerte.
Los bioelementos se clasifican según su abundancia e importancia en:
- Bioelementos primarios: Son indispensables para formar biomoléculas orgánicas y constituyen el 96,2% de la materia viva. Sin ellos, no puede haber vida.
💡 Un elemento químico se considera bioelemento cuando se utiliza para dar vida. Si no cumple esta función, simplemente es un elemento químico.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Bioelementos primarios
Existen 6 bioelementos primarios, cada uno con funciones específicas:
-
Oxígeno (O): Forma grupos funcionales polares solubles en agua como -OH, -CHO, -COOH y puede formar enlaces α-glicosídicos entre biomoléculas.
-
Carbono e hidrógeno (C, H): Forman los esqueletos carbohidrogenados de las moléculas, permitiendo una gran diversidad molecular.
-
Nitrógeno (N): Presente en proteínas y ácidos nucleicos. Forma el grupo amino de los aminoácidos.
-
Fósforo (P): Presente en los ácidos nucleicos, concretamente en el grupo fosfato de los nucleótidos.
-
Azufre (S): Se encuentra en proteínas, específicamente en los aminoácidos metionina y cisteína.
Bioelementos secundarios: Aunque frecuentes, tienen menor importancia que los primarios. Constituyen el 3,9% de la materia viva y participan en muchos procesos biológicos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Bioelementos secundarios y oligoelementos
Los 5 bioelementos secundarios incluyen:
- Calcio (Ca): Componente estructural de huesos, aportando volumen y resistencia.
- Sodio (Na): Mantiene el equilibrio hídrico y regula la cantidad de agua dentro y fuera de la célula.
- Potasio (K): Facilita la transmisión de señales nerviosas y la contracción muscular.
- Cloro (Cl): Interviene en el equilibrio de líquidos corporales y regula la presión osmótica.
- Magnesio (Mg): Forma parte de enzimas y de la clorofila, participando en reacciones como la replicación del ADN.
Oligoelementos: Elementos con presencia inferior al 0,4%, pero igualmente importantes:
- Hierro (Fe): Encargado de fabricar hemoglobina y transportar oxígeno.
- Cobre (Cu): Produce mioglobina en la sangre de invertebrados.
- Flúor (F): Presente en los dientes.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Biomoléculas
Las biomoléculas o principios inmediatos pueden clasificarse según su composición:
Simples: Formadas por átomos del mismo tipo (como el oxígeno). Compuestas: Formadas por átomos de diferentes elementos (como el agua).
Las biomoléculas compuestas se clasifican en:
Inorgánicas: Presentes tanto en materia viva como inerte
- Agua
- Sales minerales
- Dióxido de carbono
Orgánicas: Exclusivas de la materia viva
- Glúcidos
- Lípidos
- Proteínas
- Ácidos nucleicos
💡 Algunos elementos indispensables para el organismo no son bioelementos primarios porque no tienen la misma abundancia que los que forman las biomoléculas orgánicas, pero siguen siendo fundamentales para la vida.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces químicos
Los enlaces químicos pueden ser intramoleculares (fuertes y estables) o intermoleculares (débiles y dinámicos).
Enlaces intramoleculares:
- Enlace iónico: Se forma por la atracción entre un catión (+) y un anión (-).
- Se produce entre un metal y un no metal
- Los metales, poco electronegativos, pierden electrones formando cationes
- Los no metales, muy electronegativos, ganan electrones formando aniones
- Implica transferencia de electrones
- Tiene alto punto de fusión
Ejemplo de enlace iónico: Na (metal poco electronegativo) + Cl (no metal muy electronegativo) → Na⁺ + Cl⁻ → NaCl

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace covalente
Enlace covalente: Se forma entre no metales que comparten electrones. Puede ser:
-
Apolar: Entre no metales iguales con electronegatividad idéntica, donde los electrones se comparten equitativamente.
Ejemplo: H-H
-
Polar: Entre no metales diferentes con electronegatividad distinta, donde los electrones se comparten desigualmente.
Ejemplo: H-Cl (el Cl es más electronegativo que el H)
Este tipo de enlace es fundamental en la estructura de las biomoléculas orgánicas, permitiendo la formación de las complejas cadenas de carbono que caracterizan a los seres vivos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces químicos intermoleculares
Los enlaces intermoleculares son débiles y dinámicos, pero fundamentales para la estructura tridimensional de las biomoléculas. Existen cuatro tipos:
-
Puentes de hidrógeno: Se forman entre moléculas con enlaces covalentes polares. Son débiles y pueden romperse con facilidad, pero su número los hace importantes.
-
Fuerzas de Van der Waals: Se dan entre moléculas con enlaces covalentes polares o apolares. Permiten los estados líquido y sólido del agua.
-
Interacciones hidrofóbicas: Se producen entre moléculas con enlaces covalentes apolares.
-
Fuerzas de solvatación: Se forman entre agua y moléculas con enlaces iónicos .
Estos enlaces, aunque individualmente débiles, son cruciales para mantener la estructura tridimensional de proteínas, ácidos nucleicos y otras biomoléculas complejas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El agua
El agua es la sustancia química más abundante en los seres vivos (75%) y se encuentra en tres formas:
- Agua circulante: La que está en la sangre o la savia
- Agua intersticial: La que se encuentra entre células
- Agua intracelular: La que está en el citosol y dentro de los orgánulos celulares
La molécula de agua es polar y tiene carga, lo que le confiere propiedades únicas.
Características fundamentales del agua:
- Elevado grado de cohesión entre moléculas: Debido a los puentes de hidrógeno, el agua es un líquido incompresible ideal para dar volumen a las células, provocar turgencia en plantas y servir de esqueleto hidrostático en invertebrados.
💡 Las características especiales del agua la convierten en una molécula indispensable para la vida, funcionando como disolvente universal, regulador térmico y componente estructural.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades del agua
-
Elevada fuerza de adhesión: Las moléculas de agua tienden a adherirse a moléculas cargadas en la superficie de un tubo, permitiendo fenómenos de capilaridad como el ascenso de la savia bruta por los vasos del xilema.
-
Elevado calor específico: Se necesita mucha energía para aumentar su temperatura, ya que hay que romper los puentes de hidrógeno. Esto permite que actúe como amortiguador térmico que evita cambios bruscos de temperatura.
-
Elevado calor de vaporización: Se requiere mucha energía para que el agua pase a estado gaseoso, lo que permite la refrigeración del organismo mediante la evaporación.
-
Elevada constante dieléctrica o disolvente universal: Su polaridad le permite disolver compuestos iónicos como las sales minerales, que se disocian en cationes y aniones rodeados por moléculas de agua.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Más propiedades del agua
El agua también disuelve compuestos covalentes polares que contienen grupos ionizados, convirtiéndola en excelente vehículo de transporte de sustancias y para las reacciones bioquímicas.
-
Elevada tensión superficial: Es la fuerza que opone el líquido para que se rompa su superficie. Permite deformaciones del citoplasma celular y los movimientos internos de la célula.
-
Baja densidad en estado sólido: El agua puede estar en los tres estados físicos. En zonas frías, esto permite la vida marina, ya que el hielo flota y forma capas en la superficie, mientras que debajo el agua permanece líquida, permitiendo la supervivencia de las especies.
-
Bajo grado de ionización: El agua es difícil de disociar en moléculas de hidróxido negativas.
💡 La extraordinaria propiedad de que el agua sólida (hielo) sea menos densa que el agua líquida ha permitido la evolución de la vida acuática en zonas frías.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: Monosacárido
9LOS GLÚCIDOS
Apuntes de los glucidos biología 2bach
TEMA 2 GLÚCIDOS
tema glúcidos de 2bach para la EBAU
Apuntes de Biología para Ebau
Tema 1: Base molecular de la vida Tema 2: Glúcidos y lípidos Fuente: García López, M. (2016). Biología 2 bachillerato. Eldevives
Glúcidos y lípidos
Tema 2: Glúcidos y lípidos
TEMA 2 BIOLOGÍA. LOS GLÚCIDOS.
En estos apuntes hay imágenes y todo lo necesario para aprobar el examen. Contenido de 2º de bachillerato.
Tema 2 glúcidos
El grupo hidroxilo de un carbono distinto del más alejado del grupo funcional crea epímeros y ciclos en monosacáridos.
Preguntas tipo EBAU Biología - Glúcidos
Recopilación de preguntas del tema de biología "Glúcidos", que han aparecido otros años en la EBAU.
apuntes tema 1 glúcidos biología
apuntes de biología del tema 1 de glúcido
Resumen de glúcidos
Monosacáridos, monosacáridos de interés, propiedades. disacáridos, polisacáridos...
Contenidos más populares de Biología
9Replicación, transcripción y traducción
Esquema del tema de flujo de información genética del bloque de Biología Molecular
Fotosíntesis
Conceptos básicos y reacciones químicas que se producen
Descubriendo la vida: Flashcards de Biología
Aprende sobre los fundamentos de la biología con esta colección de flashcards interactivos. ¡Explora los conceptos clave y amplía tus conocimientos sobre la vida en este emocionante viaje de aprendizaje!
GENÉTICA MOLECULAR
Genética molecular 2 bachillerato y PAU
Catabolismo y anabolismo
Apuntes “esquematizados” con imágenes y visual
Anabolismo y Catabolismo
amabolismo y catabolismo
Metabolismo
Apuntes de metabolismo de segundo de bachillerato (biología). También recomiendo acompañar el estudio de este tema con el esquema que he subido para entenderlo mejor.
METABOLISMO CELULAR (CATABOLISMO + ANABOLISMO)
Apuntes completos de catabolismo y anabolismo de 2 bach
las plantas 🌳🌿
el reino de las plantas
Contenidos más populares
9Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
QUIZZ VIDA DIARIA#1
QUIZZ sobre tu vida diaria, psicológico para mejorar el estudio.:] [ Cualquier pregunta, la responderé ]^^
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.