Los seres vivos están formados por elementos químicos específicos que... Mostrar más
Biomoléculas - Apuntes 2º Bachillerato










Los Elementos de la Vida
¿Sabías que solo 6 elementos forman el 96% de tu cuerpo? Los bioelementos primarios (C, H, N, O, P, S) son literalmente los bloques de construcción de la vida. Estos elementos no están ahí por casualidad, sino porque tienen propiedades químicas perfectas para formar biomoléculas estables.
El carbono es el protagonista absoluto porque puede formar cadenas largas, ramificadas o cíclicas con facilidad. Imagínate como si fuera el "LEGO" de la química: puede conectarse de mil maneras diferentes creando estructuras complejas y variadas.
Los bioelementos secundarios (Na⁺, K⁺, Ca²⁺, Mg²⁺, Cl⁻) representan menos cantidad pero son igual de importantes. Sin ellos, tus músculos no se contraerían ni tus neuronas transmitirían impulsos.
¡Dato curioso! El 70% de tu peso corporal es agua, pero hay elementos que necesitas en cantidades microscópicas como el hierro de tu sangre o el zinc de tus enzimas.

La Arquitectura Molecular
El carbono es el arquitecto de las biomoléculas gracias a su estructura tetraédrica. Esta forma geométrica permite crear cadenas lineales, ramificadas, saturadas, insaturadas o incluso cíclicas. Es como tener un kit de construcción infinito.
Los grupos funcionales son como las herramientas especializadas de cada molécula. El grupo hidroxilo aparece en alcoholes, el carbonilo en aldehídos y cetonas, y el carboxilo en ácidos. Cada uno aporta propiedades químicas específicas.
Los bioelementos secundarios siempre aparecen ionizados en medio acuoso. Aunque solo representan una pequeña fracción, son imprescindibles para el funcionamiento celular.
Consejo de estudio: No memorices la tabla de grupos funcionales, solo entiende que cada grupo aporta características diferentes a las biomoléculas.

Biomoléculas y Enlaces
Las biomoléculas se dividen en dos grandes familias: inorgánicas (agua y sales minerales) y orgánicas (glúcidos, lípidos, proteínas y ácidos nucleicos). Cada grupo tiene funciones específicas pero todas trabajan juntas.
Los enlaces covalentes son los más fuertes y forman la estructura básica de las moléculas. Los monómeros (como aminoácidos o monosacáridos) se unen mediante estos enlaces para formar polímeros complejos.
El enlace de hidrógeno es más débil pero crucial para la estabilidad molecular. El agua es el ejemplo perfecto: sus moléculas se atraen entre sí creando propiedades únicas para la vida.
Recuerda: No necesitas describir cada enlace en detalle, pero sí reconocer su importancia en diferentes biomoléculas.

El Agua: La Molécula de la Vida
El agua representa aproximadamente el 70% del peso celular y es donde ocurren todas las reacciones metabólicas. Tu cuerpo literalmente está diseñado alrededor de las propiedades del agua.
Se distribuye como agua intracelular dentro de las células y agua extracelular (1/3) en sangre, linfa y entre tejidos. A mayor actividad metabólica, mayor proporción de agua necesitas.
La clave está en su estructura química: el oxígeno atrae más los electrones que el hidrógeno, creando una molécula dipolar. Esta polaridad es responsable de casi todas las propiedades extraordinarias del agua.
Dato interesante: Los organismos jóvenes tienen más agua que los adultos, y los órganos más activos (como el cerebro) contienen más agua que otros tejidos.

La Magia de la Polaridad
La polaridad del agua surge porque el oxígeno "roba" parcialmente los electrones del hidrógeno, creando zonas con carga parcial negativa (δ⁻) y positiva (δ⁺). Es como tener un imán molecular microscópico.
Esta estructura dipolar permite formar enlaces de hidrógeno entre moléculas de agua. Una molécula atrae a otras creando una red tridimensional que explica las propiedades únicas del agua.
Los enlaces de hidrógeno son relativamente débiles individualmente, pero juntos crean una fuerza colectiva impresionante. Es el principio de "la unión hace la fuerza" aplicado a nivel molecular.
Visualízalo: Imagina las moléculas de agua como pequeños imanes que se atraen entre sí, formando cadenas y redes que dan al agua sus propiedades especiales.

Propiedades Extraordinarias del Agua
La cohesividad mantiene unidas las moléculas de agua gracias a los puentes de hidrógeno. Esto hace que el agua sea prácticamente incompresible y capaz de dar volumen y turgencia a las células.
El elevado calor específico convierte al agua en un amortiguador térmico perfecto. Tu cuerpo puede mantener una temperatura estable incluso cuando el ambiente cambia bruscamente.
La elevada tensión superficial permite fenómenos como el ascenso de la savia por los árboles. Las moléculas de agua literalmente se "tiran" unas a otras hacia arriba.
Aplicación práctica: Cuando sudas, tu cuerpo aprovecha el elevado calor de vaporización del agua para enfriarse de manera muy eficiente.

El Agua como Disolvente Universal
El agua disuelve fácilmente compuestos iónicos como la sal y compuestos polares que pueden formar enlaces de hidrógeno con ella. A estos los llamamos hidrófilos (amigos del agua).
Los compuestos apolares como los aceites son hidrófobos (enemigos del agua) y no se disuelven. Pero existen moléculas anfipáticas que tienen ambas partes: una hidrófila y otra hidrófoba.
Las moléculas anfipáticas forman estructuras fascinantes: micelas (como las del jabón), monocapas en superficies, o bicapas lipídicas que forman las membranas celulares.
Conexión clave: Las membranas de tus células se forman gracias a esta propiedad anfipática de los fosfolípidos, creando barreras que separan el interior del exterior celular.

pH y Sales Minerales
El agua puede ionizarse formando iones H⁺ y OH⁻ en concentraciones muy bajas. Esta capacidad permite que actúe como regulador del pH, manteniendo la acidez cerca de la neutralidad (pH ≈ 7).
El pH se calcula como -log[H⁺] y es crucial para la vida. La mayoría de procesos biológicos necesitan un pH cercano a 7 para funcionar correctamente.
Las sales minerales aparecen de dos formas: insolubles (formando estructuras de sostén como huesos y caparazones) y solubles (disociadas en iones que participan en múltiples funciones celulares).
Ejemplo práctico: El calcio forma tus huesos cuando está insoluble, pero cuando está disuelto como Ca²⁺ permite la contracción de tus músculos.
Funciones de las Sales Minerales
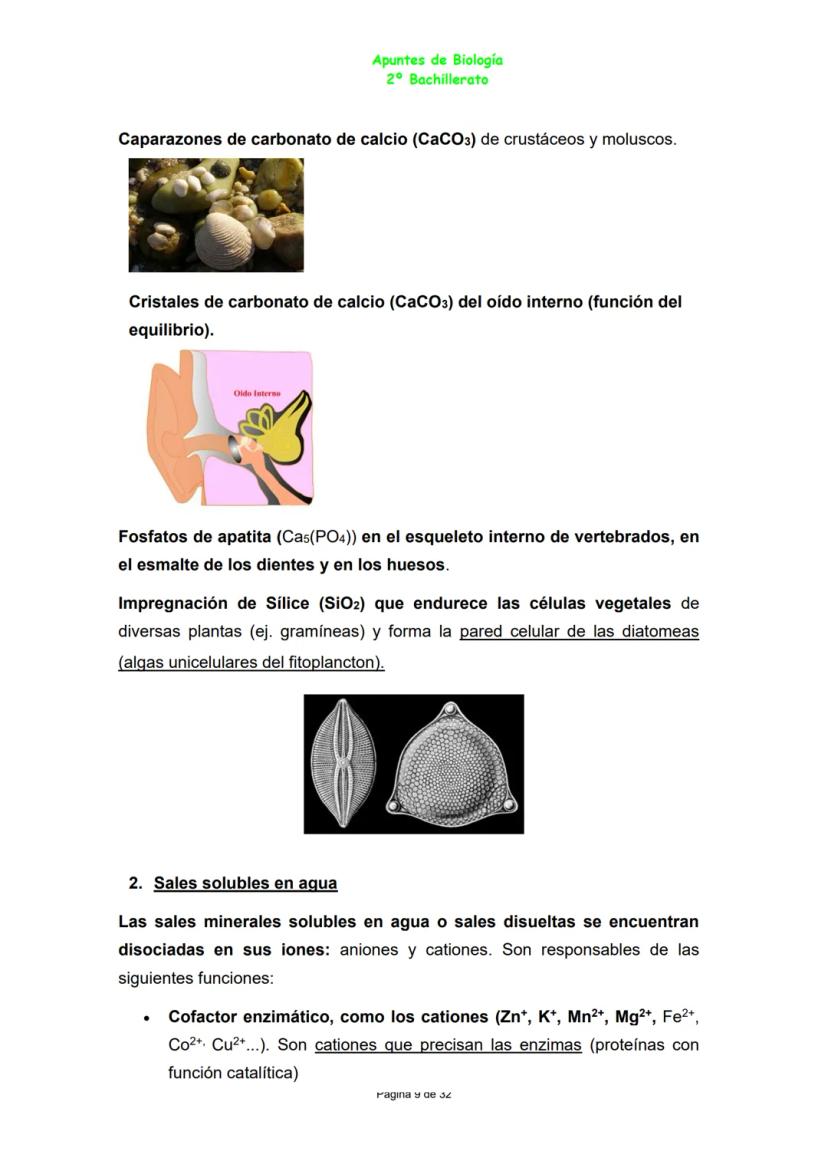
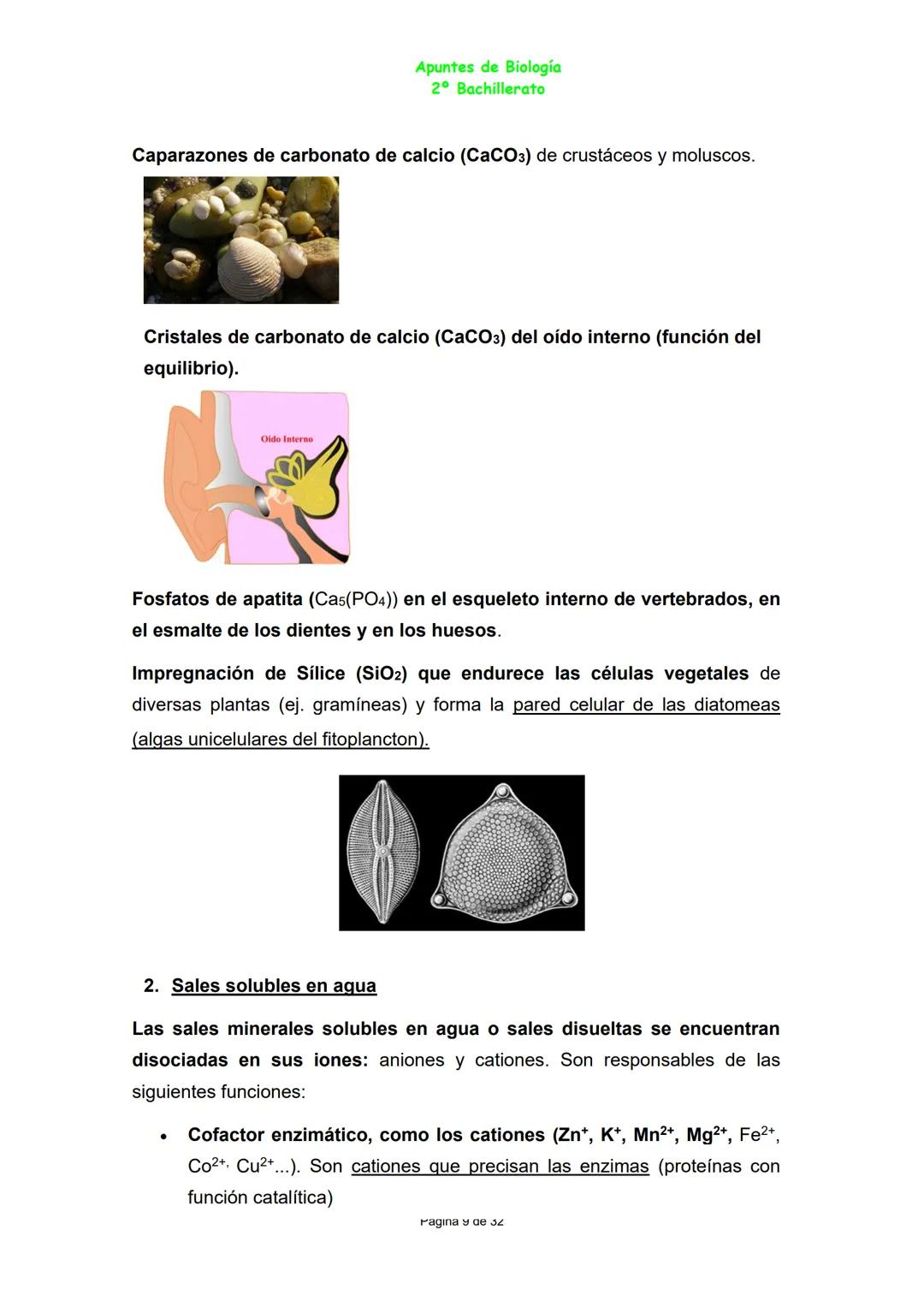
Las sales insolubles forman estructuras sólidas de protección y sostén. El carbonato de calcio crea caparazones resistentes, mientras que los fosfatos de apatita forman tus huesos y dientes.
La sílice endurece las paredes celulares vegetales, dándoles la rigidez necesaria para mantenerse erguidas. Cada mineral tiene su especialidad estructural.
Las sales solubles actúan como cofactores enzimáticos. Iones como Zn²⁺, K⁺, Mn²⁺ son indispensables para que las enzimas funcionen correctamente.
Dato clave: Los iones Na⁺ y K⁺ generan diferencias de carga eléctrica a ambos lados de las membranas, permitiendo la transmisión de impulsos nerviosos.

Introducción a los Glúcidos
Los glúcidos son biomoléculas orgánicas formadas por carbono, hidrógeno y oxígeno (C, H, O). Son fundamentales como fuente de energía y material estructural en los seres vivos.
Los monosacáridos son los glúcidos más sencillos y actúan como monómeros para formar estructuras más complejas. No se pueden hidrolizar (romper con agua) y contienen entre 3 y 7 átomos de carbono.
Químicamente son polihidroxialdehídos o polihidroxicetonas. Si tienen grupo aldehído son aldosas, si tienen grupo cetona son cetosas. Según el número de carbonos: triosas, tetrosas, pentosas o hexosas.
Ejemplos importantes: La D-glucosa es una aldohexosa y la D-fructosa es una cetohexosa .
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: macromoléculas
4Contenidos más populares de Biología
9Contenidos más populares
9¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Biomoléculas - Apuntes 2º Bachillerato
Los seres vivos están formados por elementos químicos específicos que se combinan de maneras increíbles para crear la vida tal y como la conocemos. Desde el carbono que forma nuestro ADN hasta el agua que permite todas nuestras funciones vitales,... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Los Elementos de la Vida
¿Sabías que solo 6 elementos forman el 96% de tu cuerpo? Los bioelementos primarios (C, H, N, O, P, S) son literalmente los bloques de construcción de la vida. Estos elementos no están ahí por casualidad, sino porque tienen propiedades químicas perfectas para formar biomoléculas estables.
El carbono es el protagonista absoluto porque puede formar cadenas largas, ramificadas o cíclicas con facilidad. Imagínate como si fuera el "LEGO" de la química: puede conectarse de mil maneras diferentes creando estructuras complejas y variadas.
Los bioelementos secundarios (Na⁺, K⁺, Ca²⁺, Mg²⁺, Cl⁻) representan menos cantidad pero son igual de importantes. Sin ellos, tus músculos no se contraerían ni tus neuronas transmitirían impulsos.
¡Dato curioso! El 70% de tu peso corporal es agua, pero hay elementos que necesitas en cantidades microscópicas como el hierro de tu sangre o el zinc de tus enzimas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La Arquitectura Molecular
El carbono es el arquitecto de las biomoléculas gracias a su estructura tetraédrica. Esta forma geométrica permite crear cadenas lineales, ramificadas, saturadas, insaturadas o incluso cíclicas. Es como tener un kit de construcción infinito.
Los grupos funcionales son como las herramientas especializadas de cada molécula. El grupo hidroxilo aparece en alcoholes, el carbonilo en aldehídos y cetonas, y el carboxilo en ácidos. Cada uno aporta propiedades químicas específicas.
Los bioelementos secundarios siempre aparecen ionizados en medio acuoso. Aunque solo representan una pequeña fracción, son imprescindibles para el funcionamiento celular.
Consejo de estudio: No memorices la tabla de grupos funcionales, solo entiende que cada grupo aporta características diferentes a las biomoléculas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Biomoléculas y Enlaces
Las biomoléculas se dividen en dos grandes familias: inorgánicas (agua y sales minerales) y orgánicas (glúcidos, lípidos, proteínas y ácidos nucleicos). Cada grupo tiene funciones específicas pero todas trabajan juntas.
Los enlaces covalentes son los más fuertes y forman la estructura básica de las moléculas. Los monómeros (como aminoácidos o monosacáridos) se unen mediante estos enlaces para formar polímeros complejos.
El enlace de hidrógeno es más débil pero crucial para la estabilidad molecular. El agua es el ejemplo perfecto: sus moléculas se atraen entre sí creando propiedades únicas para la vida.
Recuerda: No necesitas describir cada enlace en detalle, pero sí reconocer su importancia en diferentes biomoléculas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El Agua: La Molécula de la Vida
El agua representa aproximadamente el 70% del peso celular y es donde ocurren todas las reacciones metabólicas. Tu cuerpo literalmente está diseñado alrededor de las propiedades del agua.
Se distribuye como agua intracelular dentro de las células y agua extracelular (1/3) en sangre, linfa y entre tejidos. A mayor actividad metabólica, mayor proporción de agua necesitas.
La clave está en su estructura química: el oxígeno atrae más los electrones que el hidrógeno, creando una molécula dipolar. Esta polaridad es responsable de casi todas las propiedades extraordinarias del agua.
Dato interesante: Los organismos jóvenes tienen más agua que los adultos, y los órganos más activos (como el cerebro) contienen más agua que otros tejidos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
La Magia de la Polaridad
La polaridad del agua surge porque el oxígeno "roba" parcialmente los electrones del hidrógeno, creando zonas con carga parcial negativa (δ⁻) y positiva (δ⁺). Es como tener un imán molecular microscópico.
Esta estructura dipolar permite formar enlaces de hidrógeno entre moléculas de agua. Una molécula atrae a otras creando una red tridimensional que explica las propiedades únicas del agua.
Los enlaces de hidrógeno son relativamente débiles individualmente, pero juntos crean una fuerza colectiva impresionante. Es el principio de "la unión hace la fuerza" aplicado a nivel molecular.
Visualízalo: Imagina las moléculas de agua como pequeños imanes que se atraen entre sí, formando cadenas y redes que dan al agua sus propiedades especiales.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades Extraordinarias del Agua
La cohesividad mantiene unidas las moléculas de agua gracias a los puentes de hidrógeno. Esto hace que el agua sea prácticamente incompresible y capaz de dar volumen y turgencia a las células.
El elevado calor específico convierte al agua en un amortiguador térmico perfecto. Tu cuerpo puede mantener una temperatura estable incluso cuando el ambiente cambia bruscamente.
La elevada tensión superficial permite fenómenos como el ascenso de la savia por los árboles. Las moléculas de agua literalmente se "tiran" unas a otras hacia arriba.
Aplicación práctica: Cuando sudas, tu cuerpo aprovecha el elevado calor de vaporización del agua para enfriarse de manera muy eficiente.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El Agua como Disolvente Universal
El agua disuelve fácilmente compuestos iónicos como la sal y compuestos polares que pueden formar enlaces de hidrógeno con ella. A estos los llamamos hidrófilos (amigos del agua).
Los compuestos apolares como los aceites son hidrófobos (enemigos del agua) y no se disuelven. Pero existen moléculas anfipáticas que tienen ambas partes: una hidrófila y otra hidrófoba.
Las moléculas anfipáticas forman estructuras fascinantes: micelas (como las del jabón), monocapas en superficies, o bicapas lipídicas que forman las membranas celulares.
Conexión clave: Las membranas de tus células se forman gracias a esta propiedad anfipática de los fosfolípidos, creando barreras que separan el interior del exterior celular.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
pH y Sales Minerales
El agua puede ionizarse formando iones H⁺ y OH⁻ en concentraciones muy bajas. Esta capacidad permite que actúe como regulador del pH, manteniendo la acidez cerca de la neutralidad (pH ≈ 7).
El pH se calcula como -log[H⁺] y es crucial para la vida. La mayoría de procesos biológicos necesitan un pH cercano a 7 para funcionar correctamente.
Las sales minerales aparecen de dos formas: insolubles (formando estructuras de sostén como huesos y caparazones) y solubles (disociadas en iones que participan en múltiples funciones celulares).
Ejemplo práctico: El calcio forma tus huesos cuando está insoluble, pero cuando está disuelto como Ca²⁺ permite la contracción de tus músculos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Funciones de las Sales Minerales
Las sales insolubles forman estructuras sólidas de protección y sostén. El carbonato de calcio crea caparazones resistentes, mientras que los fosfatos de apatita forman tus huesos y dientes.
La sílice endurece las paredes celulares vegetales, dándoles la rigidez necesaria para mantenerse erguidas. Cada mineral tiene su especialidad estructural.
Las sales solubles actúan como cofactores enzimáticos. Iones como Zn²⁺, K⁺, Mn²⁺ son indispensables para que las enzimas funcionen correctamente.
Dato clave: Los iones Na⁺ y K⁺ generan diferencias de carga eléctrica a ambos lados de las membranas, permitiendo la transmisión de impulsos nerviosos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Introducción a los Glúcidos
Los glúcidos son biomoléculas orgánicas formadas por carbono, hidrógeno y oxígeno (C, H, O). Son fundamentales como fuente de energía y material estructural en los seres vivos.
Los monosacáridos son los glúcidos más sencillos y actúan como monómeros para formar estructuras más complejas. No se pueden hidrolizar (romper con agua) y contienen entre 3 y 7 átomos de carbono.
Químicamente son polihidroxialdehídos o polihidroxicetonas. Si tienen grupo aldehído son aldosas, si tienen grupo cetona son cetosas. Según el número de carbonos: triosas, tetrosas, pentosas o hexosas.
Ejemplos importantes: La D-glucosa es una aldohexosa y la D-fructosa es una cetohexosa .
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: macromoléculas
4Contenidos más populares de Biología
9Contenidos más populares
9¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.