El agua y los glúcidos son fundamentales para la vida.... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
758
•
Actualizado May 16, 2026
•
alejandra
@alejandra_mzcq8
El agua y los glúcidos son fundamentales para la vida.... Mostrar más










¿Sabías que el agua es prácticamente un "superhéroe" molecular? Sus propiedades especiales la convierten en la sustancia más importante para la vida.
La elevada constante dieléctrica del agua la convierte en el disolvente universal. Esto significa que puede disolver casi cualquier sustancia iónica o polar, lo que es perfecto para el transporte de nutrientes y desechos en tu cuerpo.
Su elevado calor específico hace que actúe como un tampón térmico. Necesitas muchísima energía para cambiar su temperatura porque parte de esa energía se usa en romper los enlaces de hidrógeno. Por eso tu cuerpo mantiene una temperatura estable aunque haga frío o calor.
El elevado calor de vaporización permite la termoregulación mediante el sudor. Cuando sudas, el agua se evapora en tu piel y te refresca. La tensión superficial permite que algunos insectos caminen sobre el agua y que las plantas transporten agua desde las raíces hasta las hojas.
¡Dato curioso! El hielo flota porque es menos denso que el agua líquida, lo que permite que los peces sobrevivan bajo la superficie congelada de lagos y ríos.

Las sales minerales son como los "electrolitos" de tu bebida deportiva favorita, pero mucho más importantes para tu organismo.
En forma sólida, forman estructuras de protección y soporte. El carbonato de calcio está en conchas y caparazones, mientras que el fosfato de calcio forma tus huesos y dientes. Son como el "cemento" que da rigidez a estas estructuras.
En disolución acuosa se separan en cationes (Na⁺, Ca²⁺, Mg²⁺) y aniones (Cl⁻, PO₄³⁻). Estos iones regulan la presión osmótica, mantienen el pH mediante disoluciones tampón como el bicarbonato en sangre, y generan los potenciales eléctricos necesarios para que funcionen tus neuronas.
La ósmosis es el movimiento del agua a través de membranas semipermeables. El agua siempre va desde donde está más diluida (hipotónica) hacia donde está más concentrada (hipertónica), buscando equilibrar las concentraciones.
Recuerda: En medio hipertónico la célula se arruga (plasmólisis en plantas), en hipotónico se hincha (turgencia), y en isotónico mantiene su volumen normal.

Entender los diferentes tipos de medios es clave para comprender cómo las células mantienen su forma y función.
En un medio hipertónico, hay más solutos fuera que dentro de la célula. El agua sale y la célula se arruga, pudiendo morir por deshidratación. En las plantas, esto se llama plasmólisis cuando la membrana se separa de la pared celular.
En un medio hipotónico ocurre lo contrario: hay menos solutos fuera que dentro. El agua entra masivamente y la célula puede explotar por exceso de agua. Este proceso se conoce como turgencia.
El medio isotónico es el ideal: igual concentración dentro y fuera. No hay intercambio neto de agua, por lo que la célula mantiene su volumen normal y funciona perfectamente.
Tip de estudio: Recuerda que "hiper" = más concentrado = célula se encoge; "hipo" = menos concentrado = célula se hincha; "iso" = igual = célula normal.

Los glúcidos o hidratos de carbono son las moléculas energéticas por excelencia. Su fórmula empírica CₙH₂ₙOₙ te dice que están formados por carbono, hidrógeno y oxígeno en proporciones específicas.
Químicamente son polialcoholes con un grupo carbonilo que puede ser aldehído (aldosas) o cetona (cetosas). La glucosa es una aldohexosa mientras que la fructosa es una cetohexosa.
Se clasifican en monosacáridos (azúcares simples no hidrolizables) y ósidos (más complejos, formados por varios monosacáridos unidos). Los ósidos se dividen en oligosacáridos como la sacarosa, polisacáridos (más de 10) como el almidón, y heterósidos que incluyen otras moléculas no glucídicas.
Para recordar: Los monosacáridos son como piezas de LEGO individuales, mientras que los polisacáridos son construcciones enormes hechas con miles de estas piezas.

Los monosacáridos son los glúcidos más simples y constituyen las unidades básicas de todos los demás. Son sólidos, cristalizables, solubles en agua, dulces y tienen poder reductor.
La presencia de carbonos asimétricos les otorga diferentes tipos de isomería. La isomería óptica les permite desviar la luz polarizada, mientras que la espacial determina si son de configuración D o L según la posición del grupo -OH más alejado del carbonilo.
Los enantiómeros tienen todos los grupos -OH en posición opuesta , mientras que los epímeros solo difieren en la posición de un -OH en un carbono específico .
En disolución acuosa adoptan estructura cíclica formando enlaces hemiacetálicos intramoleculares. Esto crea anómeros α y β . Las aldohexosas forman anillos de 6 vértices (piranosas) y las cetohexosas anillos de 5 (furanosas).
Truco visual: Imagina los anómeros como si fueras a estrechar la mano: α es con la palma hacia abajo, β es con la palma hacia arriba.

Cada tipo de monosacárido tiene funciones específicas en los seres vivos. Las triosas como gliceraldehído participan en el metabolismo energético, mientras que las pentosas forman parte de los ácidos nucleicos: ribosa en el ARN y desoxirribosa en el ADN.
Las hexosas son las más importantes energéticamente. La glucosa es el azúcar más utilizado como fuente de energía y su polimerización forma almidón y glucógeno. La galactosa se encuentra en la sangre y la fructosa abunda en frutas.
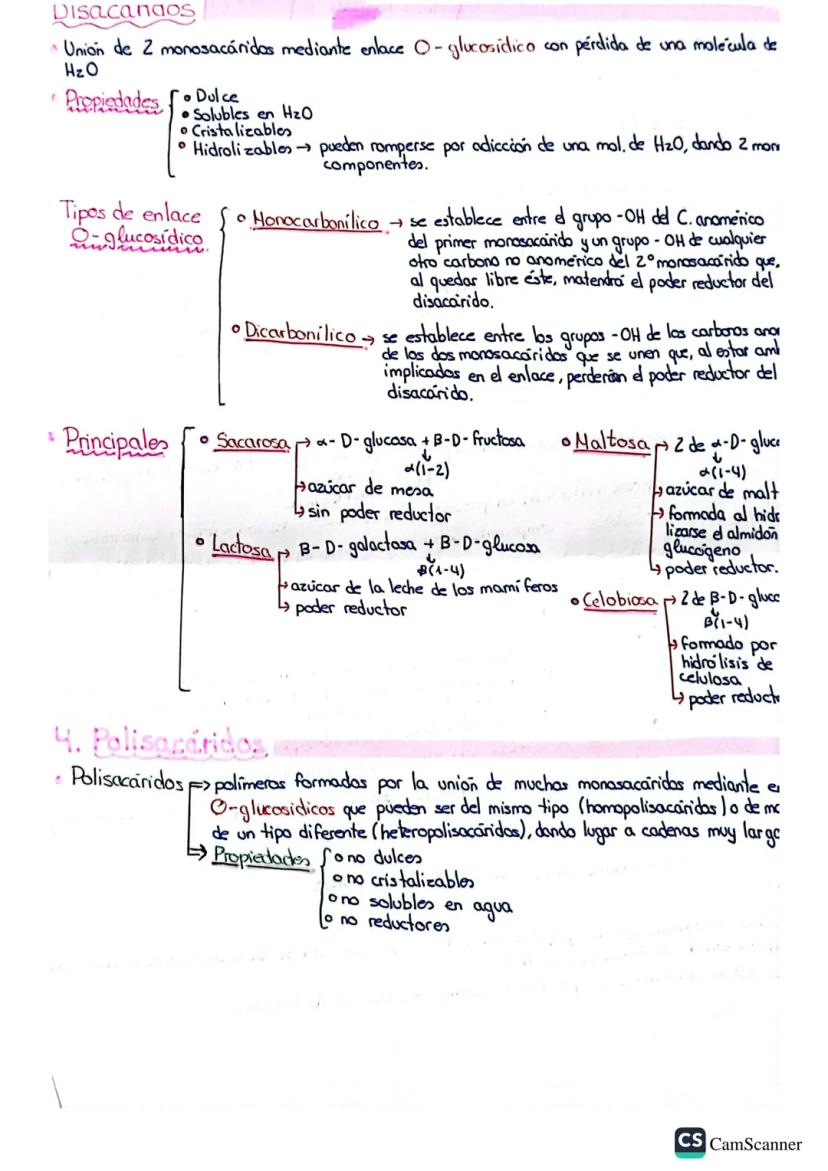
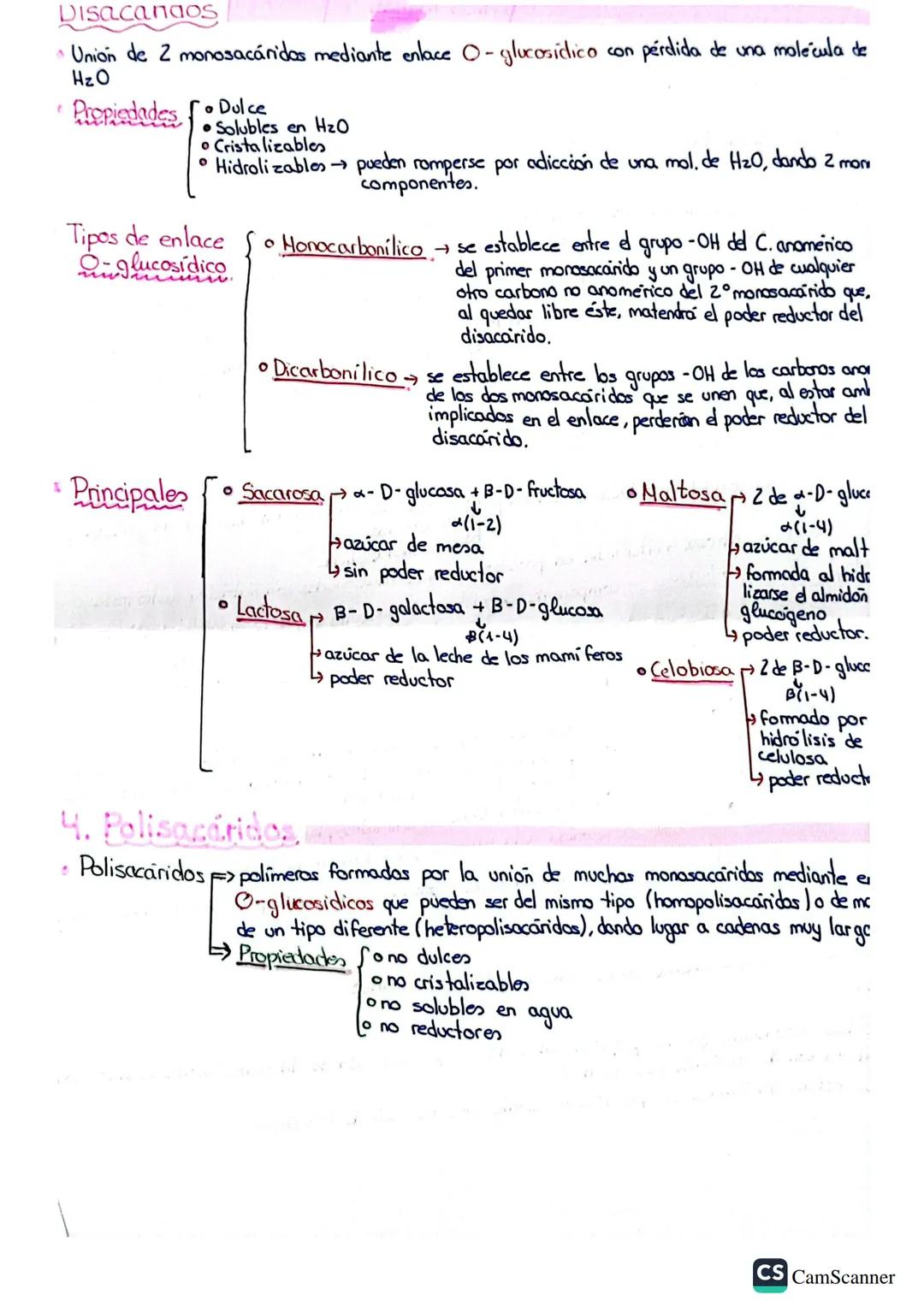
El enlace O-glucosídico une dos monosacáridos liberando agua. Puede ser monocarbonílico (mantiene poder reductor) o dicarbonílico (pierde poder reductor).
Los disacáridos principales son la sacarosa y la lactosa .
Dato útil: Si un disacárido conserva un carbono anomérico libre, tendrá poder reductor; si ambos están implicados en el enlace, lo perderá.

Los polisacáridos son polímeros gigantes formados por muchos monosacáridos. A diferencia de los azúcares simples, no son dulces, no cristalizan, no son solubles en agua y carecen de poder reductor.
Los homopolisacáridos de reserva energética incluyen el almidón (vegetal) con amilosa y amilopectina , y el glucógeno (animal) similar a la amilopectina pero más ramificado.
Los estructurales como la celulosa forman fibras resistentes en las paredes celulares vegetales mediante enlaces β(1-4) entre glucosas. La quitina constituye el exoesqueleto de artrópodos.
Los heteropolisacáridos tienen composición mixta: pectina (gelificante), hemicelulosa (pared celular), agar-agar (espesante de algas) y mucopolisacáridos (dan elasticidad a tejidos conectivos).
Comparación clave: El almidón y glucógeno son como "baterías" que almacenan energía, mientras que la celulosa y quitina son como "vigas" que dan estructura y resistencia.
Los ácidos grasos son moléculas anfipáticas con una cabeza polar hidrofílica y una cola apolar hidrofóbica (cadena carbonada). Esta dualidad les permite formar estructuras especiales como micelas en medio acuoso.
Su punto de fusión aumenta con la longitud de la cadena y disminuye con las insaturaciones. Los saturados (solo enlaces simples) son sólidos como el ácido palmítico, mientras que los insaturados (con dobles enlaces) son líquidos como el oleico.
Los triacilglicéridos se forman por esterificación de tres ácidos grasos con glicerina. Son completamente apolares e insolubles en agua. Los de origen vegetal (aceites) son líquidos por tener ácidos grasos insaturados, mientras que los animales (grasas) son sólidos por sus ácidos grasos saturados.
Sus funciones principales son reserva energética (adipocitos), aislamiento térmico, flotabilidad y protección mecánica.
Regla práctica: Si es líquido a temperatura ambiente probablemente sea vegetal e insaturado; si es sólido, probablemente sea animal y saturado.

Las ceras son ésteres de ácidos grasos de cadena larga con monoalcoholes también largos. Son sólidas e insolubles, perfectas para recubrimiento (pelo, plumas, hojas) y reserva energética en plancton.
Los fosfolípidos son los protagonistas de las membranas celulares. Tienen glicerol unido a dos ácidos grasos y un grupo fosfato con un radical polar. Su naturaleza anfipática les permite formar bicapas con las cabezas polares hacia el agua y las colas hidrofóbicas hacia el interior.
Los esfingolípidos también forman membranas, especialmente abundantes en tejido nervioso. Están formados por esfingosina (aminoalcohol), un ácido graso y un componente polar, creando la estructura básica llamada ceramida.
Visualización útil: Imagina los fosfolípidos como personas con brazos extendidos formando una barrera humana: las cabezas miran hacia fuera (al agua) y los brazos se entrelazan en el medio (evitando el agua).

Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
alejandra
@alejandra_mzcq8
El agua y los glúcidos son fundamentales para la vida. El agua actúa como el "disolvente universal" gracias a sus propiedades únicas, mientras que los glúcidos son nuestro "combustible" principal y forman estructuras celulares esenciales.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Sabías que el agua es prácticamente un "superhéroe" molecular? Sus propiedades especiales la convierten en la sustancia más importante para la vida.
La elevada constante dieléctrica del agua la convierte en el disolvente universal. Esto significa que puede disolver casi cualquier sustancia iónica o polar, lo que es perfecto para el transporte de nutrientes y desechos en tu cuerpo.
Su elevado calor específico hace que actúe como un tampón térmico. Necesitas muchísima energía para cambiar su temperatura porque parte de esa energía se usa en romper los enlaces de hidrógeno. Por eso tu cuerpo mantiene una temperatura estable aunque haga frío o calor.
El elevado calor de vaporización permite la termoregulación mediante el sudor. Cuando sudas, el agua se evapora en tu piel y te refresca. La tensión superficial permite que algunos insectos caminen sobre el agua y que las plantas transporten agua desde las raíces hasta las hojas.
¡Dato curioso! El hielo flota porque es menos denso que el agua líquida, lo que permite que los peces sobrevivan bajo la superficie congelada de lagos y ríos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las sales minerales son como los "electrolitos" de tu bebida deportiva favorita, pero mucho más importantes para tu organismo.
En forma sólida, forman estructuras de protección y soporte. El carbonato de calcio está en conchas y caparazones, mientras que el fosfato de calcio forma tus huesos y dientes. Son como el "cemento" que da rigidez a estas estructuras.
En disolución acuosa se separan en cationes (Na⁺, Ca²⁺, Mg²⁺) y aniones (Cl⁻, PO₄³⁻). Estos iones regulan la presión osmótica, mantienen el pH mediante disoluciones tampón como el bicarbonato en sangre, y generan los potenciales eléctricos necesarios para que funcionen tus neuronas.
La ósmosis es el movimiento del agua a través de membranas semipermeables. El agua siempre va desde donde está más diluida (hipotónica) hacia donde está más concentrada (hipertónica), buscando equilibrar las concentraciones.
Recuerda: En medio hipertónico la célula se arruga (plasmólisis en plantas), en hipotónico se hincha (turgencia), y en isotónico mantiene su volumen normal.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Entender los diferentes tipos de medios es clave para comprender cómo las células mantienen su forma y función.
En un medio hipertónico, hay más solutos fuera que dentro de la célula. El agua sale y la célula se arruga, pudiendo morir por deshidratación. En las plantas, esto se llama plasmólisis cuando la membrana se separa de la pared celular.
En un medio hipotónico ocurre lo contrario: hay menos solutos fuera que dentro. El agua entra masivamente y la célula puede explotar por exceso de agua. Este proceso se conoce como turgencia.
El medio isotónico es el ideal: igual concentración dentro y fuera. No hay intercambio neto de agua, por lo que la célula mantiene su volumen normal y funciona perfectamente.
Tip de estudio: Recuerda que "hiper" = más concentrado = célula se encoge; "hipo" = menos concentrado = célula se hincha; "iso" = igual = célula normal.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los glúcidos o hidratos de carbono son las moléculas energéticas por excelencia. Su fórmula empírica CₙH₂ₙOₙ te dice que están formados por carbono, hidrógeno y oxígeno en proporciones específicas.
Químicamente son polialcoholes con un grupo carbonilo que puede ser aldehído (aldosas) o cetona (cetosas). La glucosa es una aldohexosa mientras que la fructosa es una cetohexosa.
Se clasifican en monosacáridos (azúcares simples no hidrolizables) y ósidos (más complejos, formados por varios monosacáridos unidos). Los ósidos se dividen en oligosacáridos como la sacarosa, polisacáridos (más de 10) como el almidón, y heterósidos que incluyen otras moléculas no glucídicas.
Para recordar: Los monosacáridos son como piezas de LEGO individuales, mientras que los polisacáridos son construcciones enormes hechas con miles de estas piezas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los monosacáridos son los glúcidos más simples y constituyen las unidades básicas de todos los demás. Son sólidos, cristalizables, solubles en agua, dulces y tienen poder reductor.
La presencia de carbonos asimétricos les otorga diferentes tipos de isomería. La isomería óptica les permite desviar la luz polarizada, mientras que la espacial determina si son de configuración D o L según la posición del grupo -OH más alejado del carbonilo.
Los enantiómeros tienen todos los grupos -OH en posición opuesta , mientras que los epímeros solo difieren en la posición de un -OH en un carbono específico .
En disolución acuosa adoptan estructura cíclica formando enlaces hemiacetálicos intramoleculares. Esto crea anómeros α y β . Las aldohexosas forman anillos de 6 vértices (piranosas) y las cetohexosas anillos de 5 (furanosas).
Truco visual: Imagina los anómeros como si fueras a estrechar la mano: α es con la palma hacia abajo, β es con la palma hacia arriba.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Cada tipo de monosacárido tiene funciones específicas en los seres vivos. Las triosas como gliceraldehído participan en el metabolismo energético, mientras que las pentosas forman parte de los ácidos nucleicos: ribosa en el ARN y desoxirribosa en el ADN.
Las hexosas son las más importantes energéticamente. La glucosa es el azúcar más utilizado como fuente de energía y su polimerización forma almidón y glucógeno. La galactosa se encuentra en la sangre y la fructosa abunda en frutas.
El enlace O-glucosídico une dos monosacáridos liberando agua. Puede ser monocarbonílico (mantiene poder reductor) o dicarbonílico (pierde poder reductor).
Los disacáridos principales son la sacarosa y la lactosa .
Dato útil: Si un disacárido conserva un carbono anomérico libre, tendrá poder reductor; si ambos están implicados en el enlace, lo perderá.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los polisacáridos son polímeros gigantes formados por muchos monosacáridos. A diferencia de los azúcares simples, no son dulces, no cristalizan, no son solubles en agua y carecen de poder reductor.
Los homopolisacáridos de reserva energética incluyen el almidón (vegetal) con amilosa y amilopectina , y el glucógeno (animal) similar a la amilopectina pero más ramificado.
Los estructurales como la celulosa forman fibras resistentes en las paredes celulares vegetales mediante enlaces β(1-4) entre glucosas. La quitina constituye el exoesqueleto de artrópodos.
Los heteropolisacáridos tienen composición mixta: pectina (gelificante), hemicelulosa (pared celular), agar-agar (espesante de algas) y mucopolisacáridos (dan elasticidad a tejidos conectivos).
Comparación clave: El almidón y glucógeno son como "baterías" que almacenan energía, mientras que la celulosa y quitina son como "vigas" que dan estructura y resistencia.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los ácidos grasos son moléculas anfipáticas con una cabeza polar hidrofílica y una cola apolar hidrofóbica (cadena carbonada). Esta dualidad les permite formar estructuras especiales como micelas en medio acuoso.
Su punto de fusión aumenta con la longitud de la cadena y disminuye con las insaturaciones. Los saturados (solo enlaces simples) son sólidos como el ácido palmítico, mientras que los insaturados (con dobles enlaces) son líquidos como el oleico.
Los triacilglicéridos se forman por esterificación de tres ácidos grasos con glicerina. Son completamente apolares e insolubles en agua. Los de origen vegetal (aceites) son líquidos por tener ácidos grasos insaturados, mientras que los animales (grasas) son sólidos por sus ácidos grasos saturados.
Sus funciones principales son reserva energética (adipocitos), aislamiento térmico, flotabilidad y protección mecánica.
Regla práctica: Si es líquido a temperatura ambiente probablemente sea vegetal e insaturado; si es sólido, probablemente sea animal y saturado.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las ceras son ésteres de ácidos grasos de cadena larga con monoalcoholes también largos. Son sólidas e insolubles, perfectas para recubrimiento (pelo, plumas, hojas) y reserva energética en plancton.
Los fosfolípidos son los protagonistas de las membranas celulares. Tienen glicerol unido a dos ácidos grasos y un grupo fosfato con un radical polar. Su naturaleza anfipática les permite formar bicapas con las cabezas polares hacia el agua y las colas hidrofóbicas hacia el interior.
Los esfingolípidos también forman membranas, especialmente abundantes en tejido nervioso. Están formados por esfingosina (aminoalcohol), un ácido graso y un componente polar, creando la estructura básica llamada ceramida.
Visualización útil: Imagina los fosfolípidos como personas con brazos extendidos formando una barrera humana: las cabezas miran hacia fuera (al agua) y los brazos se entrelazan en el medio (evitando el agua).

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
19
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS