Los bioelementos y biomoléculas son los componentes fundamentales que hacen... Mostrar más
Bioelementos y Biomoléculas Inorgánicas: Apuntes Visuales y Esquemáticos










Características de los seres vivos y bioelementos
¿Alguna vez te has preguntado qué tienen en común una bacteria, un árbol y tú? Todos los seres vivos compartimos seis características fundamentales que nos definen como "vivos".
Las tres funciones vitales (nutrición, relación y reproducción) son el punto de partida. Además, la célula actúa como nuestra unidad básica - es como el ladrillo fundamental de la vida. Los seres vivos también mantenemos la homeostasis, que es nuestra capacidad de mantener el equilibrio interno pese a los cambios externos.
Una característica clave es que estamos formados por bioelementos (elementos químicos específicos) y biomoléculas. No utilizamos cualquier elemento de la tabla periódica, sino una selección de unos 70 elementos, de los cuales solo 20-25 están presentes en casi todas las formas de vida.
Los bioelementos primarios representan más del 95% de nuestra composición. Forman enlaces covalentes estables y crean los grupos funcionales que dan propiedades específicas a las biomoléculas.
Dato curioso: El nitrógeno es el elemento más abundante en el aire, pero no podemos utilizarlo directamente. Necesitamos que las bacterias nitrificantes lo transformen para que llegue a las plantas.

El carbono y otros bioelementos esenciales
El carbono es literalmente el elemento que sustenta la vida, y sus propiedades lo convierten en el protagonista absoluto de las biomoléculas. Su superpoder está en formar cuatro enlaces covalentes estables, crear cadenas largas y estables con otros carbonos, y combinarse con oxígeno, nitrógeno e hidrógeno para formar grupos funcionales.
Los bioelementos secundarios (alrededor del 4,5% de nuestra composición) tienen funciones muy específicas. El fósforo forma parte del ATP, nuestra "moneda energética", mientras que el azufre está en aminoácidos importantes como la cisteína. El calcio no solo endurece huesos y dientes, sino que participa en la contracción muscular.
Los oligoelementos representan menos del 0,5% de nuestra composición, pero su ausencia provoca problemas graves. El hierro transporta oxígeno en la hemoglobina, el yodo forma las hormonas tiroideas, y el flúor protege el esmalte dental.
Recuerda: Aunque estos elementos están en pequeñas cantidades, son absolutamente esenciales. Una deficiencia de hierro causa anemia, y la falta de yodo provoca problemas tiroideos.

Biomoléculas y sus enlaces
Las biomoléculas son los compuestos que forman la materia viva, y se dividen en dos grandes grupos. Las inorgánicas son simples y pobres en energía (agua, sales minerales), mientras que las orgánicas son complejas y ricas en energía (glúcidos, lípidos, proteínas, ácidos nucleicos).
Los enlaces covalentes son la base de las biomoléculas orgánicas. Pueden ser apolares o polares . Los enlaces apolares forman el esqueleto básico de las biomoléculas, mientras que los polares crean dipolos importantes.
Los enlaces iónicos se forman cuando un elemento muy electronegativo "roba" electrones a otro muy electropositivo. Esto crea cationes (carga positiva) y aniones (carga negativa) que forman las redes cristalinas características de las sales minerales.
Estos enlaces intramoleculares determinan la estructura básica de las moléculas y son fundamentales para entender cómo se construye la materia viva.
Tip de estudio: Piensa en los enlaces covalentes polares como un "tira y afloja" molecular - un átomo atrae más fuertemente los electrones compartidos.
Interacciones intermoleculares
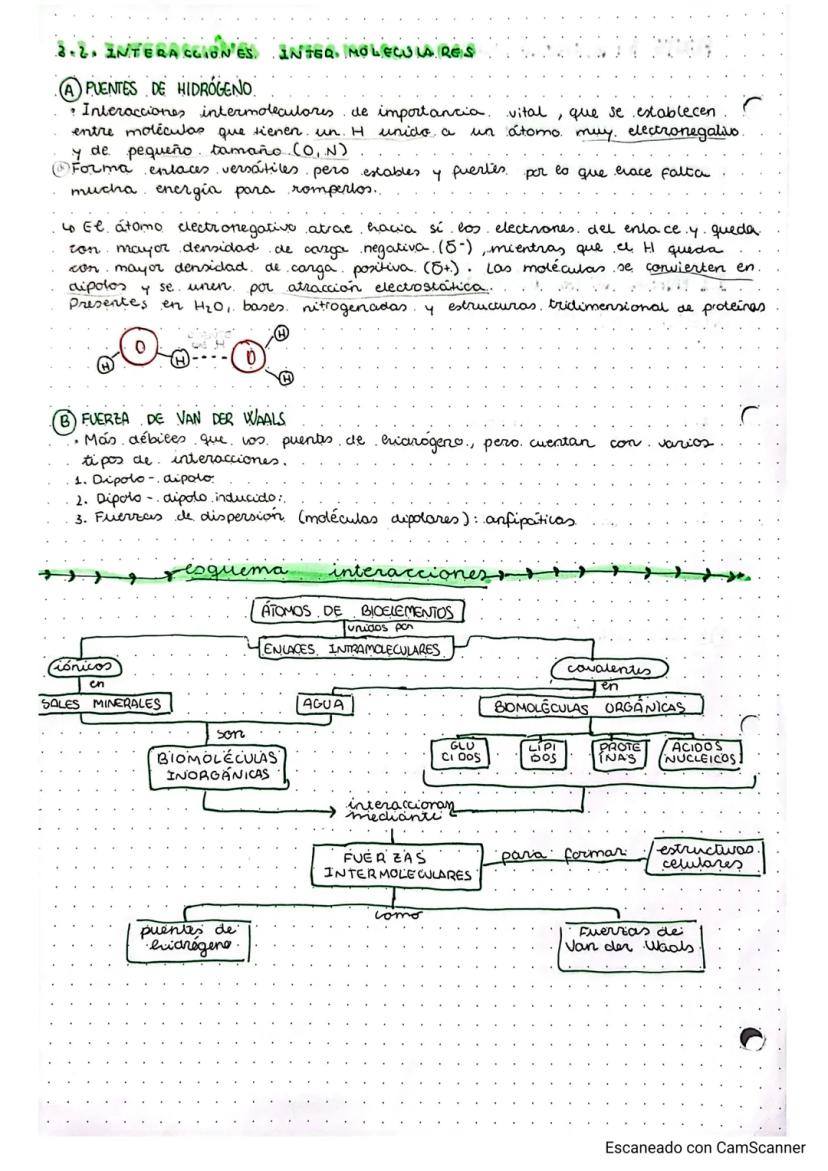
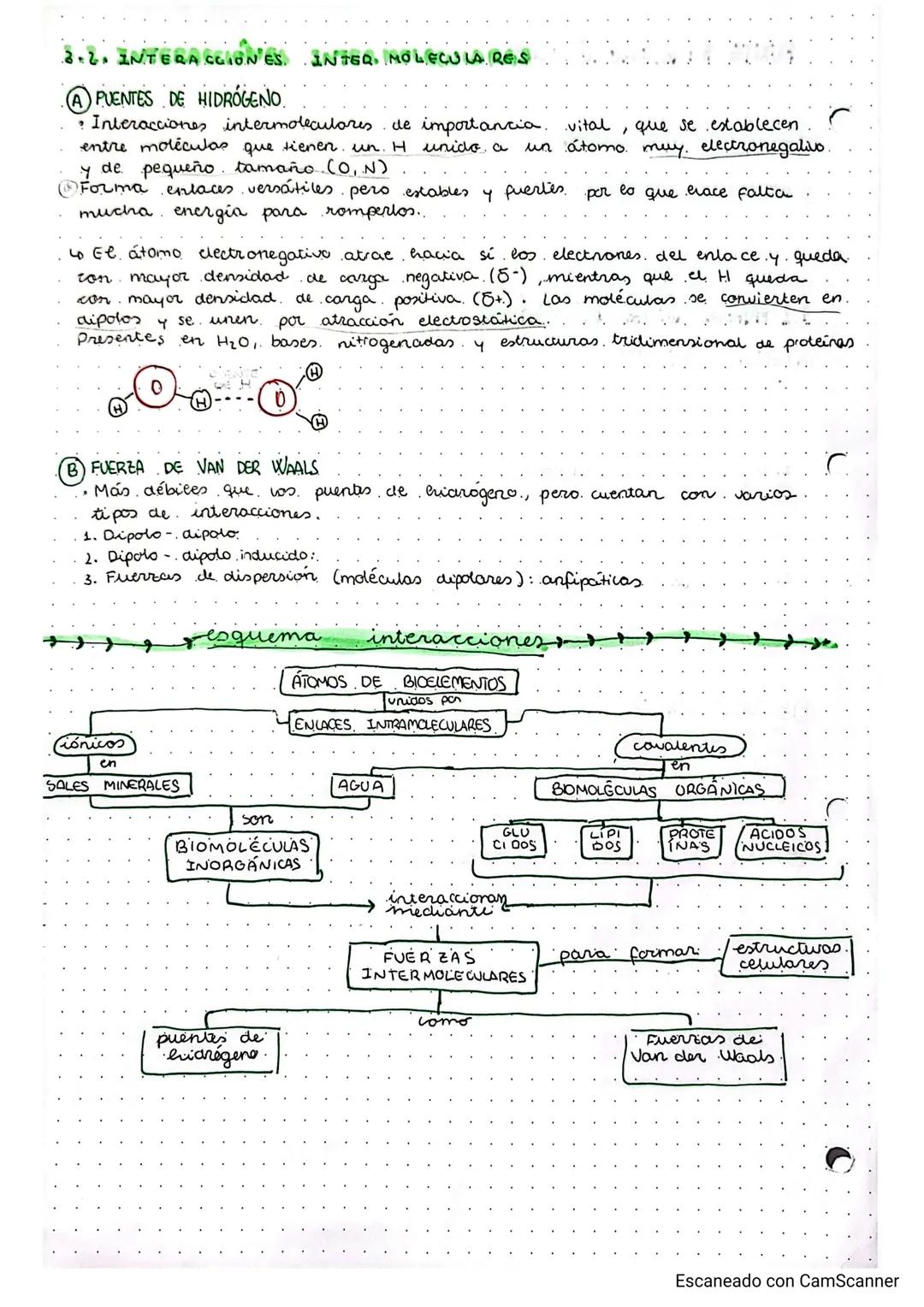
Las interacciones intermoleculares son las fuerzas que mantienen unidas las moléculas entre sí, y son cruciales para la estructura tridimensional de las biomoléculas.
Los puentes de hidrógeno son las estrellas del espectáculo. Se forman cuando un hidrógeno está unido a un átomo muy electronegativo (como oxígeno o nitrógeno). Aunque son más débiles que los enlaces covalentes, son lo suficientemente fuertes como para necesitar mucha energía para romperse. Están presentes en el agua, las bases nitrogenadas del ADN, y determinan la forma tridimensional de las proteínas.
Las fuerzas de Van der Waals son más débiles pero incluyen varios tipos de interacciones: dipolo-dipolo, dipolo-dipolo inducido, y fuerzas de dispersión. Son especialmente importantes en moléculas anfipáticas (que tienen partes solubles e insolubles).
Estas interacciones permiten que las biomoléculas mantengan estructuras complejas y funcionales, desde la doble hélice del ADN hasta la forma específica de las enzimas.
Conexión importante: Sin puentes de hidrógeno, el ADN no mantendría su estructura de doble hélice y las proteínas no tendrían su forma funcional.

El agua: la molécula de la vida
El agua es el componente mayoritario de todos los seres vivos y absolutamente indispensable para la vida. En el ser humano, representa diferentes porcentajes según la edad, el tipo de tejido y el sexo, siendo mayor en los hombres.
La distribución del agua en nuestro organismo es fascinante: dos tercios están dentro de las células (agua intracelular), y el tercio restante se reparte entre el líquido intersticial (80%) y el plasma sanguíneo (20%). Entre estos compartimentos hay un intercambio constante.
La estructura del agua es clave para entender sus propiedades. Dos átomos de hidrógeno se unen mediante enlaces covalentes polares a un átomo de oxígeno, formando un ángulo de 104,5°. Esta estructura dipolar facilita la formación de puentes de hidrógeno entre moléculas de agua.
Los diferentes estados del agua (sólido, líquido, gaseoso) dependen de cómo se forman y rompen estos puentes de hidrógeno. En el hielo, los puentes mantienen posiciones fijas; en estado líquido, se forman y rompen continuamente; en vapor, se rompen completamente.
Dato vital: No podemos almacenar ni sintetizar agua, por eso debemos ingerir constantemente este líquido para compensar las pérdidas diarias.

Propiedades extraordinarias del agua
Las propiedades del agua son resultado directo de los puentes de hidrógeno, y cada una tiene una importancia biológica específica.
El elevado calor específico significa que necesitas mucha energía para cambiar la temperatura del agua. Esto permite que mantenga su temperatura constante e influye en el clima de las zonas costeras. Su alto calor de vaporización hace que al evaporarse absorba más calor que cualquier otra sustancia, lo que es perfecto para la regulación térmica.
La capilaridad permite que el agua ascienda por conductos estrechos (como los vasos de las plantas) gracias a la cohesión entre sus moléculas y su capacidad de adhesión a superficies.
Una propiedad única es que su densidad máxima se alcanza a 4°C. Cuando se enfría más, los puentes de hidrógeno ocupan más volumen y disminuye la densidad, por eso el hielo flota. Esto permite la vida en los polos, ya que el hielo actúa como aislante.
El alto poder disolvente convierte al agua en el "disolvente universal", capaz de disolver gran cantidad de sustancias iónicas y polares.
Aplicación práctica: Estas propiedades explican por qué sudamos para refrescarnos (calor de vaporización) y por qué las plantas pueden transportar agua desde las raíces (capilaridad).

Solubilidad y comportamiento de las sustancias en agua
Según su solubilidad en agua, las sustancias se clasifican en tres grupos importantes que debes conocer perfectamente.
Las sustancias hidrófilas (solubles) incluyen las iónicas como la sal (NaCl) y las covalentes polares como monosacáridos, aminoácidos y nucleótidos. Estas se disuelven fácilmente porque interaccionan bien con las moléculas de agua.
Las sustancias hidrófobas (insolubles) son covalentes apolares como los triglicéridos (grasas). No se disuelven porque no pueden formar puentes de hidrógeno con el agua.
Las sustancias anfipáticas tienen partes solubles y partes insolubles, y su comportamiento es fascinante. Pueden formar tres estructuras diferentes: monocapas en la superficie del agua (como el aceite), micelas esféricas con las partes insolubles hacia dentro (como el jabón limpiando), y bicapas que separan dos medios acuosos (como las membranas celulares).
Ejemplo cotidiano: Cuando lavas los platos con jabón, las micelas "atrapan" la grasa en su interior hidrófobo mientras su exterior hidrófilo se disuelve en el agua.

Sales minerales y regulación del pH
Las sales minerales existen en dos formas en los seres vivos, cada una con funciones específicas que debes distinguir claramente.
Las sales precipitadas tienen función estructural y de protección. Los fosfatos y carbonatos de calcio forman nuestro esqueleto, el carbonato cálcico endurece caparazones de crustáceos, y la sílice da rigidez a esponjas y plantas.
Las sales ionizadas forman los fluidos corporales e incluyen cationes como Na⁺, K⁺, Ca²⁺ y aniones como Cl⁻, PO₄³⁻. Tienen funciones específicas: Na⁺ y K⁺ mantienen el potencial de membrana, varios iones actúan como cofactores enzimáticos.
La función homeostática más importante es la regulación del pH mediante sistemas tampón o buffer. El sistema bicarbonato actúa a nivel extracelular, mientras que el sistema fosfato funciona intracelularmente. Ambos mantienen el pH constante añadiendo o quitando protones (H⁺) según sea necesario.
Recuerda que pH bajo significa más ácido (más H⁺), mientras que pH alto significa más básico (menos H⁺).
Conexión vital: Sin estos sistemas tampón, pequeños cambios en la acidez podrían alterar la forma de las proteínas y detener procesos vitales.

Sistemas tampón y procesos osmóticos
Los sistemas tampón funcionan como reguladores automáticos del pH en tu organismo. El tampón bicarbonato actúa principalmente en la sangre, mientras que el tampón fosfato funciona dentro de las células.
La ósmosis es el movimiento de agua a través de membranas semipermeables, desde la solución más diluida (hipotónica) hacia la más concentrada (hipertónica), hasta igualar concentraciones (isotónicas).
En células vegetales, la ósmosis crea tres estados: turgencia (célula hinchada en medio hipotónico), flacidez (equilibrio en medio isotónico), y plasmólisis (célula deshidratada en medio hipertónico). La pared celular rígida protege contra la rotura.
En células animales, sin pared protectora, los efectos son más dramáticos: lisis (rotura en medio hipotónico), estado normal (en medio isotónico), y crenación o retracción (en medio hipertónico).
Aplicación médica: Los sueros intravenosos deben ser isotónicos con la sangre para evitar dañar los glóbulos rojos por lisis o crenación.

Difusión y diálisis
La difusión y la diálisis son procesos de transporte pasivo fundamentales para el funcionamiento celular y tienen aplicaciones médicas importantes.
La difusión consiste en el movimiento de moléculas disueltas desde áreas de mayor concentración hacia áreas de menor concentración, hasta igualar las concentraciones. Es el concepto inverso a la ósmosis: aquí se mueven los solutos en lugar del agua.
Este proceso es fundamental para la respiración celular, ya que permite que el oxígeno entre en las células y el dióxido de carbono salga, siguiendo sus gradientes de concentración respectivos.
La diálisis es el paso de agua y partículas pequeñas (como sales minerales) a través de membranas que permiten este tránsito pero no el de macromoléculas. Este principio se utiliza en las máquinas de diálisis renal, donde se eliminan toxinas de la sangre cuando los riñones no funcionan correctamente.
Ambos procesos son pasivos, lo que significa que no requieren gasto energético por parte de la célula, aprovechando la energía cinética natural de las moléculas.
Aplicación médica: La diálisis renal salva vidas al reemplazar artificialmente una función vital de los riñones mediante estos principios físico-químicos básicos.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: elementos biológicos
9Apuntes de bioelementos y biomoléculas
Apuntes de bioelementos y biomoléculas
bioelementos agua y sales minerales
agua y sales minerales
bioelementos. Agua y sales
Tema de primero y segundo de bachillerato que habla acerca del agua y las sales minerales
biomoléculas y bioelementos
esquema de conceptos
BG: bloque 1 pt.1
Agua, ósmosis, sales minerales y bioelementos.
Tema 1 Biología
Biología tema 1: los bioelementos
Bioelementos, agua y sales minerales
Bioelementos, agua y sales minerales
Tema 1 - los bioelementos y biomoléculas
Trata lo que son los bioelementos y las biomoléculas y sus propiedades correspondientes
Los biolementos y biomoléculas
Bioelementos y biomoléculas
Contenidos más populares de Biología
9Replicación, transcripción y traducción
Esquema del tema de flujo de información genética del bloque de Biología Molecular
Fotosíntesis
Conceptos básicos y reacciones químicas que se producen
Descubriendo la vida: Flashcards de Biología
Aprende sobre los fundamentos de la biología con esta colección de flashcards interactivos. ¡Explora los conceptos clave y amplía tus conocimientos sobre la vida en este emocionante viaje de aprendizaje!
GENÉTICA MOLECULAR
Genética molecular 2 bachillerato y PAU
Catabolismo y anabolismo
Apuntes “esquematizados” con imágenes y visual
Anabolismo y Catabolismo
amabolismo y catabolismo
Metabolismo
Apuntes de metabolismo de segundo de bachillerato (biología). También recomiendo acompañar el estudio de este tema con el esquema que he subido para entenderlo mejor.
METABOLISMO CELULAR (CATABOLISMO + ANABOLISMO)
Apuntes completos de catabolismo y anabolismo de 2 bach
las plantas 🌳🌿
el reino de las plantas
Contenidos más populares
9Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
QUIZZ VIDA DIARIA#1
QUIZZ sobre tu vida diaria, psicológico para mejorar el estudio.:] [ Cualquier pregunta, la responderé ]^^
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Bioelementos y Biomoléculas Inorgánicas: Apuntes Visuales y Esquemáticos
Los bioelementos y biomoléculas son los componentes fundamentales que hacen posible la vida. Entender cómo el carbono, hidrógeno, oxígeno y otros elementos se combinan para formar las estructuras básicas de todos los seres vivos te ayudará a comprender desde el... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Características de los seres vivos y bioelementos
¿Alguna vez te has preguntado qué tienen en común una bacteria, un árbol y tú? Todos los seres vivos compartimos seis características fundamentales que nos definen como "vivos".
Las tres funciones vitales (nutrición, relación y reproducción) son el punto de partida. Además, la célula actúa como nuestra unidad básica - es como el ladrillo fundamental de la vida. Los seres vivos también mantenemos la homeostasis, que es nuestra capacidad de mantener el equilibrio interno pese a los cambios externos.
Una característica clave es que estamos formados por bioelementos (elementos químicos específicos) y biomoléculas. No utilizamos cualquier elemento de la tabla periódica, sino una selección de unos 70 elementos, de los cuales solo 20-25 están presentes en casi todas las formas de vida.
Los bioelementos primarios representan más del 95% de nuestra composición. Forman enlaces covalentes estables y crean los grupos funcionales que dan propiedades específicas a las biomoléculas.
Dato curioso: El nitrógeno es el elemento más abundante en el aire, pero no podemos utilizarlo directamente. Necesitamos que las bacterias nitrificantes lo transformen para que llegue a las plantas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El carbono y otros bioelementos esenciales
El carbono es literalmente el elemento que sustenta la vida, y sus propiedades lo convierten en el protagonista absoluto de las biomoléculas. Su superpoder está en formar cuatro enlaces covalentes estables, crear cadenas largas y estables con otros carbonos, y combinarse con oxígeno, nitrógeno e hidrógeno para formar grupos funcionales.
Los bioelementos secundarios (alrededor del 4,5% de nuestra composición) tienen funciones muy específicas. El fósforo forma parte del ATP, nuestra "moneda energética", mientras que el azufre está en aminoácidos importantes como la cisteína. El calcio no solo endurece huesos y dientes, sino que participa en la contracción muscular.
Los oligoelementos representan menos del 0,5% de nuestra composición, pero su ausencia provoca problemas graves. El hierro transporta oxígeno en la hemoglobina, el yodo forma las hormonas tiroideas, y el flúor protege el esmalte dental.
Recuerda: Aunque estos elementos están en pequeñas cantidades, son absolutamente esenciales. Una deficiencia de hierro causa anemia, y la falta de yodo provoca problemas tiroideos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Biomoléculas y sus enlaces
Las biomoléculas son los compuestos que forman la materia viva, y se dividen en dos grandes grupos. Las inorgánicas son simples y pobres en energía (agua, sales minerales), mientras que las orgánicas son complejas y ricas en energía (glúcidos, lípidos, proteínas, ácidos nucleicos).
Los enlaces covalentes son la base de las biomoléculas orgánicas. Pueden ser apolares o polares . Los enlaces apolares forman el esqueleto básico de las biomoléculas, mientras que los polares crean dipolos importantes.
Los enlaces iónicos se forman cuando un elemento muy electronegativo "roba" electrones a otro muy electropositivo. Esto crea cationes (carga positiva) y aniones (carga negativa) que forman las redes cristalinas características de las sales minerales.
Estos enlaces intramoleculares determinan la estructura básica de las moléculas y son fundamentales para entender cómo se construye la materia viva.
Tip de estudio: Piensa en los enlaces covalentes polares como un "tira y afloja" molecular - un átomo atrae más fuertemente los electrones compartidos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Interacciones intermoleculares
Las interacciones intermoleculares son las fuerzas que mantienen unidas las moléculas entre sí, y son cruciales para la estructura tridimensional de las biomoléculas.
Los puentes de hidrógeno son las estrellas del espectáculo. Se forman cuando un hidrógeno está unido a un átomo muy electronegativo (como oxígeno o nitrógeno). Aunque son más débiles que los enlaces covalentes, son lo suficientemente fuertes como para necesitar mucha energía para romperse. Están presentes en el agua, las bases nitrogenadas del ADN, y determinan la forma tridimensional de las proteínas.
Las fuerzas de Van der Waals son más débiles pero incluyen varios tipos de interacciones: dipolo-dipolo, dipolo-dipolo inducido, y fuerzas de dispersión. Son especialmente importantes en moléculas anfipáticas (que tienen partes solubles e insolubles).
Estas interacciones permiten que las biomoléculas mantengan estructuras complejas y funcionales, desde la doble hélice del ADN hasta la forma específica de las enzimas.
Conexión importante: Sin puentes de hidrógeno, el ADN no mantendría su estructura de doble hélice y las proteínas no tendrían su forma funcional.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El agua: la molécula de la vida
El agua es el componente mayoritario de todos los seres vivos y absolutamente indispensable para la vida. En el ser humano, representa diferentes porcentajes según la edad, el tipo de tejido y el sexo, siendo mayor en los hombres.
La distribución del agua en nuestro organismo es fascinante: dos tercios están dentro de las células (agua intracelular), y el tercio restante se reparte entre el líquido intersticial (80%) y el plasma sanguíneo (20%). Entre estos compartimentos hay un intercambio constante.
La estructura del agua es clave para entender sus propiedades. Dos átomos de hidrógeno se unen mediante enlaces covalentes polares a un átomo de oxígeno, formando un ángulo de 104,5°. Esta estructura dipolar facilita la formación de puentes de hidrógeno entre moléculas de agua.
Los diferentes estados del agua (sólido, líquido, gaseoso) dependen de cómo se forman y rompen estos puentes de hidrógeno. En el hielo, los puentes mantienen posiciones fijas; en estado líquido, se forman y rompen continuamente; en vapor, se rompen completamente.
Dato vital: No podemos almacenar ni sintetizar agua, por eso debemos ingerir constantemente este líquido para compensar las pérdidas diarias.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades extraordinarias del agua
Las propiedades del agua son resultado directo de los puentes de hidrógeno, y cada una tiene una importancia biológica específica.
El elevado calor específico significa que necesitas mucha energía para cambiar la temperatura del agua. Esto permite que mantenga su temperatura constante e influye en el clima de las zonas costeras. Su alto calor de vaporización hace que al evaporarse absorba más calor que cualquier otra sustancia, lo que es perfecto para la regulación térmica.
La capilaridad permite que el agua ascienda por conductos estrechos (como los vasos de las plantas) gracias a la cohesión entre sus moléculas y su capacidad de adhesión a superficies.
Una propiedad única es que su densidad máxima se alcanza a 4°C. Cuando se enfría más, los puentes de hidrógeno ocupan más volumen y disminuye la densidad, por eso el hielo flota. Esto permite la vida en los polos, ya que el hielo actúa como aislante.
El alto poder disolvente convierte al agua en el "disolvente universal", capaz de disolver gran cantidad de sustancias iónicas y polares.
Aplicación práctica: Estas propiedades explican por qué sudamos para refrescarnos (calor de vaporización) y por qué las plantas pueden transportar agua desde las raíces (capilaridad).

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Solubilidad y comportamiento de las sustancias en agua
Según su solubilidad en agua, las sustancias se clasifican en tres grupos importantes que debes conocer perfectamente.
Las sustancias hidrófilas (solubles) incluyen las iónicas como la sal (NaCl) y las covalentes polares como monosacáridos, aminoácidos y nucleótidos. Estas se disuelven fácilmente porque interaccionan bien con las moléculas de agua.
Las sustancias hidrófobas (insolubles) son covalentes apolares como los triglicéridos (grasas). No se disuelven porque no pueden formar puentes de hidrógeno con el agua.
Las sustancias anfipáticas tienen partes solubles y partes insolubles, y su comportamiento es fascinante. Pueden formar tres estructuras diferentes: monocapas en la superficie del agua (como el aceite), micelas esféricas con las partes insolubles hacia dentro (como el jabón limpiando), y bicapas que separan dos medios acuosos (como las membranas celulares).
Ejemplo cotidiano: Cuando lavas los platos con jabón, las micelas "atrapan" la grasa en su interior hidrófobo mientras su exterior hidrófilo se disuelve en el agua.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sales minerales y regulación del pH
Las sales minerales existen en dos formas en los seres vivos, cada una con funciones específicas que debes distinguir claramente.
Las sales precipitadas tienen función estructural y de protección. Los fosfatos y carbonatos de calcio forman nuestro esqueleto, el carbonato cálcico endurece caparazones de crustáceos, y la sílice da rigidez a esponjas y plantas.
Las sales ionizadas forman los fluidos corporales e incluyen cationes como Na⁺, K⁺, Ca²⁺ y aniones como Cl⁻, PO₄³⁻. Tienen funciones específicas: Na⁺ y K⁺ mantienen el potencial de membrana, varios iones actúan como cofactores enzimáticos.
La función homeostática más importante es la regulación del pH mediante sistemas tampón o buffer. El sistema bicarbonato actúa a nivel extracelular, mientras que el sistema fosfato funciona intracelularmente. Ambos mantienen el pH constante añadiendo o quitando protones (H⁺) según sea necesario.
Recuerda que pH bajo significa más ácido (más H⁺), mientras que pH alto significa más básico (menos H⁺).
Conexión vital: Sin estos sistemas tampón, pequeños cambios en la acidez podrían alterar la forma de las proteínas y detener procesos vitales.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sistemas tampón y procesos osmóticos
Los sistemas tampón funcionan como reguladores automáticos del pH en tu organismo. El tampón bicarbonato actúa principalmente en la sangre, mientras que el tampón fosfato funciona dentro de las células.
La ósmosis es el movimiento de agua a través de membranas semipermeables, desde la solución más diluida (hipotónica) hacia la más concentrada (hipertónica), hasta igualar concentraciones (isotónicas).
En células vegetales, la ósmosis crea tres estados: turgencia (célula hinchada en medio hipotónico), flacidez (equilibrio en medio isotónico), y plasmólisis (célula deshidratada en medio hipertónico). La pared celular rígida protege contra la rotura.
En células animales, sin pared protectora, los efectos son más dramáticos: lisis (rotura en medio hipotónico), estado normal (en medio isotónico), y crenación o retracción (en medio hipertónico).
Aplicación médica: Los sueros intravenosos deben ser isotónicos con la sangre para evitar dañar los glóbulos rojos por lisis o crenación.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Difusión y diálisis
La difusión y la diálisis son procesos de transporte pasivo fundamentales para el funcionamiento celular y tienen aplicaciones médicas importantes.
La difusión consiste en el movimiento de moléculas disueltas desde áreas de mayor concentración hacia áreas de menor concentración, hasta igualar las concentraciones. Es el concepto inverso a la ósmosis: aquí se mueven los solutos en lugar del agua.
Este proceso es fundamental para la respiración celular, ya que permite que el oxígeno entre en las células y el dióxido de carbono salga, siguiendo sus gradientes de concentración respectivos.
La diálisis es el paso de agua y partículas pequeñas (como sales minerales) a través de membranas que permiten este tránsito pero no el de macromoléculas. Este principio se utiliza en las máquinas de diálisis renal, donde se eliminan toxinas de la sangre cuando los riñones no funcionan correctamente.
Ambos procesos son pasivos, lo que significa que no requieren gasto energético por parte de la célula, aprovechando la energía cinética natural de las moléculas.
Aplicación médica: La diálisis renal salva vidas al reemplazar artificialmente una función vital de los riñones mediante estos principios físico-químicos básicos.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: elementos biológicos
9Apuntes de bioelementos y biomoléculas
Apuntes de bioelementos y biomoléculas
bioelementos agua y sales minerales
agua y sales minerales
bioelementos. Agua y sales
Tema de primero y segundo de bachillerato que habla acerca del agua y las sales minerales
biomoléculas y bioelementos
esquema de conceptos
BG: bloque 1 pt.1
Agua, ósmosis, sales minerales y bioelementos.
Tema 1 Biología
Biología tema 1: los bioelementos
Bioelementos, agua y sales minerales
Bioelementos, agua y sales minerales
Tema 1 - los bioelementos y biomoléculas
Trata lo que son los bioelementos y las biomoléculas y sus propiedades correspondientes
Los biolementos y biomoléculas
Bioelementos y biomoléculas
Contenidos más populares de Biología
9Replicación, transcripción y traducción
Esquema del tema de flujo de información genética del bloque de Biología Molecular
Fotosíntesis
Conceptos básicos y reacciones químicas que se producen
Descubriendo la vida: Flashcards de Biología
Aprende sobre los fundamentos de la biología con esta colección de flashcards interactivos. ¡Explora los conceptos clave y amplía tus conocimientos sobre la vida en este emocionante viaje de aprendizaje!
GENÉTICA MOLECULAR
Genética molecular 2 bachillerato y PAU
Catabolismo y anabolismo
Apuntes “esquematizados” con imágenes y visual
Anabolismo y Catabolismo
amabolismo y catabolismo
Metabolismo
Apuntes de metabolismo de segundo de bachillerato (biología). También recomiendo acompañar el estudio de este tema con el esquema que he subido para entenderlo mejor.
METABOLISMO CELULAR (CATABOLISMO + ANABOLISMO)
Apuntes completos de catabolismo y anabolismo de 2 bach
las plantas 🌳🌿
el reino de las plantas
Contenidos más populares
9Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
QUIZZ VIDA DIARIA#1
QUIZZ sobre tu vida diaria, psicológico para mejorar el estudio.:] [ Cualquier pregunta, la responderé ]^^
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.