La termoquímica y cinética son fundamentales para entender cómo y... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
251
•
Actualizado May 12, 2026
•
Ariadna Queupumil Alarza
@ariadna.q4
La termoquímica y cinética son fundamentales para entender cómo y... Mostrar más







¿Te has preguntado por qué algunas reacciones liberan calor y otras lo absorben? La termoquímica estudia los intercambios de energía en las reacciones químicas, mientras que la cinética analiza qué tan rápido ocurren.
Estos conceptos te ayudarán a predecir si una reacción será espontánea y a controlar su velocidad. Son la base para entender todo, desde la combustión del gas hasta el funcionamiento de las baterías.
💡 Dato curioso: La velocidad de una reacción puede cambiar millones de veces solo ajustando la temperatura o añadiendo un catalizador.
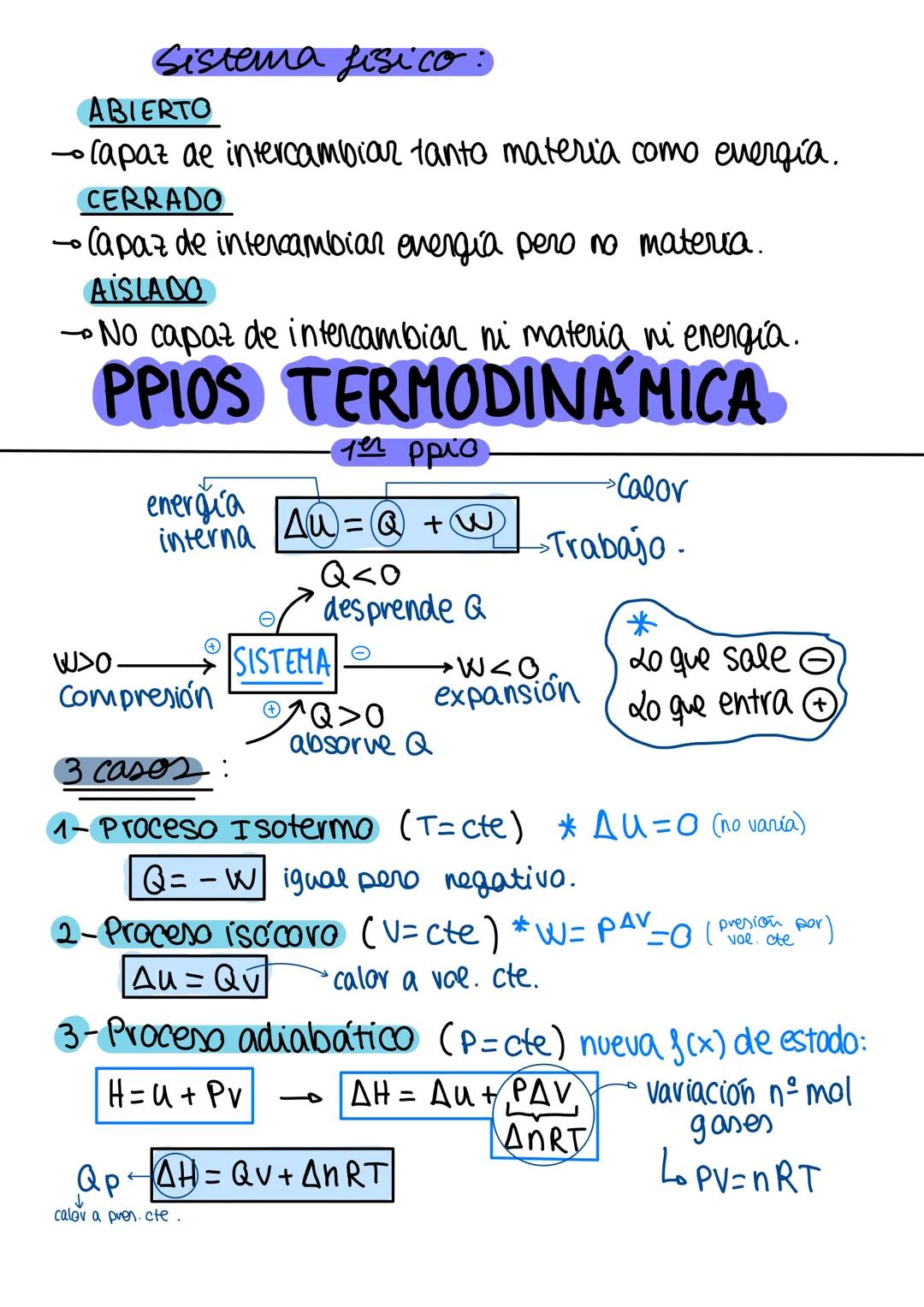
Los sistemas físicos se clasifican según qué pueden intercambiar con el entorno. Un sistema abierto intercambia materia y energía (como una olla sin tapa), uno cerrado solo energía (olla con tapa), y uno aislado no intercambia nada (termo perfecto).
El primer principio dice que la energía se conserva: ΔU = Q + W. Aquí Q es calor (positivo si se absorbe) y W es trabajo (positivo en compresión).
Hay tres procesos clave: isotermo , isócoro e isobárico (presión constante, donde aparece la entalpía H).
💡 Recuerda: En procesos isobáricos usamos entalpía (H) porque es más práctica que la energía interna (U).

Las reacciones endotérmicas (ΔH > 0) absorben calor y las exotérmicas (ΔH < 0) lo liberan. Los diagramas entálpicos muestran esto gráficamente: si los productos están más arriba que los reactivos, es endotérmica.
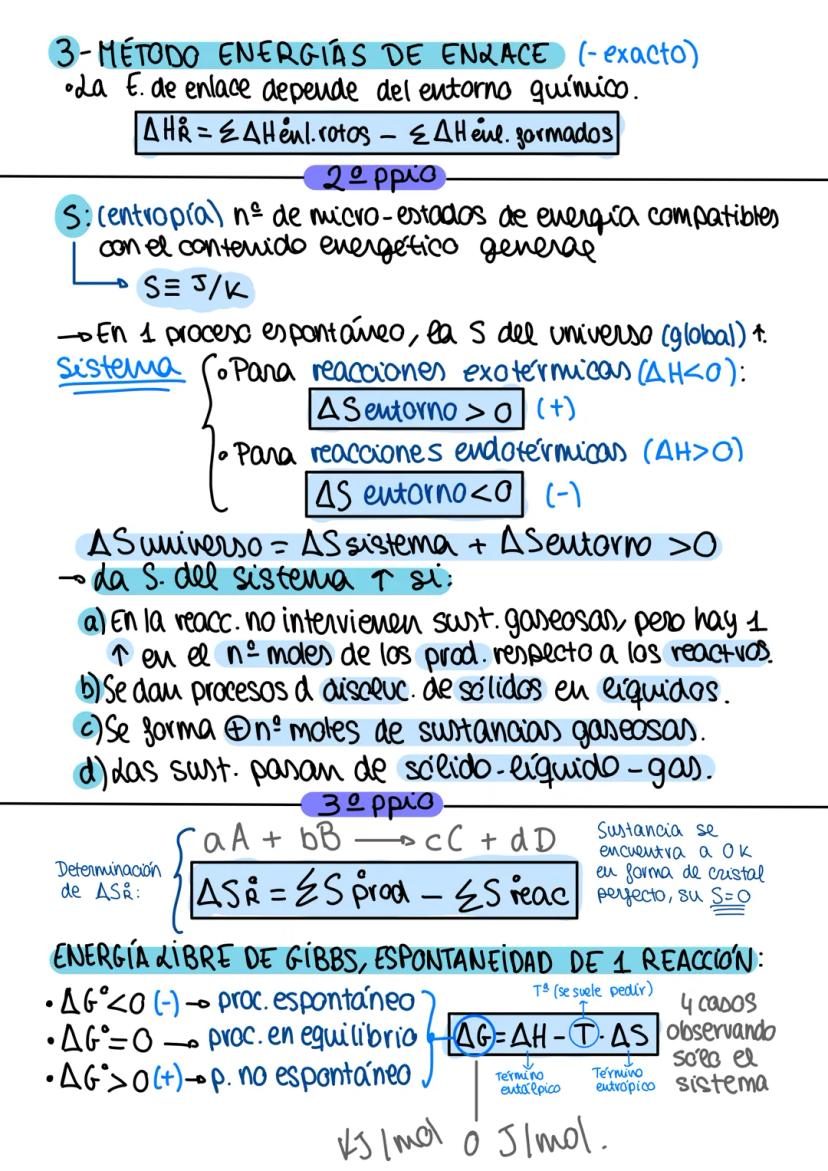
Para calcular entalpías tienes tres métodos principales. El método de formación usa: ΔH°R = ΣΔH°f(productos) - ΣΔH°f(reactivos). Los elementos en estado estándar tienen entalpía de formación cero.
La ley de Hess permite combinar reacciones conocidas para encontrar entalpías desconocidas. El método de energías de enlace usa: ΔHR = ΣΔHenlaces rotos - ΣΔHenlaces formados.
💡 Truco: Para aplicar Hess, suma las reacciones como ecuaciones algebraicas y las entalpías también se suman.
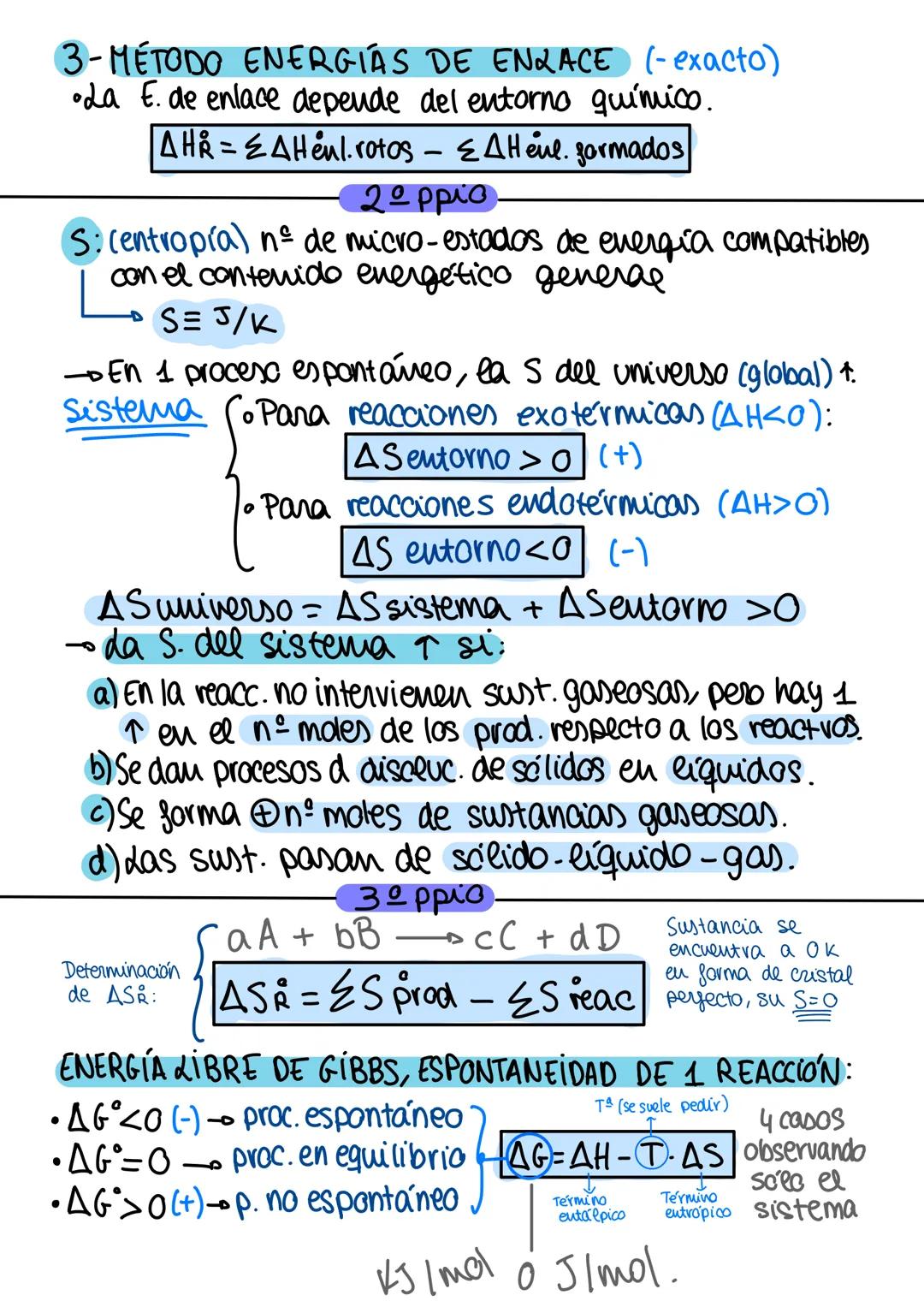
La entropía (S) mide el desorden del sistema. En procesos espontáneos, la entropía del universo siempre aumenta. La entropía aumenta cuando: hay más moles de gases en productos, se disuelven sólidos, o las sustancias cambian de sólido→líquido→gas.
El tercer principio establece que la entropía de un cristal perfecto a 0 K es cero. Para calcular: ΔS°R = ΣS°productos - ΣS°reactivos.
La energía libre de Gibbs determina la espontaneidad: ΔG = ΔH - TΔS. Si ΔG < 0, el proceso es espontáneo; si ΔG = 0, está en equilibrio; si ΔG > 0, no es espontáneo.
💡 Clave: La temperatura puede cambiar la espontaneidad de una reacción según los signos de ΔH y ΔS.
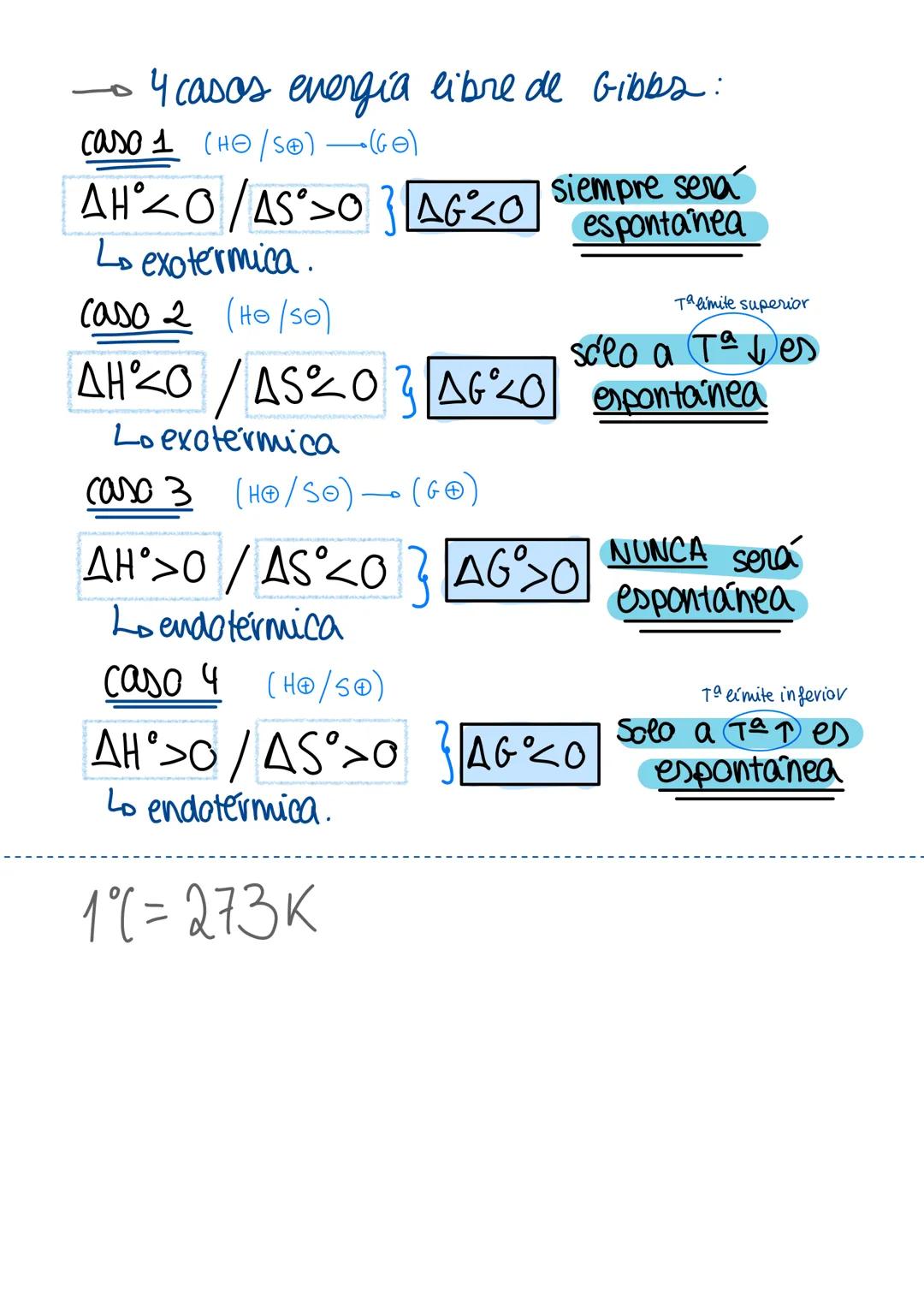
Dependiendo de los signos de ΔH y ΔS, hay cuatro situaciones posibles. Caso 1 (ΔH < 0, ΔS > 0): siempre espontánea a cualquier temperatura. Caso 2 (ΔH < 0, ΔS < 0): espontánea solo a temperaturas bajas.
Caso 3 (ΔH > 0, ΔS > 0): espontánea solo a temperaturas altas. Caso 4 (ΔH > 0, ΔS < 0): nunca espontánea a ninguna temperatura.
La temperatura límite se calcula cuando ΔG = 0, es decir: T = ΔH/ΔS. Por encima o debajo de esta temperatura cambia la espontaneidad.
💡 Memoriza: Exotérmica + entropía favorable = siempre espontánea. Endotérmica + entropía desfavorable = nunca espontánea.
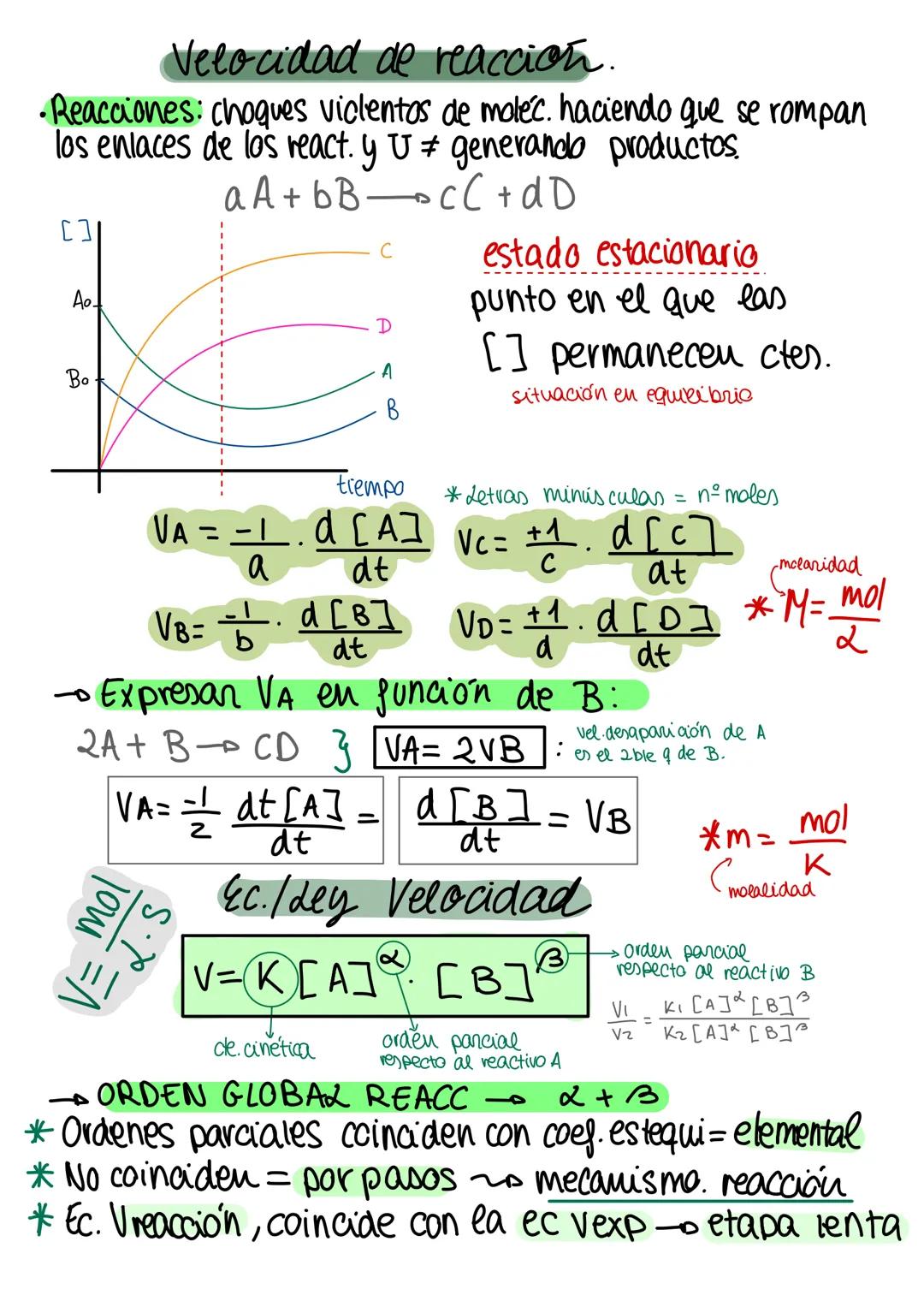
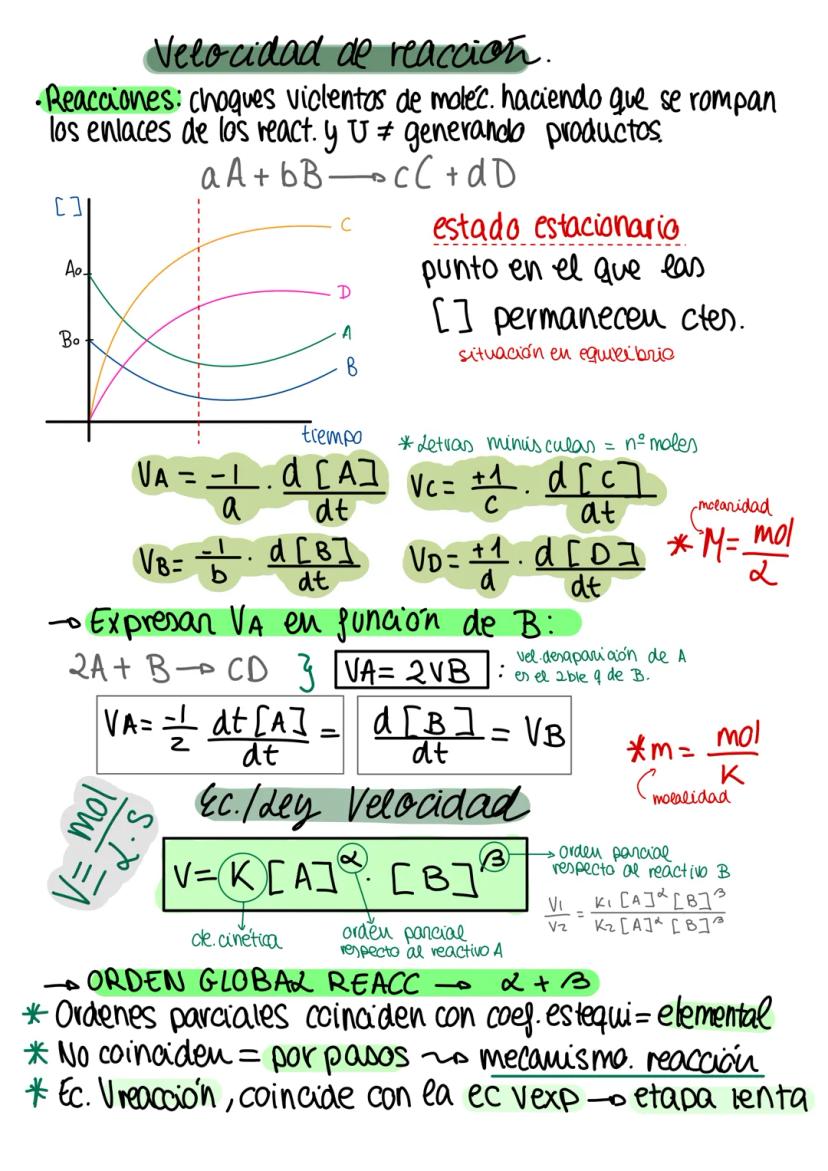
Las reacciones ocurren por choques eficaces entre moléculas que rompen enlaces y forman productos. La velocidad se define como el cambio de concentración por unidad de tiempo, ajustada por los coeficientes estequiométricos.
La ecuación de velocidad tiene la forma: v = k[A]^m[B]^n, donde k es la constante cinética, m y n son los órdenes parciales. El orden global es m + n.
Cuando los órdenes coinciden con los coeficientes estequiométricos, la reacción es elemental. Si no coinciden, la reacción ocurre por pasos y la ecuación corresponde a la etapa lenta.
💡 Importante: Los órdenes de reacción se determinan experimentalmente, no se pueden predecir desde la ecuación química.

Para cada orden de reacción hay ecuaciones integradas específicas. Orden 0: [A] = [A]₀ - kt. Orden 1: ln[A] = ln[A]₀ - kt. Orden 2: 1/[A] = 1/[A]₀ + kt.
El tiempo de vida media es cuando la concentración se reduce a la mitad. Para orden 1: t₁/₂ = ln2/k (independiente de concentración inicial).
Los mecanismos de reacción son secuencias de etapas elementales. La molecularidad es el número de moléculas que participan en una etapa elemental. El mecanismo más probable es aquel cuya etapa lenta coincide con la ley de velocidad experimental.
💡 Diferencia clave: Orden se determina experimentalmente; molecularidad se cuenta en la ecuación de cada etapa elemental.

La teoría de colisiones dice que las moléculas necesitan energía de activación (Ea) para reaccionar. Solo las moléculas activadas con suficiente energía y orientación correcta producen choques eficientes.
La teoría del estado de transición propone que se forma un complejo activado inestable donde los enlaces se están rompiendo y formando simultáneamente. Este complejo evoluciona hacia productos.
En el diagrama energético, la diferencia entre Ea directa y Ea inversa da el ΔH de reacción. Las reacciones exotérmicas tienen Ea directa mayor que la inversa.
💡 Visualiza: Imagina el complejo activado como el punto más alto de una montaña entre reactivos y productos.
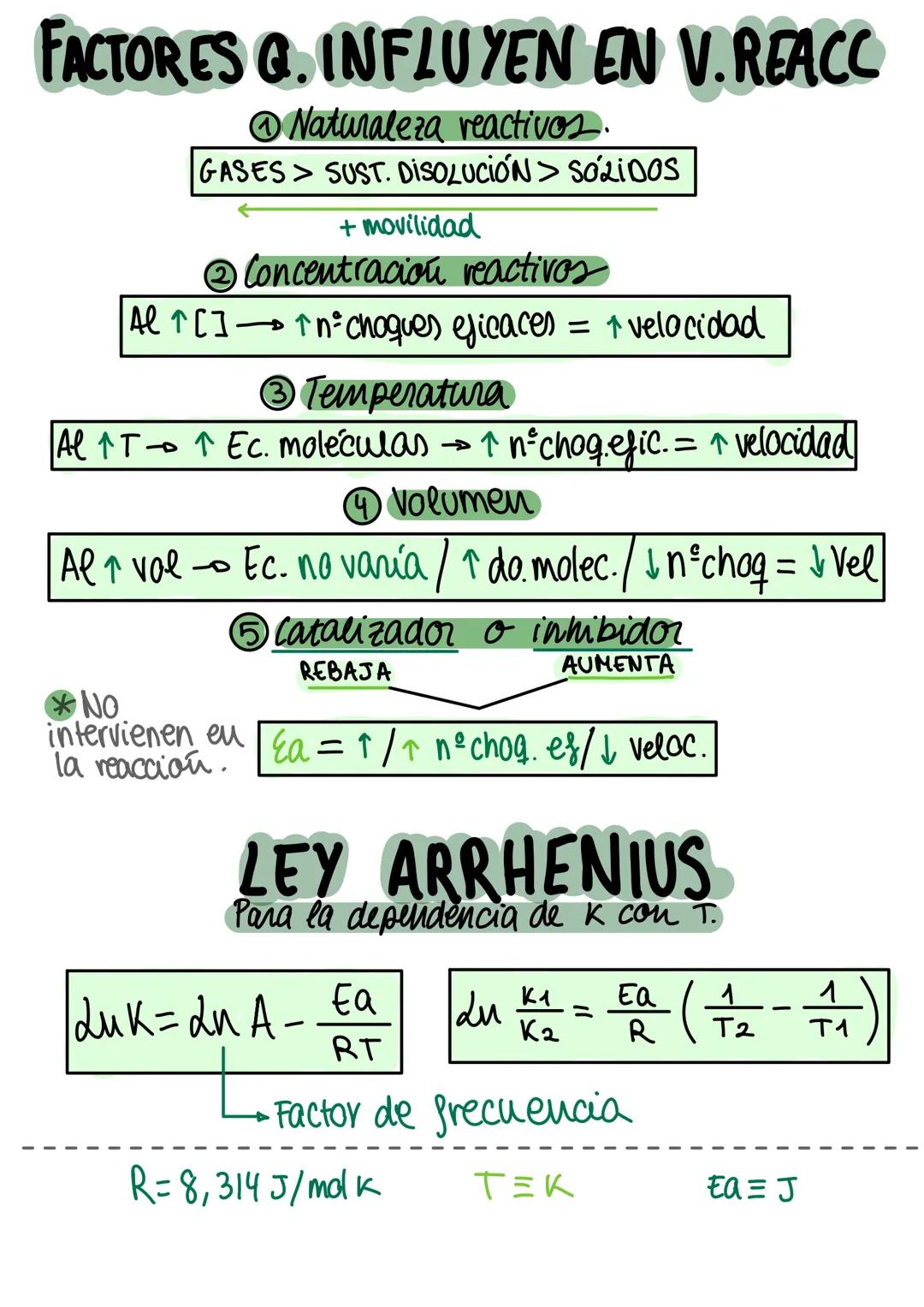
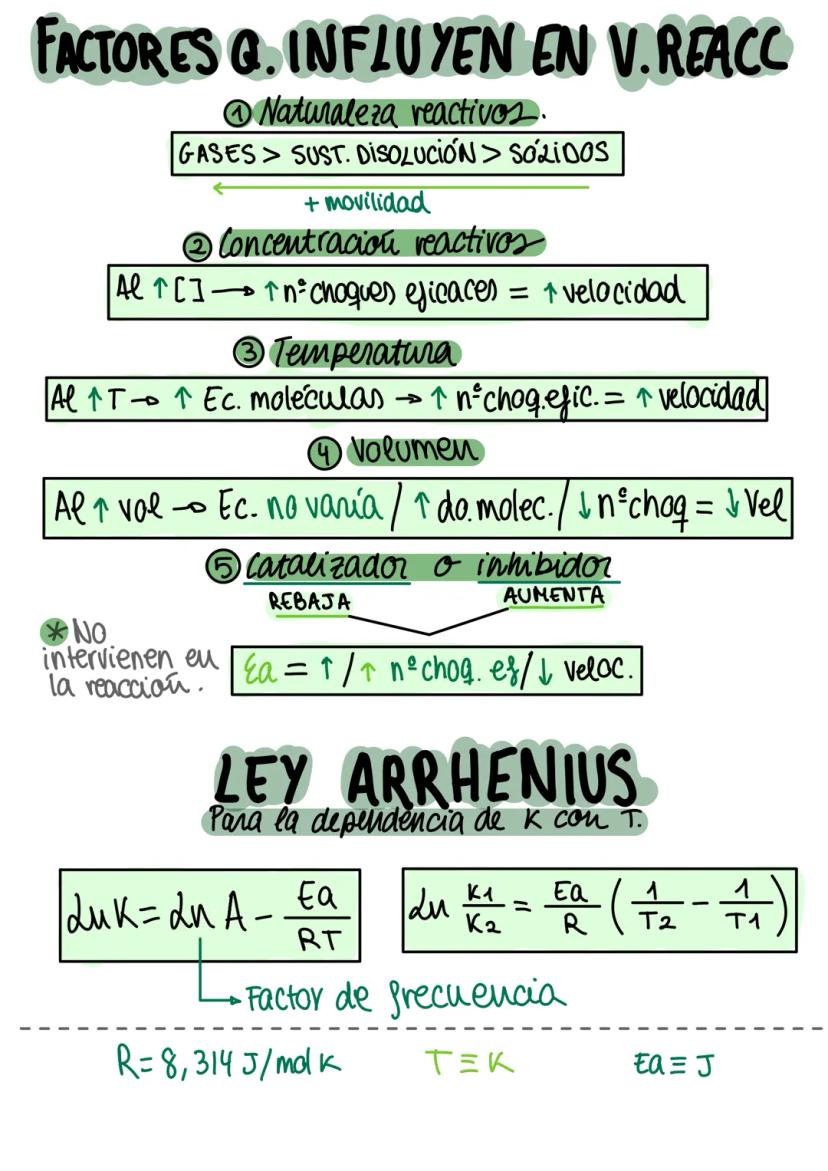
Cinco factores principales controlan la velocidad. La naturaleza de reactivos: gases > disoluciones > sólidos por mayor movilidad molecular. La concentración: más concentración = más choques eficaces.
La temperatura aumenta la energía cinética y el número de choques eficaces. El volumen tiene efecto inverso: mayor volumen = menor densidad = menos choques.
Los catalizadores disminuyen la Ea sin consumirse, mientras los inhibidores la aumentan. La ecuación de Arrhenius relaciona la constante k con la temperatura: ln = .
💡 Regla práctica: Aumentar 10°C la temperatura suele duplicar o triplicar la velocidad de reacción.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
Ariadna Queupumil Alarza
@ariadna.q4
La termoquímica y cinética son fundamentales para entender cómo y por qué ocurren las reacciones químicas. Aquí descubrirás desde los principios de la termodinámica hasta los factores que controlan la velocidad de las reacciones.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Te has preguntado por qué algunas reacciones liberan calor y otras lo absorben? La termoquímica estudia los intercambios de energía en las reacciones químicas, mientras que la cinética analiza qué tan rápido ocurren.
Estos conceptos te ayudarán a predecir si una reacción será espontánea y a controlar su velocidad. Son la base para entender todo, desde la combustión del gas hasta el funcionamiento de las baterías.
💡 Dato curioso: La velocidad de una reacción puede cambiar millones de veces solo ajustando la temperatura o añadiendo un catalizador.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los sistemas físicos se clasifican según qué pueden intercambiar con el entorno. Un sistema abierto intercambia materia y energía (como una olla sin tapa), uno cerrado solo energía (olla con tapa), y uno aislado no intercambia nada (termo perfecto).
El primer principio dice que la energía se conserva: ΔU = Q + W. Aquí Q es calor (positivo si se absorbe) y W es trabajo (positivo en compresión).
Hay tres procesos clave: isotermo , isócoro e isobárico (presión constante, donde aparece la entalpía H).
💡 Recuerda: En procesos isobáricos usamos entalpía (H) porque es más práctica que la energía interna (U).

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las reacciones endotérmicas (ΔH > 0) absorben calor y las exotérmicas (ΔH < 0) lo liberan. Los diagramas entálpicos muestran esto gráficamente: si los productos están más arriba que los reactivos, es endotérmica.
Para calcular entalpías tienes tres métodos principales. El método de formación usa: ΔH°R = ΣΔH°f(productos) - ΣΔH°f(reactivos). Los elementos en estado estándar tienen entalpía de formación cero.
La ley de Hess permite combinar reacciones conocidas para encontrar entalpías desconocidas. El método de energías de enlace usa: ΔHR = ΣΔHenlaces rotos - ΣΔHenlaces formados.
💡 Truco: Para aplicar Hess, suma las reacciones como ecuaciones algebraicas y las entalpías también se suman.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La entropía (S) mide el desorden del sistema. En procesos espontáneos, la entropía del universo siempre aumenta. La entropía aumenta cuando: hay más moles de gases en productos, se disuelven sólidos, o las sustancias cambian de sólido→líquido→gas.
El tercer principio establece que la entropía de un cristal perfecto a 0 K es cero. Para calcular: ΔS°R = ΣS°productos - ΣS°reactivos.
La energía libre de Gibbs determina la espontaneidad: ΔG = ΔH - TΔS. Si ΔG < 0, el proceso es espontáneo; si ΔG = 0, está en equilibrio; si ΔG > 0, no es espontáneo.
💡 Clave: La temperatura puede cambiar la espontaneidad de una reacción según los signos de ΔH y ΔS.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Dependiendo de los signos de ΔH y ΔS, hay cuatro situaciones posibles. Caso 1 (ΔH < 0, ΔS > 0): siempre espontánea a cualquier temperatura. Caso 2 (ΔH < 0, ΔS < 0): espontánea solo a temperaturas bajas.
Caso 3 (ΔH > 0, ΔS > 0): espontánea solo a temperaturas altas. Caso 4 (ΔH > 0, ΔS < 0): nunca espontánea a ninguna temperatura.
La temperatura límite se calcula cuando ΔG = 0, es decir: T = ΔH/ΔS. Por encima o debajo de esta temperatura cambia la espontaneidad.
💡 Memoriza: Exotérmica + entropía favorable = siempre espontánea. Endotérmica + entropía desfavorable = nunca espontánea.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las reacciones ocurren por choques eficaces entre moléculas que rompen enlaces y forman productos. La velocidad se define como el cambio de concentración por unidad de tiempo, ajustada por los coeficientes estequiométricos.
La ecuación de velocidad tiene la forma: v = k[A]^m[B]^n, donde k es la constante cinética, m y n son los órdenes parciales. El orden global es m + n.
Cuando los órdenes coinciden con los coeficientes estequiométricos, la reacción es elemental. Si no coinciden, la reacción ocurre por pasos y la ecuación corresponde a la etapa lenta.
💡 Importante: Los órdenes de reacción se determinan experimentalmente, no se pueden predecir desde la ecuación química.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Para cada orden de reacción hay ecuaciones integradas específicas. Orden 0: [A] = [A]₀ - kt. Orden 1: ln[A] = ln[A]₀ - kt. Orden 2: 1/[A] = 1/[A]₀ + kt.
El tiempo de vida media es cuando la concentración se reduce a la mitad. Para orden 1: t₁/₂ = ln2/k (independiente de concentración inicial).
Los mecanismos de reacción son secuencias de etapas elementales. La molecularidad es el número de moléculas que participan en una etapa elemental. El mecanismo más probable es aquel cuya etapa lenta coincide con la ley de velocidad experimental.
💡 Diferencia clave: Orden se determina experimentalmente; molecularidad se cuenta en la ecuación de cada etapa elemental.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La teoría de colisiones dice que las moléculas necesitan energía de activación (Ea) para reaccionar. Solo las moléculas activadas con suficiente energía y orientación correcta producen choques eficientes.
La teoría del estado de transición propone que se forma un complejo activado inestable donde los enlaces se están rompiendo y formando simultáneamente. Este complejo evoluciona hacia productos.
En el diagrama energético, la diferencia entre Ea directa y Ea inversa da el ΔH de reacción. Las reacciones exotérmicas tienen Ea directa mayor que la inversa.
💡 Visualiza: Imagina el complejo activado como el punto más alto de una montaña entre reactivos y productos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Cinco factores principales controlan la velocidad. La naturaleza de reactivos: gases > disoluciones > sólidos por mayor movilidad molecular. La concentración: más concentración = más choques eficaces.
La temperatura aumenta la energía cinética y el número de choques eficaces. El volumen tiene efecto inverso: mayor volumen = menor densidad = menos choques.
Los catalizadores disminuyen la Ea sin consumirse, mientras los inhibidores la aumentan. La ecuación de Arrhenius relaciona la constante k con la temperatura: ln = .
💡 Regla práctica: Aumentar 10°C la temperatura suele duplicar o triplicar la velocidad de reacción.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
8
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS