El sistema periódico es como el mapa de ruta de... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
145
•
Actualizado May 5, 2026
•
Andrea PB
@andreapb_amng
El sistema periódico es como el mapa de ruta de... Mostrar más

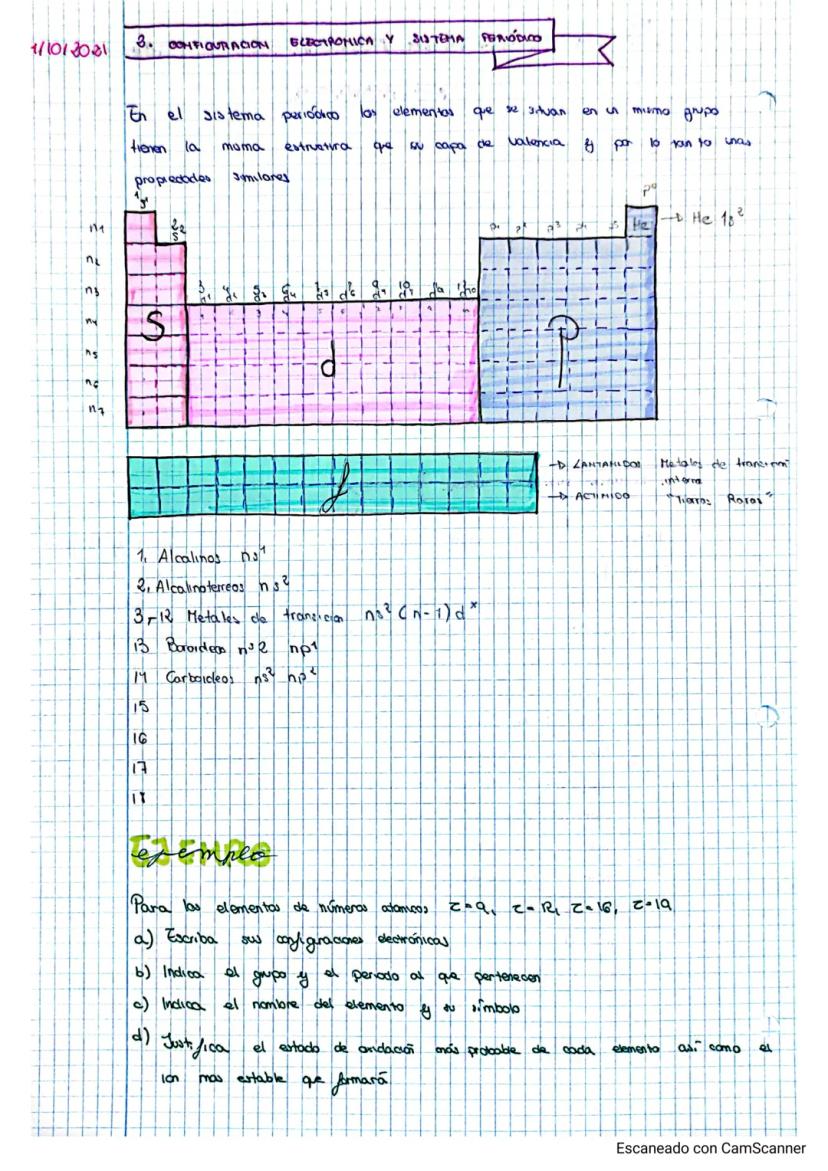






¿Sabías que la tabla periódica es básicamente como un código secreto que los químicos usan para entender todos los elementos? Está organizada en 7 periodos (las filas horizontales) y 18 grupos (las columnas verticales), y cada elemento está colocado según su número atómico creciente.
Lo genial es que los elementos del mismo grupo son como hermanos químicos: tienen propiedades muy parecidas porque comparten la misma estructura de la capa de valencia. Por ejemplo, todos los del grupo 1 son metales alcalinos súper reactivos.
Los grupos más importantes que debes conocer son: alcalinos (grupo 1), alcalinotérreos (grupo 2), metales de transición , halógenos (grupo 17) y gases nobles (grupo 18). Cada uno tiene su personalidad química única.
¡Ojo! Si memorizas las familias de elementos, podrás predecir muchas propiedades sin necesidad de buscarlas.
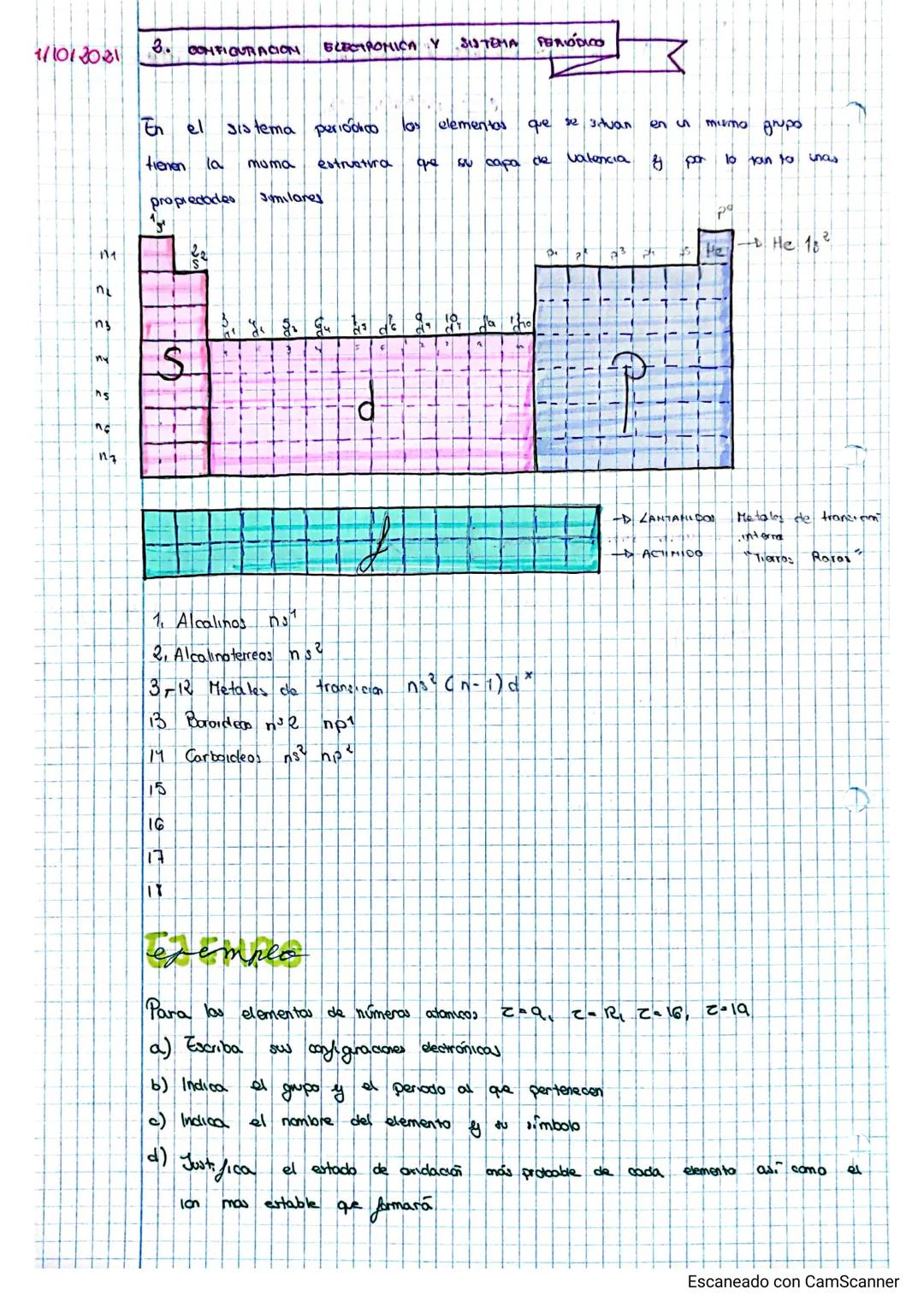
La configuración electrónica es la clave para entender por qué los elementos se comportan como lo hacen. Los elementos del mismo grupo tienen exactamente la misma configuración en su capa de valencia, y por eso actúan de forma similar.
Cada tipo de orbital (s, p, d, f) corresponde a una zona específica de la tabla periódica. Los grupos 1 y 2 terminan en orbitales s, los grupos 13-18 en orbitales p, y los metales de transición en orbitales d.
Para resolver problemas, sigue estos pasos: escribe la configuración electrónica, identifica la capa de valencia, determina el grupo y periodo, y finalmente predice el estado de oxidación más probable. Los elementos tienden a ganar o perder electrones para conseguir configuración de gas noble.
Truco de examen: El periodo siempre coincide con el nivel energético más alto en la configuración electrónica.

La energía de ionización es la energía que necesitas para "robarle" un electrón a un átomo neutro. Siempre es positiva porque tienes que aportar energía para vencer la atracción del núcleo.
Esta propiedad está súper relacionada con el radio atómico: cuanto más grande es el átomo, más lejos están los electrones del núcleo y más fácil es arrancarlos. Por eso la energía de ionización disminuye hacia abajo en un grupo y aumenta hacia la derecha en un periodo.
Las energías de ionización sucesivas van aumentando: 1ªEI < 2ªEI < 3ªEI... Cuando ves un salto gigante entre dos energías consecutivas, significa que el átomo ya tenía configuración estable después de perder el electrón anterior.
Fundamental: Siempre justifica las variaciones de energía de ionización en función del radio atómico.

La afinidad electrónica mide la tendencia de un átomo a "aceptar" un electrón extra. Puede ser positiva o negativa, dependiendo de si el átomo realmente quiere ese electrón. Aumenta hacia la derecha en un periodo y hacia arriba en un grupo.
La electronegatividad es súper importante para entender los enlaces. Mide cuánto "tira" un átomo de los electrones cuando forma enlaces covalentes. El flúor es el más "egoísta" con un valor de 4 en la escala de Pauling.
Ambas propiedades siguen la misma tendencia: aumentan hacia la derecha y hacia arriba en la tabla periódica. Esto se debe a que los átomos más pequeños con más protones atraen más fuertemente a los electrones.
Dato clave: Si la diferencia de electronegatividad entre dos átomos es grande, el enlace será polar.

Cuando te pidan analizar elementos por su número atómico, sigue este método ordenado: primero escribe la configuración electrónica, luego identifica el grupo y periodo, nombra el elemento y finalmente determina su estado de oxidación más probable.
Los estados de oxidación dependen de cuántos electrones debe ganar o perder el átomo para conseguir configuración de gas noble. Los metales tienden a perder electrones (estados positivos) y los no metales a ganarlos (estados negativos).
Por ejemplo, el flúor con configuración 1s² 2s² 2p⁵ necesita ganar un electrón para completar su octeto, así que su estado de oxidación típico es -1. El magnesio con 1s² 2s² 2p⁶ 3s² pierde fácilmente 2 electrones, dando Mg²⁺.
Estrategia de examen: Identifica primero si el elemento es metal o no metal para predecir si ganará o perderá electrones.

El radio atómico es básicamente el "tamaño" del átomo, y varía de forma muy predecible en la tabla periódica. Aumenta hacia abajo (más capas electrónicas) y disminuye hacia la derecha (más protones atraen más fuerte).
El radio iónico es diferente del atómico. Los cationes (iones positivos) son más pequeños que sus átomos neutros porque han perdido electrones y el núcleo atrae más fuerte. Los aniones (iones negativos) son más grandes porque tienen electrones extra que se repelen.
Cuando varios iones son isoelectrónicos (mismo número de electrones), el que tenga más protones será más pequeño. Es como si tuvieras la misma cantidad de pelotas (electrones) pero con imanes de diferente fuerza (protones) atrayéndolas.
Regla de oro: Siempre compara primero el número de capas electrónicas; el que tenga más capas será siempre más grande.

El carácter metálico está directamente relacionado con la facilidad para perder electrones. Cuanto menor sea la energía de ionización, más metálico será el elemento. Los metales del grupo 1 son los campeones en esto.
Cuando compares elementos, recuerda que el carácter metálico aumenta hacia abajo y hacia la izquierda en la tabla periódica. Es exactamente lo contrario que la electronegatividad.
En los problemas de energías de ionización sucesivas, fíjate en los saltos gigantes de energía. Un salto muy grande indica que el ion ya tiene configuración estable y arrancar otro electrón cuesta muchísimo más.
Tip para exámenes: Si ves una diferencia de energía de ionización mayor a 3000-4000 kJ/mol, probablemente el átomo ya alcanzó configuración de gas noble.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
Andrea PB
@andreapb_amng
El sistema periódico es como el mapa de ruta de la química que te permite predecir las propiedades de los elementos. Con solo saber la posición de un elemento, puedes averiguar cómo se comporta, qué tamaño tiene y cómo reaccionará... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Sabías que la tabla periódica es básicamente como un código secreto que los químicos usan para entender todos los elementos? Está organizada en 7 periodos (las filas horizontales) y 18 grupos (las columnas verticales), y cada elemento está colocado según su número atómico creciente.
Lo genial es que los elementos del mismo grupo son como hermanos químicos: tienen propiedades muy parecidas porque comparten la misma estructura de la capa de valencia. Por ejemplo, todos los del grupo 1 son metales alcalinos súper reactivos.
Los grupos más importantes que debes conocer son: alcalinos (grupo 1), alcalinotérreos (grupo 2), metales de transición , halógenos (grupo 17) y gases nobles (grupo 18). Cada uno tiene su personalidad química única.
¡Ojo! Si memorizas las familias de elementos, podrás predecir muchas propiedades sin necesidad de buscarlas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La configuración electrónica es la clave para entender por qué los elementos se comportan como lo hacen. Los elementos del mismo grupo tienen exactamente la misma configuración en su capa de valencia, y por eso actúan de forma similar.
Cada tipo de orbital (s, p, d, f) corresponde a una zona específica de la tabla periódica. Los grupos 1 y 2 terminan en orbitales s, los grupos 13-18 en orbitales p, y los metales de transición en orbitales d.
Para resolver problemas, sigue estos pasos: escribe la configuración electrónica, identifica la capa de valencia, determina el grupo y periodo, y finalmente predice el estado de oxidación más probable. Los elementos tienden a ganar o perder electrones para conseguir configuración de gas noble.
Truco de examen: El periodo siempre coincide con el nivel energético más alto en la configuración electrónica.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La energía de ionización es la energía que necesitas para "robarle" un electrón a un átomo neutro. Siempre es positiva porque tienes que aportar energía para vencer la atracción del núcleo.
Esta propiedad está súper relacionada con el radio atómico: cuanto más grande es el átomo, más lejos están los electrones del núcleo y más fácil es arrancarlos. Por eso la energía de ionización disminuye hacia abajo en un grupo y aumenta hacia la derecha en un periodo.
Las energías de ionización sucesivas van aumentando: 1ªEI < 2ªEI < 3ªEI... Cuando ves un salto gigante entre dos energías consecutivas, significa que el átomo ya tenía configuración estable después de perder el electrón anterior.
Fundamental: Siempre justifica las variaciones de energía de ionización en función del radio atómico.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La afinidad electrónica mide la tendencia de un átomo a "aceptar" un electrón extra. Puede ser positiva o negativa, dependiendo de si el átomo realmente quiere ese electrón. Aumenta hacia la derecha en un periodo y hacia arriba en un grupo.
La electronegatividad es súper importante para entender los enlaces. Mide cuánto "tira" un átomo de los electrones cuando forma enlaces covalentes. El flúor es el más "egoísta" con un valor de 4 en la escala de Pauling.
Ambas propiedades siguen la misma tendencia: aumentan hacia la derecha y hacia arriba en la tabla periódica. Esto se debe a que los átomos más pequeños con más protones atraen más fuertemente a los electrones.
Dato clave: Si la diferencia de electronegatividad entre dos átomos es grande, el enlace será polar.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Cuando te pidan analizar elementos por su número atómico, sigue este método ordenado: primero escribe la configuración electrónica, luego identifica el grupo y periodo, nombra el elemento y finalmente determina su estado de oxidación más probable.
Los estados de oxidación dependen de cuántos electrones debe ganar o perder el átomo para conseguir configuración de gas noble. Los metales tienden a perder electrones (estados positivos) y los no metales a ganarlos (estados negativos).
Por ejemplo, el flúor con configuración 1s² 2s² 2p⁵ necesita ganar un electrón para completar su octeto, así que su estado de oxidación típico es -1. El magnesio con 1s² 2s² 2p⁶ 3s² pierde fácilmente 2 electrones, dando Mg²⁺.
Estrategia de examen: Identifica primero si el elemento es metal o no metal para predecir si ganará o perderá electrones.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El radio atómico es básicamente el "tamaño" del átomo, y varía de forma muy predecible en la tabla periódica. Aumenta hacia abajo (más capas electrónicas) y disminuye hacia la derecha (más protones atraen más fuerte).
El radio iónico es diferente del atómico. Los cationes (iones positivos) son más pequeños que sus átomos neutros porque han perdido electrones y el núcleo atrae más fuerte. Los aniones (iones negativos) son más grandes porque tienen electrones extra que se repelen.
Cuando varios iones son isoelectrónicos (mismo número de electrones), el que tenga más protones será más pequeño. Es como si tuvieras la misma cantidad de pelotas (electrones) pero con imanes de diferente fuerza (protones) atrayéndolas.
Regla de oro: Siempre compara primero el número de capas electrónicas; el que tenga más capas será siempre más grande.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El carácter metálico está directamente relacionado con la facilidad para perder electrones. Cuanto menor sea la energía de ionización, más metálico será el elemento. Los metales del grupo 1 son los campeones en esto.
Cuando compares elementos, recuerda que el carácter metálico aumenta hacia abajo y hacia la izquierda en la tabla periódica. Es exactamente lo contrario que la electronegatividad.
En los problemas de energías de ionización sucesivas, fíjate en los saltos gigantes de energía. Un salto muy grande indica que el ion ya tiene configuración estable y arrancar otro electrón cuesta muchísimo más.
Tip para exámenes: Si ves una diferencia de energía de ionización mayor a 3000-4000 kJ/mol, probablemente el átomo ya alcanzó configuración de gas noble.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
3
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
Resumen de la parte teórica del tema Sistema Periódico de química (2º Bachillerato).
Resumen de los primeros descubrimientos del siglo XIX en química y los modelos atómicos propuestos por Thomson y Rutherford.
Tabla de Mendeléiev, la tabla actual, propiedades periódicas...
Propiedades periódicas
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS