¿Alguna vez te has preguntado cómo llegamos a entender la... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
196
•
Actualizado May 12, 2026
•
Gabriela Alejandra Madrigal Pérez
@gabrielaa_1zta3
¿Alguna vez te has preguntado cómo llegamos a entender la... Mostrar más
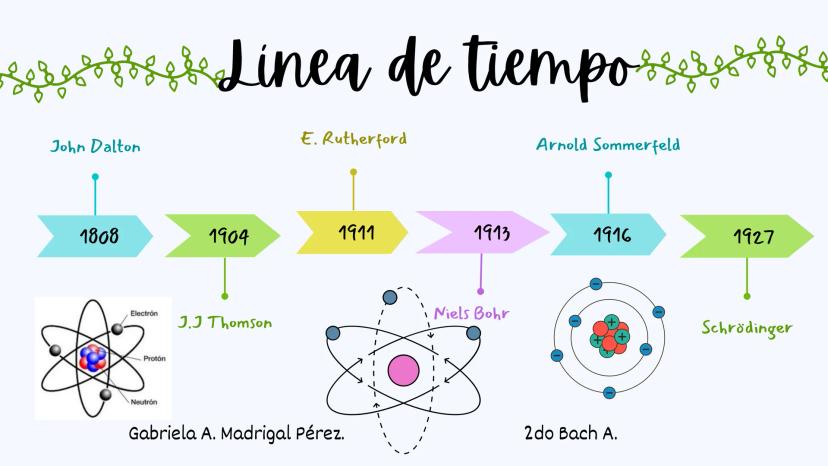
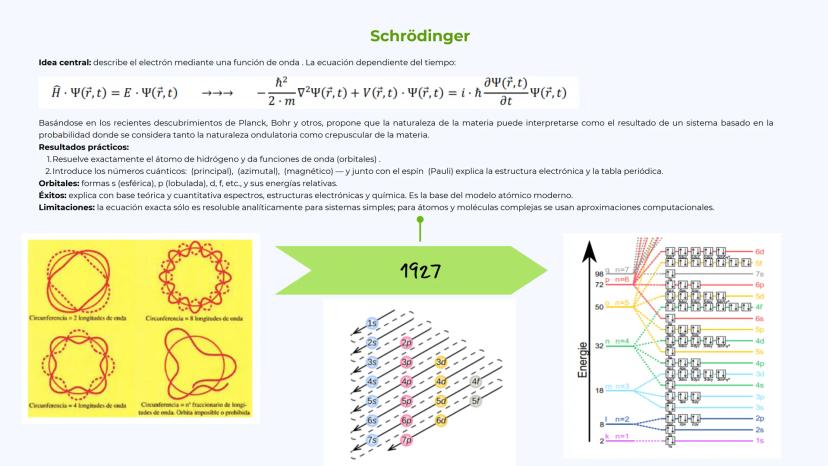
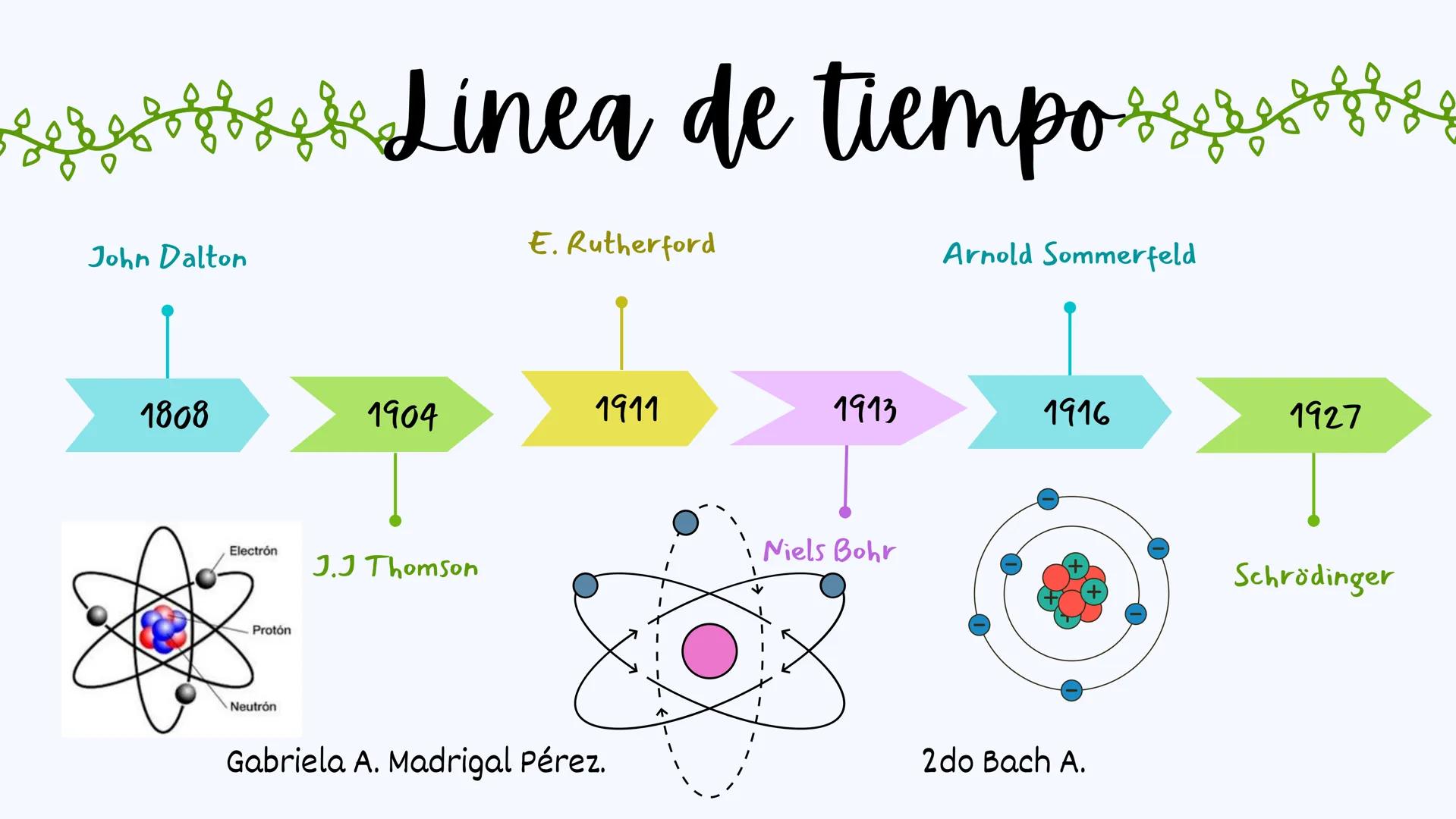
La evolución del modelo atómico es una de las historias más fascinantes de la ciencia. Desde 1808 hasta 1927, diferentes científicos fueron construyendo pieza a pieza nuestra comprensión actual del átomo.
Todo empezó con John Dalton en 1808, que imaginó los átomos como pequeñas esferas sólidas. Luego vinieron J.J. Thomson (1904), Ernest Rutherford (1911), Niels Bohr (1913), Arnold Sommerfeld (1916) y finalmente Schrödinger (1927), cada uno añadiendo nuevas piezas al puzzle.
Durante este período también se descubrieron las partículas subatómicas: primero el electrón, después el protón y más tarde el neutrón. Cada descubrimiento obligó a los científicos a repensar completamente sus ideas anteriores.
💡 Dato curioso: Cada modelo no "reemplazaba" completamente al anterior, sino que explicaba cosas que el anterior no podía explicar. ¡La ciencia es así de genial!
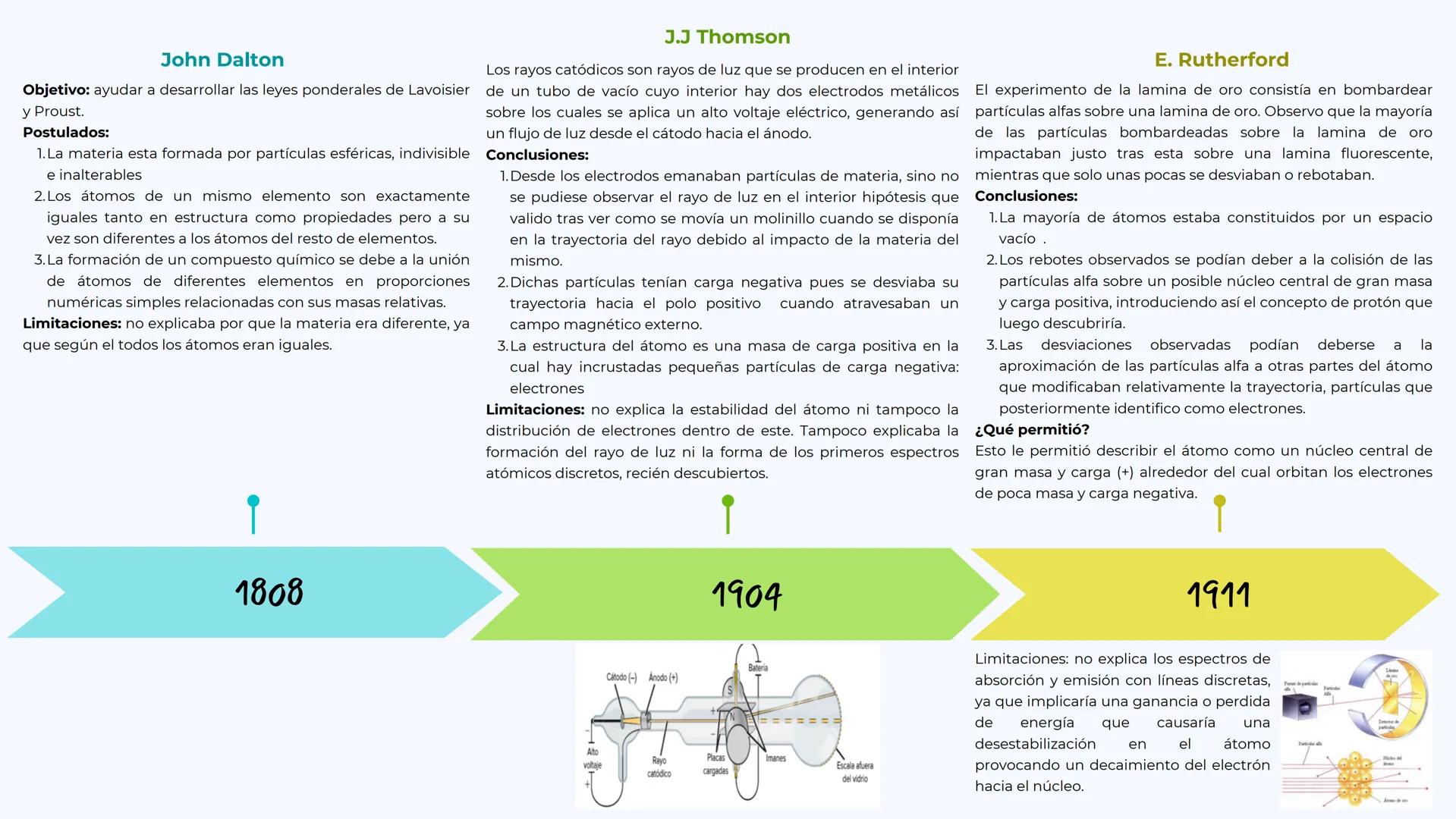
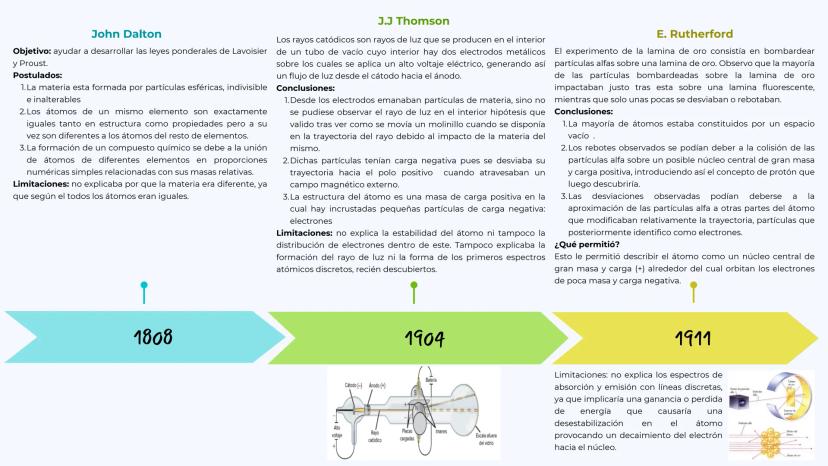
John Dalton (1808) propuso que los átomos eran como esferas sólidas e indivisibles. Su idea era súper simple: todos los átomos de un elemento son iguales, pero diferentes a los de otros elementos. Aunque no explicaba por qué la materia era tan diversa, sentó las bases de todo lo que vino después.
J.J. Thomson (1904) descubrió el electrón usando los famosos rayos catódicos. Su experimento con tubos de vacío demostró que existían partículas con carga negativa. Propuso el modelo del "pudín de pasas": una masa positiva con electrones incrustados como pasas en un pudín.
Ernest Rutherford (1911) lo cambió todo con su experimento de la lámina de oro. Bombardeó una lámina súper fina de oro con partículas alfa y descubrió algo increíble: la mayoría pasaban de largo, pero algunas rebotaban. Esto significaba que el átomo era en su mayor parte espacio vacío con un núcleo central denso y positivo.
⚡ Experimento clave: El experimento de Rutherford fue como disparar balas de cañón a una hoja de papel y ver que algunas rebotaban hacia atrás. ¡Totalmente inesperado!
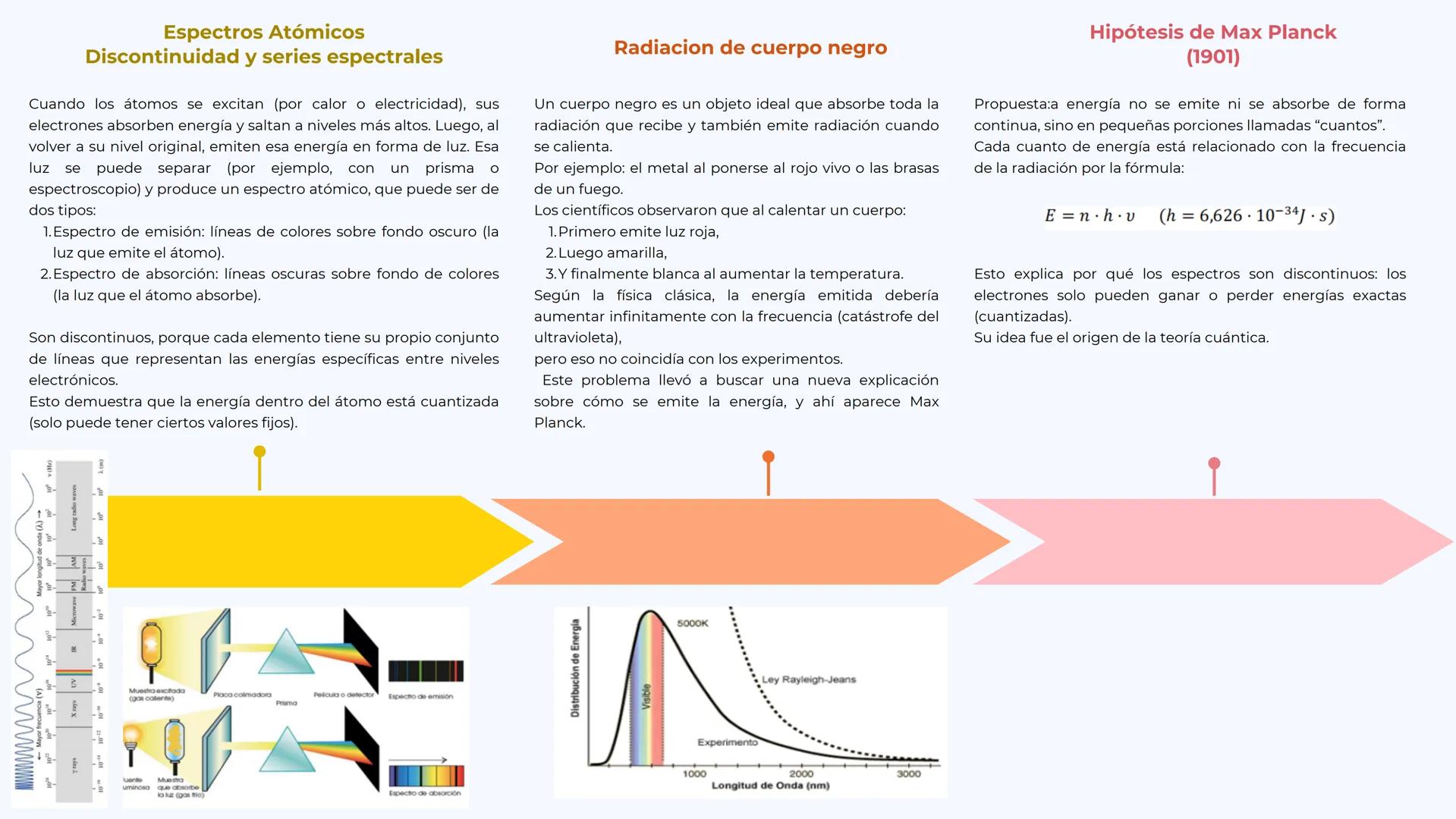
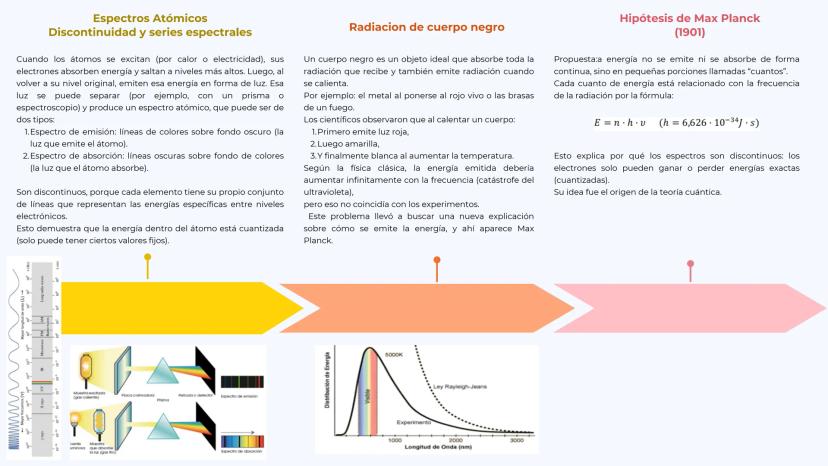
Los espectros atómicos son como las "huellas dactilares" de cada elemento. Cuando calientas un gas, los electrones absorben energía y luego la emiten como luz de colores específicos. Cada elemento produce un patrón único de líneas.
Hay dos tipos: espectros de emisión (líneas brillantes sobre fondo oscuro) y espectros de absorción (líneas oscuras sobre fondo brillante). Lo crucial es que son discontinuos: solo aparecen ciertas líneas, no un arcoíris continuo.
La radiación de cuerpo negro era otro misterio. Cuando calientas un metal, primero se pone rojo, luego amarillo y finalmente blanco. La física clásica predecía resultados completamente erróneos (la famosa "catástrofe del ultravioleta").
Max Planck (1901) resolvió el problema proponiendo que la energía viene en "paquetes" llamados cuantos. Su fórmula E = n·h·v cambió la física para siempre y explicó por qué los espectros son discontinuos.
🌈 Visualízalo: Es como si los electrones fueran por una escalera en lugar de por una rampa: solo pueden estar en ciertos "escalones" de energía.
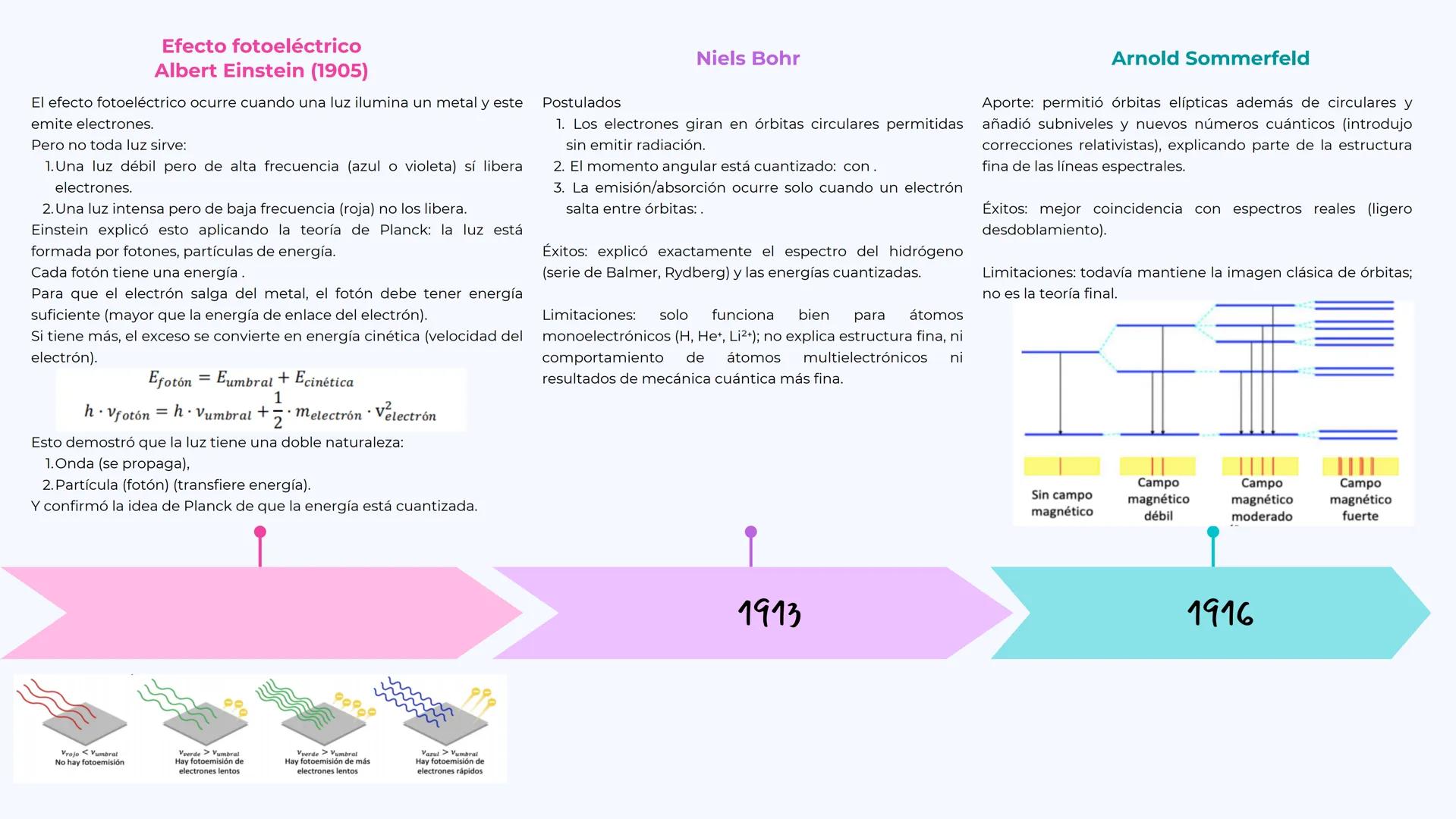
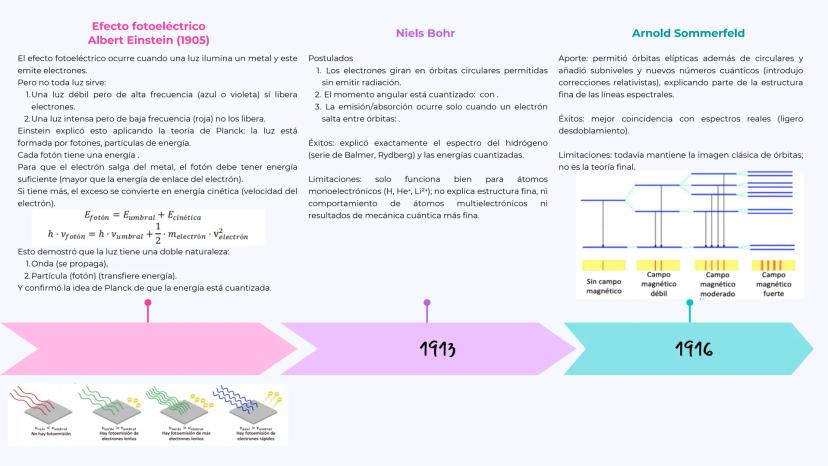
Einstein (1905) explicó el efecto fotoeléctrico y ganó el Nobel por ello. Descubrió algo raro: una luz débil pero azul puede sacar electrones de un metal, pero una luz roja intensa no puede. La explicación: la luz son partículas llamadas fotones, y cada una necesita energía mínima para liberar un electrón.
Niels Bohr (1913) creó el primer modelo que realmente funcionaba para el hidrógeno. Propuso que los electrones giran en órbitas fijas sin emitir radiación, y solo emiten o absorben energía cuando saltan entre órbitas. Su modelo explicó perfectamente el espectro del hidrógeno.
Arnold Sommerfeld (1916) mejoró el modelo de Bohr añadiendo órbitas elípticas además de las circulares. Esto explicó mejor algunos detalles finos de los espectros, aunque seguía siendo una aproximación.
Ambos modelos tenían limitaciones: solo funcionaban bien para átomos simples como el hidrógeno, y seguían tratando a los electrones como partículas clásicas en órbitas definidas.
🎯 Punto clave: Bohr fue el primero en combinar exitosamente la física clásica con las ideas cuánticas de Planck.
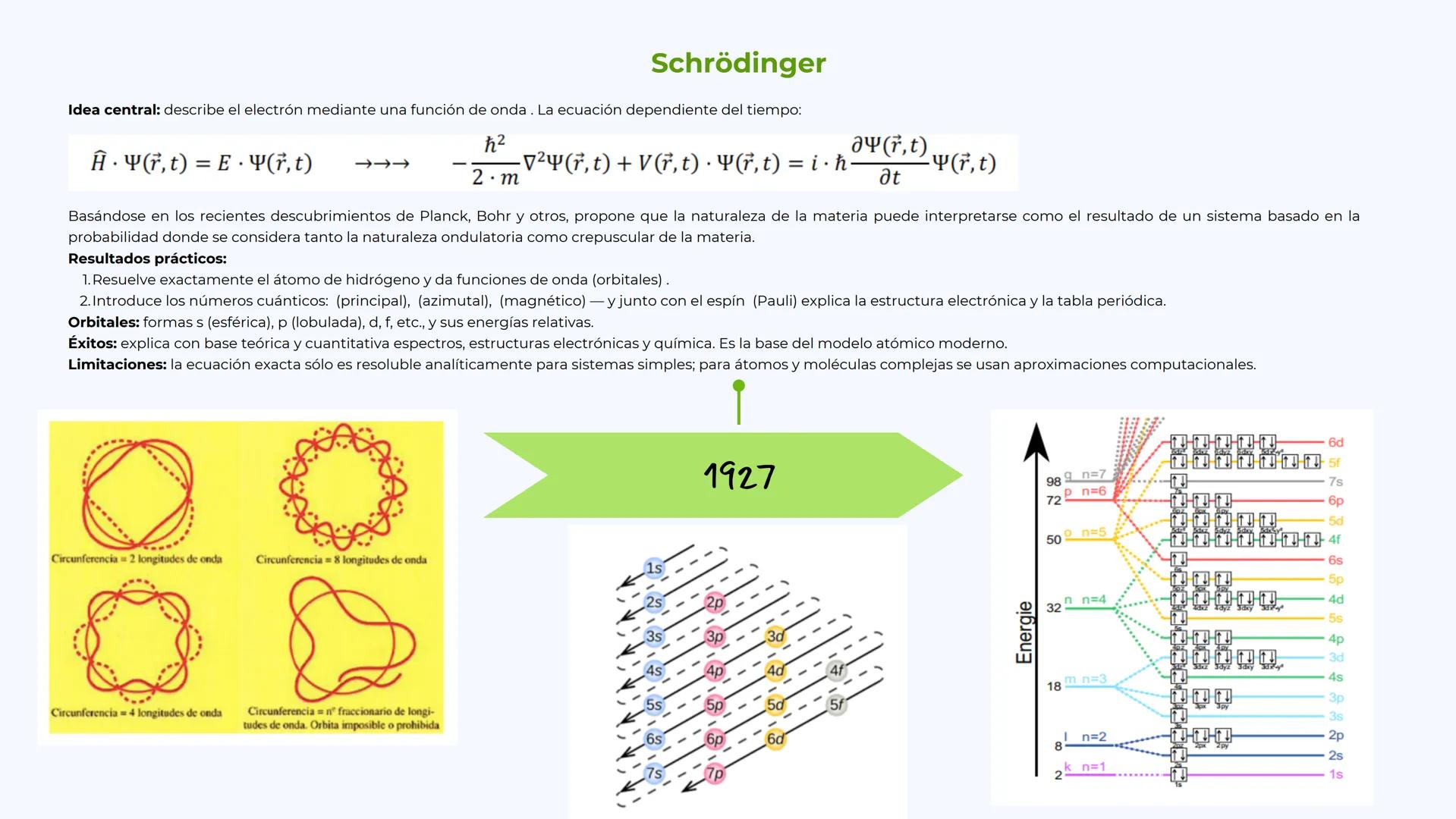
Schrödinger (1927) revolucionó todo con su ecuación de onda. En lugar de órbitas fijas, propuso que los electrones se comportan como ondas y solo podemos calcular la probabilidad de encontrarlos en cierta región del espacio.
Su enfoque matemático introduce los números cuánticos (n, l, m) que describen completamente el estado de un electrón. Esto da origen a los orbitales: las famosas formas s (esféricas), p (con forma de mancuerna), d y f que seguramente has visto en química.
El modelo de Schrödinger explica no solo el hidrógeno, sino también átomos complejos, enlaces químicos y la estructura de la tabla periódica. Es el modelo atómico moderno que usamos hoy en día.
La diferencia clave: ya no hablamos de órbitas definidas, sino de nubes de probabilidad donde es más probable encontrar al electrón. Es como pasar de saber exactamente dónde está una pelota a conocer las zonas donde probablemente la encontraremos.
🎲 Concepto revolucionario: En el mundo cuántico, la probabilidad no es ignorancia, ¡es la naturaleza fundamental de la realidad!
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
Gabriela Alejandra Madrigal Pérez
@gabrielaa_1zta3
¿Alguna vez te has preguntado cómo llegamos a entender la estructura del átomo? La historia del modelo atómico es como un thriller científico lleno de experimentos geniales y descubrimientos que cambiaron todo lo que creíamos saber sobre la materia.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La evolución del modelo atómico es una de las historias más fascinantes de la ciencia. Desde 1808 hasta 1927, diferentes científicos fueron construyendo pieza a pieza nuestra comprensión actual del átomo.
Todo empezó con John Dalton en 1808, que imaginó los átomos como pequeñas esferas sólidas. Luego vinieron J.J. Thomson (1904), Ernest Rutherford (1911), Niels Bohr (1913), Arnold Sommerfeld (1916) y finalmente Schrödinger (1927), cada uno añadiendo nuevas piezas al puzzle.
Durante este período también se descubrieron las partículas subatómicas: primero el electrón, después el protón y más tarde el neutrón. Cada descubrimiento obligó a los científicos a repensar completamente sus ideas anteriores.
💡 Dato curioso: Cada modelo no "reemplazaba" completamente al anterior, sino que explicaba cosas que el anterior no podía explicar. ¡La ciencia es así de genial!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
John Dalton (1808) propuso que los átomos eran como esferas sólidas e indivisibles. Su idea era súper simple: todos los átomos de un elemento son iguales, pero diferentes a los de otros elementos. Aunque no explicaba por qué la materia era tan diversa, sentó las bases de todo lo que vino después.
J.J. Thomson (1904) descubrió el electrón usando los famosos rayos catódicos. Su experimento con tubos de vacío demostró que existían partículas con carga negativa. Propuso el modelo del "pudín de pasas": una masa positiva con electrones incrustados como pasas en un pudín.
Ernest Rutherford (1911) lo cambió todo con su experimento de la lámina de oro. Bombardeó una lámina súper fina de oro con partículas alfa y descubrió algo increíble: la mayoría pasaban de largo, pero algunas rebotaban. Esto significaba que el átomo era en su mayor parte espacio vacío con un núcleo central denso y positivo.
⚡ Experimento clave: El experimento de Rutherford fue como disparar balas de cañón a una hoja de papel y ver que algunas rebotaban hacia atrás. ¡Totalmente inesperado!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los espectros atómicos son como las "huellas dactilares" de cada elemento. Cuando calientas un gas, los electrones absorben energía y luego la emiten como luz de colores específicos. Cada elemento produce un patrón único de líneas.
Hay dos tipos: espectros de emisión (líneas brillantes sobre fondo oscuro) y espectros de absorción (líneas oscuras sobre fondo brillante). Lo crucial es que son discontinuos: solo aparecen ciertas líneas, no un arcoíris continuo.
La radiación de cuerpo negro era otro misterio. Cuando calientas un metal, primero se pone rojo, luego amarillo y finalmente blanco. La física clásica predecía resultados completamente erróneos (la famosa "catástrofe del ultravioleta").
Max Planck (1901) resolvió el problema proponiendo que la energía viene en "paquetes" llamados cuantos. Su fórmula E = n·h·v cambió la física para siempre y explicó por qué los espectros son discontinuos.
🌈 Visualízalo: Es como si los electrones fueran por una escalera en lugar de por una rampa: solo pueden estar en ciertos "escalones" de energía.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Einstein (1905) explicó el efecto fotoeléctrico y ganó el Nobel por ello. Descubrió algo raro: una luz débil pero azul puede sacar electrones de un metal, pero una luz roja intensa no puede. La explicación: la luz son partículas llamadas fotones, y cada una necesita energía mínima para liberar un electrón.
Niels Bohr (1913) creó el primer modelo que realmente funcionaba para el hidrógeno. Propuso que los electrones giran en órbitas fijas sin emitir radiación, y solo emiten o absorben energía cuando saltan entre órbitas. Su modelo explicó perfectamente el espectro del hidrógeno.
Arnold Sommerfeld (1916) mejoró el modelo de Bohr añadiendo órbitas elípticas además de las circulares. Esto explicó mejor algunos detalles finos de los espectros, aunque seguía siendo una aproximación.
Ambos modelos tenían limitaciones: solo funcionaban bien para átomos simples como el hidrógeno, y seguían tratando a los electrones como partículas clásicas en órbitas definidas.
🎯 Punto clave: Bohr fue el primero en combinar exitosamente la física clásica con las ideas cuánticas de Planck.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Schrödinger (1927) revolucionó todo con su ecuación de onda. En lugar de órbitas fijas, propuso que los electrones se comportan como ondas y solo podemos calcular la probabilidad de encontrarlos en cierta región del espacio.
Su enfoque matemático introduce los números cuánticos (n, l, m) que describen completamente el estado de un electrón. Esto da origen a los orbitales: las famosas formas s (esféricas), p (con forma de mancuerna), d y f que seguramente has visto en química.
El modelo de Schrödinger explica no solo el hidrógeno, sino también átomos complejos, enlaces químicos y la estructura de la tabla periódica. Es el modelo atómico moderno que usamos hoy en día.
La diferencia clave: ya no hablamos de órbitas definidas, sino de nubes de probabilidad donde es más probable encontrar al electrón. Es como pasar de saber exactamente dónde está una pelota a conocer las zonas donde probablemente la encontraremos.
🎲 Concepto revolucionario: En el mundo cuántico, la probabilidad no es ignorancia, ¡es la naturaleza fundamental de la realidad!
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
4
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS