La Termoquímica es la rama de la química que estudia... Mostrar más
Termoquímica: Principios y Apuntes Fundamentales para Bachillerato CLM









Fundamentos de la Termoquímica
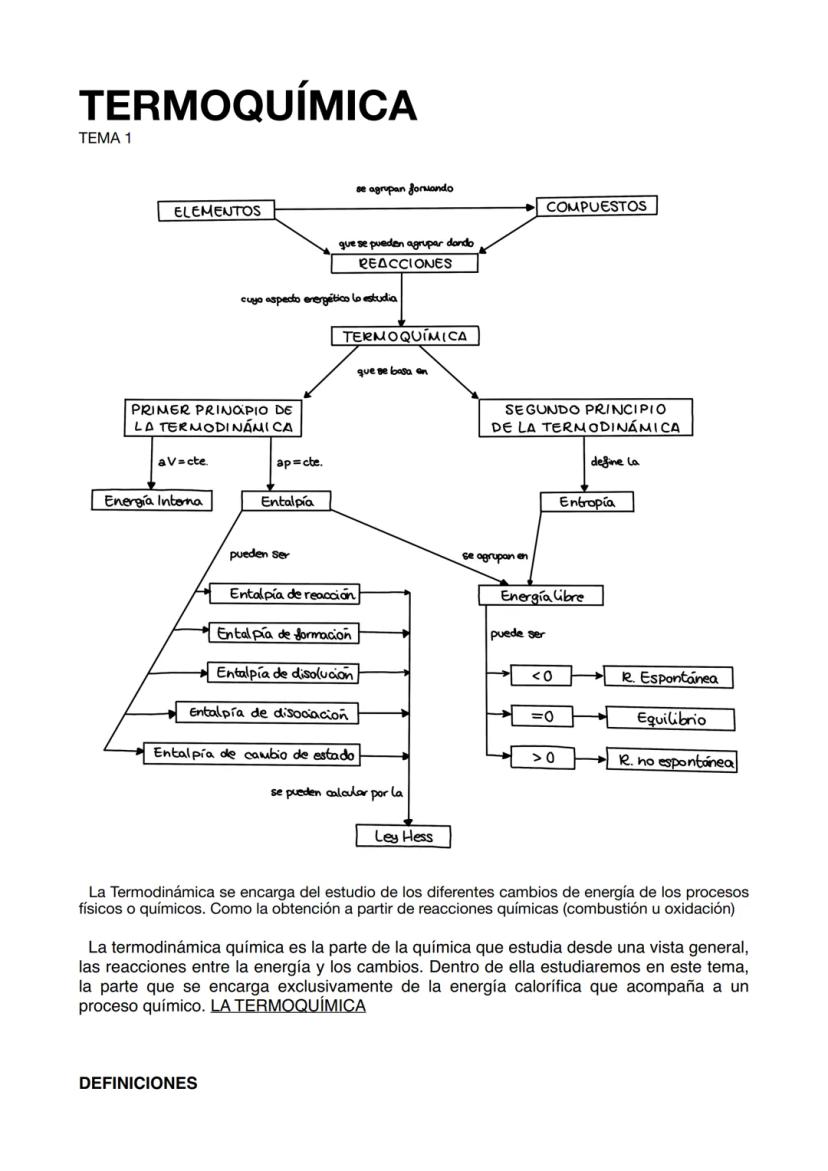
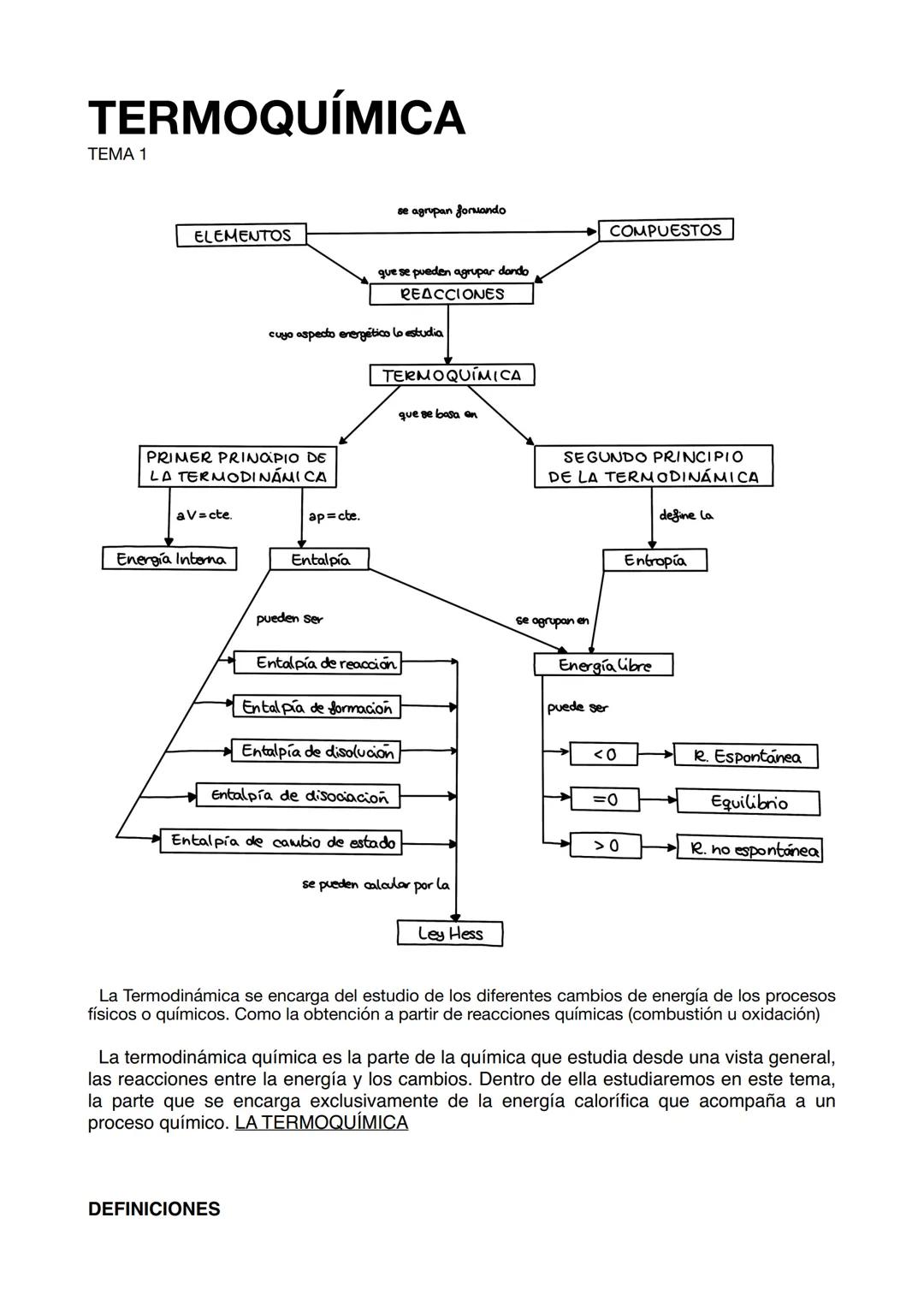
La Termoquímica estudia específicamente la energía calorífica que acompaña a las reacciones químicas. Este campo forma parte de la termodinámica química, que analiza la relación entre la energía y los cambios químicos desde una perspectiva más general.
Cuando hablamos de termoquímica, nos referimos a cómo la energía se transforma durante procesos como combustiones u oxidaciones. Estos procesos son fundamentales en nuestra vida cotidiana, desde la energía que libera la gasolina en un motor hasta la que produce nuestro propio cuerpo al metabolizar los alimentos.
La termoquímica se basa en dos principios fundamentales: el Primer Principio de la Termodinámica, que nos habla sobre la conservación de la energía, y el Segundo Principio, que introduce el concepto de entropía y nos ayuda a determinar si un proceso ocurrirá de forma espontánea.
⚡ Dato clave: Las reacciones químicas no solo transforman materia sino también energía. Esta energía puede manifestarse como calor, trabajo o cambios en la energía interna del sistema.

Sistemas Termodinámicos y Variables
Un sistema termodinámico es una porción del universo que elegimos estudiar. Según su interacción con el entorno, puede ser abierto (intercambia materia y energía), cerrado (solo intercambia energía) o aislado (no intercambia ni materia ni energía).
Los sistemas también pueden clasificarse según sus fases como homogéneos (una sola fase) o heterogéneos (varias fases). Una fase es una parte del sistema que tiene propiedades uniformes en toda su extensión.
Para describir un sistema necesitamos variables termodinámicas, que pueden ser:
- Extensivas: dependen de la cantidad de material (masa, volumen, entropía)
- Intensivas: tienen un valor definido en cada punto del sistema (temperatura, presión, densidad)
Las funciones de estado son propiedades que solo dependen del estado actual del sistema, no de cómo llegó a él. Por ejemplo, la energía interna, la entalpía, el volumen o la presión. Un cambio en estas funciones solo depende de los estados inicial y final.
🔍 Observación importante: Para determinar completamente un sistema, no necesitamos conocer todas sus variables, ya que muchas están relacionadas entre sí mediante ecuaciones de estado.

Trabajo, Calor y Energía Interna
El trabajo en termoquímica suele referirse principalmente al trabajo de expansión de gases. Cuando un sistema se expande, realiza trabajo positivo sobre el entorno; cuando se comprime, el trabajo es negativo (el entorno realiza trabajo sobre el sistema).
El calor es la energía que se transfiere entre un sistema y su entorno debido a una diferencia de temperatura. Es importante entender que un cuerpo no "tiene" calor, sino que intercambia energía en forma de calor. El calor es positivo cuando el sistema absorbe energía (proceso endotérmico) y negativo cuando la cede (proceso exotérmico).
La energía interna (U) es la suma total de todas las energías contenidas en el sistema:
- Energía de traslación de partículas
- Energía de rotación y vibración molecular
- Energía nuclear y electrónica
- Cualquier otra forma de energía presente
La energía interna es una función de estado, lo que significa que su cambio solo depende del estado inicial y final, independientemente del camino seguido.
🔥 Recuerda: La energía no se crea ni se destruye, solo se transforma. Esta es la esencia del Primer Principio de la Termodinámica, que establece que ΔU = q + W (el cambio de energía interna es igual al calor absorbido más el trabajo realizado por el sistema).

Primer Principio de la Termodinámica y Entalpía
El Primer Principio de la Termodinámica establece que "la energía puede transformarse de una forma a otra, pero nunca se crea ni se destruye". Matemáticamente se expresa como:
ΔU = q + W
Donde:
- ΔU es el cambio de la energía interna
- q es el calor absorbido o cedido
- W es el trabajo realizado por o sobre el sistema
En las reacciones químicas, este principio nos ayuda a entender los intercambios energéticos:
- q positivo → el sistema absorbe calor (endotérmico)
- q negativo → el sistema cede calor (exotérmico)
- W negativo → el sistema realiza trabajo sobre el entorno
- W positivo → el entorno realiza trabajo sobre el sistema
La entalpía (H) es una función de estado definida como H = U + pV. Es especialmente útil porque la mayoría de las reacciones químicas ocurren a presión constante (por ejemplo, en recipientes abiertos a la atmósfera). En estas condiciones:
ΔH = qp (a presión constante)
Esto significa que el cambio de entalpía es igual al calor intercambiado a presión constante, lo que facilita enormemente los cálculos termoquímicos.
📊 Aplicación práctica: Cuando veas valores de ΔH negativos, sabrás que la reacción libera calor (exotérmica), mientras que valores positivos indican que la reacción absorbe calor (endotérmica).

Entalpía de Reacción y Formación
La entalpía de reacción es el calor intercambiado cuando una reacción se produce a presión constante. Se calcula como:
ΔH = ∑H(productos) - ∑H(reactivos)
En termoquímica, no podemos conocer valores absolutos de entalpía, solo sus variaciones. Por eso, se establece un sistema de referencia basado en entalpías estándar, que se miden en condiciones normalizadas:
- Temperatura: 25°C (298 K)
- Presión: 1 atmósfera
- Estados físicos específicos (gas, líquido puro, sólido puro, disolución 1M)
La entalpía de formación (ΔHf°) es el cambio de entalpía cuando se forma un mol de un compuesto a partir de sus elementos constituyentes en sus estados estándar. Por definición, la entalpía de formación de los elementos en sus estados estándar es cero.
Las entalpías de formación nos indican la estabilidad de los compuestos:
- ΔHf° negativa → el compuesto es más estable que sus elementos
- ΔHf° positiva → los elementos son más estables que el compuesto
- Cuanto más negativa sea la ΔHf°, más estable será el compuesto
En los cálculos, una ventaja importante es que podemos determinar la entalpía de cualquier reacción si conocemos las entalpías de formación de todas las sustancias involucradas:
ΔH° = ∑ΔHf°(productos) - ∑ΔHf°(reactivos)
💡 Truco de estudio: Para recordar si restas productos menos reactivos o al revés, piensa en la frase "siempre se resta hacia donde va la flecha de la reacción" .

Otros Tipos de Entalpía y Ley de Hess
Además de la entalpía de formación, existen otros tipos importantes:
-
Entalpía de disociación: Es la energía necesaria para descomponer 1 mol de una sustancia en sus átomos constituyentes en estado gaseoso.
-
Entalpía de cambio de estado: También llamada calor latente, es la energía intercambiada cuando 1 mol de sustancia cambia de estado físico (fusión, vaporización, etc.) a temperatura y presión constantes.
-
Entalpía de disolución: Es la energía intercambiada cuando 1 mol de una sustancia se disuelve completamente en una cantidad suficiente de disolvente.
La Ley de Hess es un principio fundamental que establece: "El cambio de entalpía de una reacción es el mismo, ya sea que la reacción ocurra en una sola etapa o en varias". Esta ley nos permite calcular entalpías de reacción difíciles de medir directamente.
Según la Ley de Hess, cuando una reacción se expresa como suma algebraica de otras reacciones, su entalpía de reacción será igual a la suma algebraica de las entalpías de esas reacciones parciales.
La Ley de Hess funciona porque la entalpía es una función de estado, por lo que su variación solo depende de los estados inicial y final, no del camino seguido.
🧪 Aplicación práctica: La Ley de Hess nos permite diseñar "rutas alternativas" para calcular entalpías de reacción que no podemos medir directamente en el laboratorio.

Espontaneidad y Segundo Principio
¿Qué determina si una reacción ocurrirá espontáneamente? La variación de entalpía no es suficiente para predecirlo, ya que existen reacciones endotérmicas que ocurren de forma espontánea.
El Segundo Principio de la Termodinámica introduce el concepto de entropía (S), una medida del desorden o aleatoriedad de un sistema. Este principio establece que "en los procesos espontáneos, la entropía del universo tiende a aumentar".
Matemáticamente: ΔSuniverso = ΔSsistema + ΔSalrededores > 0 (para procesos espontáneos)
La entropía es una función de estado que:
- Está definida solo en condiciones de equilibrio
- Es una propiedad extensiva (depende de la cantidad de materia)
- Su variación solo depende de los estados inicial y final
Las sustancias sólidas tienen menor entropía que las líquidas, y éstas menor que las gaseosas. Los procesos que aumentan el desorden (como fusión, ebullición o disociación) provocan un aumento de entropía.
Para reacciones en condiciones estándar, calculamos la entropía de reacción como: ΔS° = ∑S°(productos) - ∑S°(reactivos)
🌡️ Concepto clave: En procesos reversibles (ideales), ΔSuniverso = 0, representando el equilibrio. En procesos reales (irreversibles), ΔSuniverso > 0, indicando espontaneidad.

Segundo Principio y Reversibilidad
Un proceso termodinámicamente reversible es aquél que puede invertir su sentido modificando infinitesimalmente las condiciones externas. Este concepto es teórico, ya que requeriría un cambio infinitamente lento, manteniendo el sistema siempre en equilibrio. En la práctica, todos los procesos reales son irreversibles.
El Segundo Principio de la Termodinámica afirma que en los cambios espontáneos, el universo tiende hacia un mayor desorden. Esta ley fundamental:
- Se basa en la experiencia observada
- No puede demostrarse a partir de principios más básicos
- Introduce la entropía como una propiedad macroscópica de los sistemas
Para un sistema aislado, podemos establecer criterios claros:
- Proceso reversible (equilibrio): ΔSuniverso = 0
- Proceso irreversible (espontáneo): ΔSuniverso > 0
La entropía (S) cumple tres propiedades fundamentales:
- Su valor está definido únicamente en condiciones de equilibrio
- Es una propiedad extensiva (depende de la masa del sistema)
- Su variación solo depende de los estados inicial y final
La entropía puede calcularse mediante la relación ΔS = ΔH/T para cambios reversibles a temperatura constante.
🔄 Reflexión importante: La entropía es una medida del grado de desorden o aleatoriedad. Un sistema ordenado (como un cristal perfecto) tiene baja entropía, mientras que un sistema desordenado (como un gas) tiene alta entropía.

Entropía y Energía Libre
La entropía nos ayuda a predecir el sentido de evolución en sistemas aislados, pero la mayoría de los procesos químicos ocurren en sistemas que intercambian energía con el entorno. ¿Cómo predecir la espontaneidad en estos casos?
La entropía estándar de una reacción se calcula como: ΔS°r = ∑S°(productos) - ∑S°(reactivos)
Donde S° son las entropías estándar de cada sustancia.
Las entropías siguen un patrón general:
- Sólidos < Líquidos < Gases
- La fusión aumenta la entropía (se rompe la estructura ordenada del sólido)
- La ebullición conlleva un aumento mayor de entropía (las moléculas adquieren mucha más libertad de movimiento)
La entropía nos permite entender por qué algunos procesos son espontáneos incluso cuando son endotérmicos. Sin embargo, para sistemas que no están aislados necesitamos otra función termodinámica que combine los efectos de entalpía y entropía.
Esta función es la energía libre de Gibbs, que veremos en la siguiente página. La energía libre nos proporcionará un criterio único para predecir la espontaneidad en condiciones de presión y temperatura constantes.
🌍 Ejemplo cotidiano: La evaporación del agua es un proceso endotérmico (absorbe calor) pero espontáneo a temperatura ambiente debido al gran aumento de entropía cuando las moléculas de agua pasan del estado líquido al gaseoso.

Energía Libre de Gibbs
La energía libre de Gibbs (G) es una función termodinámica que combina los efectos de la entalpía y la entropía. Se define como:
G = H - T·S
Esta función es especialmente útil porque nos permite establecer un único criterio para predecir la espontaneidad de procesos a presión y temperatura constantes (condiciones típicas de muchas reacciones químicas).
A presión y temperatura constantes:
- ΔG < 0: el proceso es espontáneo
- ΔG = 0: el sistema está en equilibrio
- ΔG > 0: el proceso no es espontáneo (el proceso inverso sería espontáneo)
Cuando la energía libre disminuye (ΔG < 0), podemos obtener trabajo útil del sistema. De hecho, -ΔG representa el trabajo máximo que puede obtenerse de un proceso, excluyendo el trabajo de expansión.
La energía libre nos ayuda a entender por qué algunas reacciones endotérmicas (ΔH > 0) pueden ser espontáneas. Si el término T·ΔS es mayor que ΔH, entonces ΔG será negativo y el proceso será espontáneo a pesar de absorber calor.
Existe también la energía libre de Helmholtz (A), definida como A = U - T·S, que es más adecuada para procesos a volumen constante.
⚖️ Concepto clave: La energía libre es una "batalla" entre entalpía y entropía. A temperaturas bajas, el factor entálpico (ΔH) suele dominar, mientras que a temperaturas altas, el factor entrópico (T·ΔS) cobra mayor importancia.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: primera ley de la termodinámica
4TRABAJO Y ENERGIA MECÁNICA. FÓRMULAS
Fórmulas
EJERCICIOS RESUELTOS DE TERMOQUÍMICA
EJERCICIOS RESUELTOS DE TERMOQUÍMICA
Resumen termoquímica
Fórmulas y principios de la termodinámica .
Termodinámica y cinética química 2bach
Resumen sobre las fórmulas de termodinámica y cinética química 2 bach
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Termoquímica: Principios y Apuntes Fundamentales para Bachillerato CLM
La Termoquímica es la rama de la química que estudia los cambios energéticos que ocurren durante las reacciones químicas. Entender estos cambios nos permitirá predecir si una reacción es espontánea o no, cuánta energía libera o absorbe, y cómo podemos... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fundamentos de la Termoquímica
La Termoquímica estudia específicamente la energía calorífica que acompaña a las reacciones químicas. Este campo forma parte de la termodinámica química, que analiza la relación entre la energía y los cambios químicos desde una perspectiva más general.
Cuando hablamos de termoquímica, nos referimos a cómo la energía se transforma durante procesos como combustiones u oxidaciones. Estos procesos son fundamentales en nuestra vida cotidiana, desde la energía que libera la gasolina en un motor hasta la que produce nuestro propio cuerpo al metabolizar los alimentos.
La termoquímica se basa en dos principios fundamentales: el Primer Principio de la Termodinámica, que nos habla sobre la conservación de la energía, y el Segundo Principio, que introduce el concepto de entropía y nos ayuda a determinar si un proceso ocurrirá de forma espontánea.
⚡ Dato clave: Las reacciones químicas no solo transforman materia sino también energía. Esta energía puede manifestarse como calor, trabajo o cambios en la energía interna del sistema.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sistemas Termodinámicos y Variables
Un sistema termodinámico es una porción del universo que elegimos estudiar. Según su interacción con el entorno, puede ser abierto (intercambia materia y energía), cerrado (solo intercambia energía) o aislado (no intercambia ni materia ni energía).
Los sistemas también pueden clasificarse según sus fases como homogéneos (una sola fase) o heterogéneos (varias fases). Una fase es una parte del sistema que tiene propiedades uniformes en toda su extensión.
Para describir un sistema necesitamos variables termodinámicas, que pueden ser:
- Extensivas: dependen de la cantidad de material (masa, volumen, entropía)
- Intensivas: tienen un valor definido en cada punto del sistema (temperatura, presión, densidad)
Las funciones de estado son propiedades que solo dependen del estado actual del sistema, no de cómo llegó a él. Por ejemplo, la energía interna, la entalpía, el volumen o la presión. Un cambio en estas funciones solo depende de los estados inicial y final.
🔍 Observación importante: Para determinar completamente un sistema, no necesitamos conocer todas sus variables, ya que muchas están relacionadas entre sí mediante ecuaciones de estado.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Trabajo, Calor y Energía Interna
El trabajo en termoquímica suele referirse principalmente al trabajo de expansión de gases. Cuando un sistema se expande, realiza trabajo positivo sobre el entorno; cuando se comprime, el trabajo es negativo (el entorno realiza trabajo sobre el sistema).
El calor es la energía que se transfiere entre un sistema y su entorno debido a una diferencia de temperatura. Es importante entender que un cuerpo no "tiene" calor, sino que intercambia energía en forma de calor. El calor es positivo cuando el sistema absorbe energía (proceso endotérmico) y negativo cuando la cede (proceso exotérmico).
La energía interna (U) es la suma total de todas las energías contenidas en el sistema:
- Energía de traslación de partículas
- Energía de rotación y vibración molecular
- Energía nuclear y electrónica
- Cualquier otra forma de energía presente
La energía interna es una función de estado, lo que significa que su cambio solo depende del estado inicial y final, independientemente del camino seguido.
🔥 Recuerda: La energía no se crea ni se destruye, solo se transforma. Esta es la esencia del Primer Principio de la Termodinámica, que establece que ΔU = q + W (el cambio de energía interna es igual al calor absorbido más el trabajo realizado por el sistema).

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Primer Principio de la Termodinámica y Entalpía
El Primer Principio de la Termodinámica establece que "la energía puede transformarse de una forma a otra, pero nunca se crea ni se destruye". Matemáticamente se expresa como:
ΔU = q + W
Donde:
- ΔU es el cambio de la energía interna
- q es el calor absorbido o cedido
- W es el trabajo realizado por o sobre el sistema
En las reacciones químicas, este principio nos ayuda a entender los intercambios energéticos:
- q positivo → el sistema absorbe calor (endotérmico)
- q negativo → el sistema cede calor (exotérmico)
- W negativo → el sistema realiza trabajo sobre el entorno
- W positivo → el entorno realiza trabajo sobre el sistema
La entalpía (H) es una función de estado definida como H = U + pV. Es especialmente útil porque la mayoría de las reacciones químicas ocurren a presión constante (por ejemplo, en recipientes abiertos a la atmósfera). En estas condiciones:
ΔH = qp (a presión constante)
Esto significa que el cambio de entalpía es igual al calor intercambiado a presión constante, lo que facilita enormemente los cálculos termoquímicos.
📊 Aplicación práctica: Cuando veas valores de ΔH negativos, sabrás que la reacción libera calor (exotérmica), mientras que valores positivos indican que la reacción absorbe calor (endotérmica).

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Entalpía de Reacción y Formación
La entalpía de reacción es el calor intercambiado cuando una reacción se produce a presión constante. Se calcula como:
ΔH = ∑H(productos) - ∑H(reactivos)
En termoquímica, no podemos conocer valores absolutos de entalpía, solo sus variaciones. Por eso, se establece un sistema de referencia basado en entalpías estándar, que se miden en condiciones normalizadas:
- Temperatura: 25°C (298 K)
- Presión: 1 atmósfera
- Estados físicos específicos (gas, líquido puro, sólido puro, disolución 1M)
La entalpía de formación (ΔHf°) es el cambio de entalpía cuando se forma un mol de un compuesto a partir de sus elementos constituyentes en sus estados estándar. Por definición, la entalpía de formación de los elementos en sus estados estándar es cero.
Las entalpías de formación nos indican la estabilidad de los compuestos:
- ΔHf° negativa → el compuesto es más estable que sus elementos
- ΔHf° positiva → los elementos son más estables que el compuesto
- Cuanto más negativa sea la ΔHf°, más estable será el compuesto
En los cálculos, una ventaja importante es que podemos determinar la entalpía de cualquier reacción si conocemos las entalpías de formación de todas las sustancias involucradas:
ΔH° = ∑ΔHf°(productos) - ∑ΔHf°(reactivos)
💡 Truco de estudio: Para recordar si restas productos menos reactivos o al revés, piensa en la frase "siempre se resta hacia donde va la flecha de la reacción" .

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Otros Tipos de Entalpía y Ley de Hess
Además de la entalpía de formación, existen otros tipos importantes:
-
Entalpía de disociación: Es la energía necesaria para descomponer 1 mol de una sustancia en sus átomos constituyentes en estado gaseoso.
-
Entalpía de cambio de estado: También llamada calor latente, es la energía intercambiada cuando 1 mol de sustancia cambia de estado físico (fusión, vaporización, etc.) a temperatura y presión constantes.
-
Entalpía de disolución: Es la energía intercambiada cuando 1 mol de una sustancia se disuelve completamente en una cantidad suficiente de disolvente.
La Ley de Hess es un principio fundamental que establece: "El cambio de entalpía de una reacción es el mismo, ya sea que la reacción ocurra en una sola etapa o en varias". Esta ley nos permite calcular entalpías de reacción difíciles de medir directamente.
Según la Ley de Hess, cuando una reacción se expresa como suma algebraica de otras reacciones, su entalpía de reacción será igual a la suma algebraica de las entalpías de esas reacciones parciales.
La Ley de Hess funciona porque la entalpía es una función de estado, por lo que su variación solo depende de los estados inicial y final, no del camino seguido.
🧪 Aplicación práctica: La Ley de Hess nos permite diseñar "rutas alternativas" para calcular entalpías de reacción que no podemos medir directamente en el laboratorio.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Espontaneidad y Segundo Principio
¿Qué determina si una reacción ocurrirá espontáneamente? La variación de entalpía no es suficiente para predecirlo, ya que existen reacciones endotérmicas que ocurren de forma espontánea.
El Segundo Principio de la Termodinámica introduce el concepto de entropía (S), una medida del desorden o aleatoriedad de un sistema. Este principio establece que "en los procesos espontáneos, la entropía del universo tiende a aumentar".
Matemáticamente: ΔSuniverso = ΔSsistema + ΔSalrededores > 0 (para procesos espontáneos)
La entropía es una función de estado que:
- Está definida solo en condiciones de equilibrio
- Es una propiedad extensiva (depende de la cantidad de materia)
- Su variación solo depende de los estados inicial y final
Las sustancias sólidas tienen menor entropía que las líquidas, y éstas menor que las gaseosas. Los procesos que aumentan el desorden (como fusión, ebullición o disociación) provocan un aumento de entropía.
Para reacciones en condiciones estándar, calculamos la entropía de reacción como: ΔS° = ∑S°(productos) - ∑S°(reactivos)
🌡️ Concepto clave: En procesos reversibles (ideales), ΔSuniverso = 0, representando el equilibrio. En procesos reales (irreversibles), ΔSuniverso > 0, indicando espontaneidad.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Segundo Principio y Reversibilidad
Un proceso termodinámicamente reversible es aquél que puede invertir su sentido modificando infinitesimalmente las condiciones externas. Este concepto es teórico, ya que requeriría un cambio infinitamente lento, manteniendo el sistema siempre en equilibrio. En la práctica, todos los procesos reales son irreversibles.
El Segundo Principio de la Termodinámica afirma que en los cambios espontáneos, el universo tiende hacia un mayor desorden. Esta ley fundamental:
- Se basa en la experiencia observada
- No puede demostrarse a partir de principios más básicos
- Introduce la entropía como una propiedad macroscópica de los sistemas
Para un sistema aislado, podemos establecer criterios claros:
- Proceso reversible (equilibrio): ΔSuniverso = 0
- Proceso irreversible (espontáneo): ΔSuniverso > 0
La entropía (S) cumple tres propiedades fundamentales:
- Su valor está definido únicamente en condiciones de equilibrio
- Es una propiedad extensiva (depende de la masa del sistema)
- Su variación solo depende de los estados inicial y final
La entropía puede calcularse mediante la relación ΔS = ΔH/T para cambios reversibles a temperatura constante.
🔄 Reflexión importante: La entropía es una medida del grado de desorden o aleatoriedad. Un sistema ordenado (como un cristal perfecto) tiene baja entropía, mientras que un sistema desordenado (como un gas) tiene alta entropía.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Entropía y Energía Libre
La entropía nos ayuda a predecir el sentido de evolución en sistemas aislados, pero la mayoría de los procesos químicos ocurren en sistemas que intercambian energía con el entorno. ¿Cómo predecir la espontaneidad en estos casos?
La entropía estándar de una reacción se calcula como: ΔS°r = ∑S°(productos) - ∑S°(reactivos)
Donde S° son las entropías estándar de cada sustancia.
Las entropías siguen un patrón general:
- Sólidos < Líquidos < Gases
- La fusión aumenta la entropía (se rompe la estructura ordenada del sólido)
- La ebullición conlleva un aumento mayor de entropía (las moléculas adquieren mucha más libertad de movimiento)
La entropía nos permite entender por qué algunos procesos son espontáneos incluso cuando son endotérmicos. Sin embargo, para sistemas que no están aislados necesitamos otra función termodinámica que combine los efectos de entalpía y entropía.
Esta función es la energía libre de Gibbs, que veremos en la siguiente página. La energía libre nos proporcionará un criterio único para predecir la espontaneidad en condiciones de presión y temperatura constantes.
🌍 Ejemplo cotidiano: La evaporación del agua es un proceso endotérmico (absorbe calor) pero espontáneo a temperatura ambiente debido al gran aumento de entropía cuando las moléculas de agua pasan del estado líquido al gaseoso.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Energía Libre de Gibbs
La energía libre de Gibbs (G) es una función termodinámica que combina los efectos de la entalpía y la entropía. Se define como:
G = H - T·S
Esta función es especialmente útil porque nos permite establecer un único criterio para predecir la espontaneidad de procesos a presión y temperatura constantes (condiciones típicas de muchas reacciones químicas).
A presión y temperatura constantes:
- ΔG < 0: el proceso es espontáneo
- ΔG = 0: el sistema está en equilibrio
- ΔG > 0: el proceso no es espontáneo (el proceso inverso sería espontáneo)
Cuando la energía libre disminuye (ΔG < 0), podemos obtener trabajo útil del sistema. De hecho, -ΔG representa el trabajo máximo que puede obtenerse de un proceso, excluyendo el trabajo de expansión.
La energía libre nos ayuda a entender por qué algunas reacciones endotérmicas (ΔH > 0) pueden ser espontáneas. Si el término T·ΔS es mayor que ΔH, entonces ΔG será negativo y el proceso será espontáneo a pesar de absorber calor.
Existe también la energía libre de Helmholtz (A), definida como A = U - T·S, que es más adecuada para procesos a volumen constante.
⚖️ Concepto clave: La energía libre es una "batalla" entre entalpía y entropía. A temperaturas bajas, el factor entálpico (ΔH) suele dominar, mientras que a temperaturas altas, el factor entrópico (T·ΔS) cobra mayor importancia.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: primera ley de la termodinámica
4TRABAJO Y ENERGIA MECÁNICA. FÓRMULAS
Fórmulas
EJERCICIOS RESUELTOS DE TERMOQUÍMICA
EJERCICIOS RESUELTOS DE TERMOQUÍMICA
Resumen termoquímica
Fórmulas y principios de la termodinámica .
Termodinámica y cinética química 2bach
Resumen sobre las fórmulas de termodinámica y cinética química 2 bach
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.