¡Prepárate para dominar uno de los temas más importantes de... Mostrar más
Introducción a la Estructura Atómica y Enlaces Químicos en el Sistema Periódico








Números Cuánticos: El GPS de los Electrones
¿Te has preguntado cómo podemos localizar un electrón en un átomo? Los números cuánticos son como las coordenadas GPS que nos dicen exactamente dónde encontrar cada electrón.
El número cuántico principal (n) te dice en qué "piso" vive el electrón. Cuanto más alto el número (1, 2, 3...), más lejos del núcleo y con más energía está el electrón.
El número cuántico orbital (l) define el "tipo de habitación": l=0 son orbitales s (esféricos), l=1 son orbitales p (con forma de ocho), l=2 son orbitales d, y l=3 son orbitales f. El número magnético (ml) indica hacia dónde apunta el orbital en el espacio, mientras que el número de espín (ms) nos dice si el electrón gira hacia arriba (+1/2) o hacia abajo (-1/2).
💡 Recuerda: Cada electrón tiene su propia "dirección" única definida por estos cuatro números cuánticos.
Configuración Electrónica y el Sistema Periódico
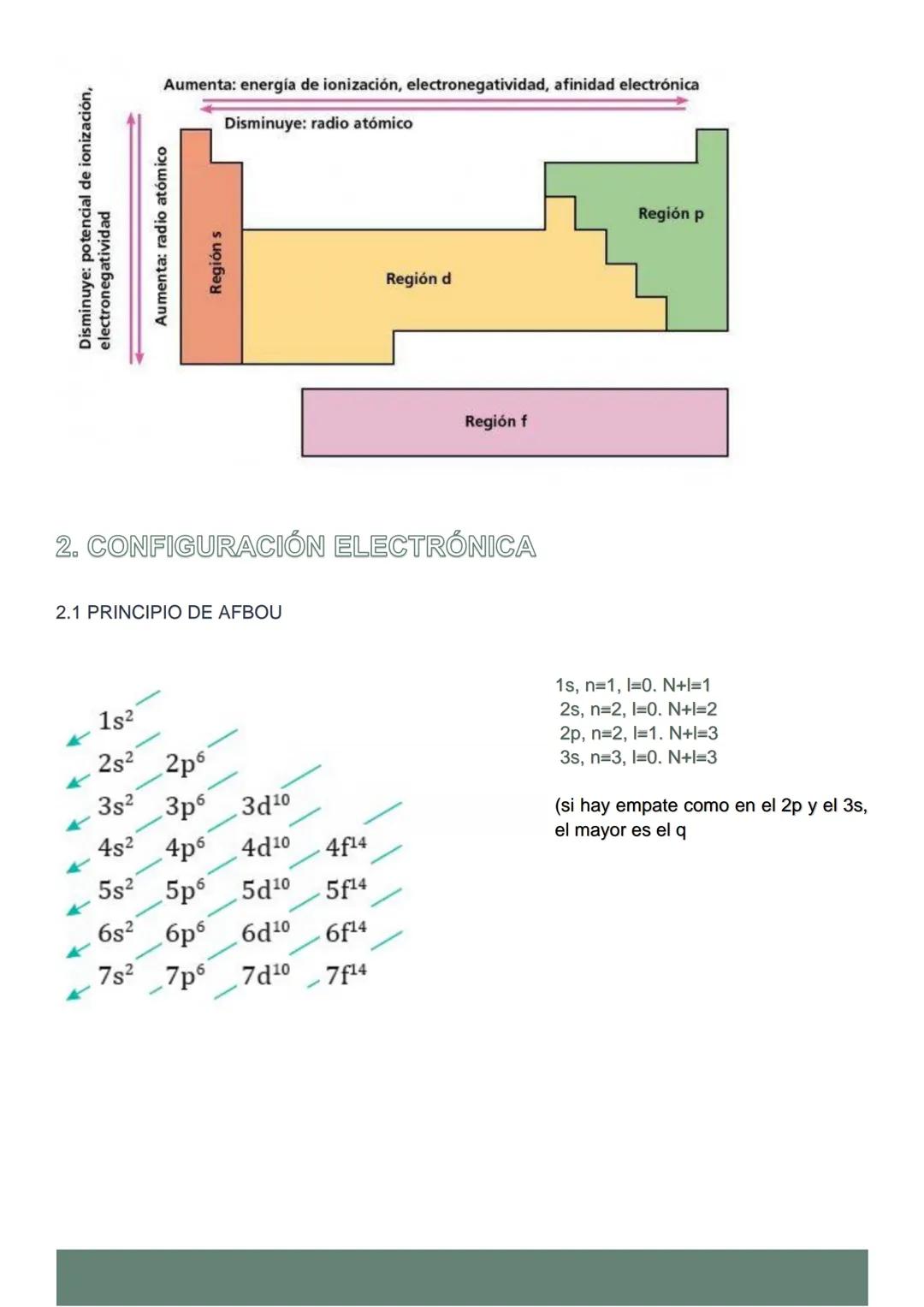
La configuración electrónica es como el plano de un edificio que muestra dónde vive cada electrón. Los electrones son un poco perezosos: siempre ocupan primero los lugares con menos energía siguiendo el principio de Aufbau.
El truco está en la regla n+l: los orbitales se llenan en orden creciente de n+l. Por ejemplo, el 2p se llena después del 3s porque cuando hay empate, gana el de menor n.
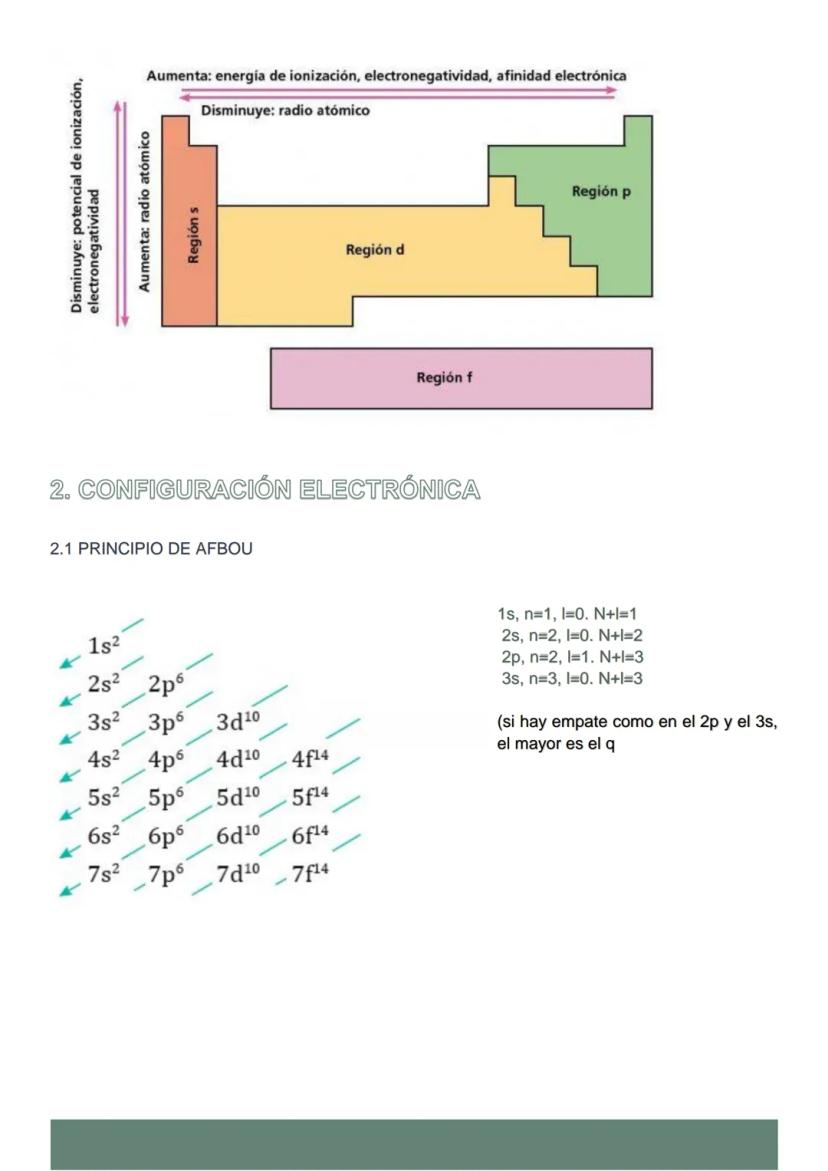
En la tabla periódica, las propiedades periódicas siguen patrones súper útiles. De izquierda a derecha aumentan la energía de ionización y la electronegatividad, pero disminuye el tamaño atómico. De arriba hacia abajo es justo lo contrario.
💡 Tip de examen: Dibuja flechas en tu tabla periódica para recordar hacia dónde aumenta cada propiedad.

Afinidad Electrónica: La Atracción por los Electrones
La afinidad electrónica mide cuánta energía se libera cuando un átomo "atrapa" un electrón extra. Es como medir qué tan desesperado está un átomo por conseguir un electrón más.
Esta propiedad sigue las mismas tendencias que la electronegatividad: aumenta hacia la derecha en un periodo porque los átomos tienen más carga nuclear efectiva y "atraen" más fuerte. Hacia abajo en un grupo disminuye porque el electrón nuevo queda más lejos del núcleo.
Los elementos del grupo 17 (halógenos) son los campeones en afinidad electrónica. El flúor y el cloro son especialmente "hambrientos" de electrones.
💡 Conexión clave: La afinidad electrónica te ayuda a predecir qué elementos formarán iones negativos fácilmente.

Electronegatividad y Enlaces Químicos
La electronegatividad es la capacidad de un átomo para "robar" electrones en un enlace covalente. Es como medir qué tan egoísta es cada elemento con los electrones.
Esta propiedad es clave para entender el carácter metálico: cuanto más electronegativo es un elemento, menos metálico se comporta. Los metales son generosos con sus electrones, mientras que los no metales son más posesivos.
Los enlaces químicos se forman porque los átomos buscan estabilidad siguiendo la regla del octeto (8 electrones en su capa externa). Para conseguirlo, pueden ceder, ganar o compartir electrones según su electronegatividad.
La diferencia de electronegatividad entre dos átomos determina qué tipo de enlace formarán: si es muy grande será iónico, si es pequeña será covalente.
💡 Truco mental: La electronegatividad aumenta hacia la esquina superior derecha de la tabla periódica (donde está el flúor).

Enlace Iónico: Cuando los Opuestos se Atraen
El enlace iónico ocurre entre un metal (que cede electrones fácilmente) y un no metal (que los acepta con gusto). Es como un matrimonio donde uno da y el otro recibe.
Cuando el litio se encuentra con el flúor, el Li pierde un electrón convirtiéndose en Li⁺, mientras que el F gana ese electrón transformándose en F⁻. Los iones resultantes se atraen formando una red cristalina súper ordenada.
La energía reticular mide qué tan fuerte es la atracción entre los iones. Cuanto mayor sea la carga de los iones y menor su tamaño, más fuerte será el enlace y más estable el compuesto.
La fórmula de un compuesto iónico solo indica la proporción mínima de iones, pero en realidad forman estructuras tridimensionales gigantes donde cada ion se rodea del máximo número posible de iones del signo opuesto.
💡 Dato curioso: Los cristales de sal que usas para cocinar son redes cristalinas de Na⁺ y Cl⁻.

Propiedades de Compuestos Iónicos y Enlace Metálico
Los compuestos iónicos tienen características muy reconocibles. Son sólidos duros pero quebradizos, con puntos de fusión altos porque hace falta mucha energía para romper esas atracciones entre iones. Se disuelven bien en agua pero solo conducen electricidad cuando están fundidos o disueltos.
El enlace metálico es completamente diferente: imagina un "mar de electrones" flotando libremente entre cationes metálicos. Los átomos metálicos ceden sus electrones de valencia a un fondo común que pertenece a todo el metal.
Esta estructura especial explica por qué los metales brillan, conducen electricidad y calor, y se pueden moldear fácilmente en hilos (ductilidad) o láminas (maleabilidad). Los electrones libres pueden moverse y transmitir energía por todo el material.
La mayoría de metales son sólidos a temperatura ambiente (excepto el mercurio) y tienen propiedades mecánicas excelentes gracias a este enlace flexible pero fuerte.
💡 Aplicación práctica: Los cables eléctricos son de cobre porque el enlace metálico permite que los electrones fluyan libremente.

Enlace Covalente: Compartir es Vivir
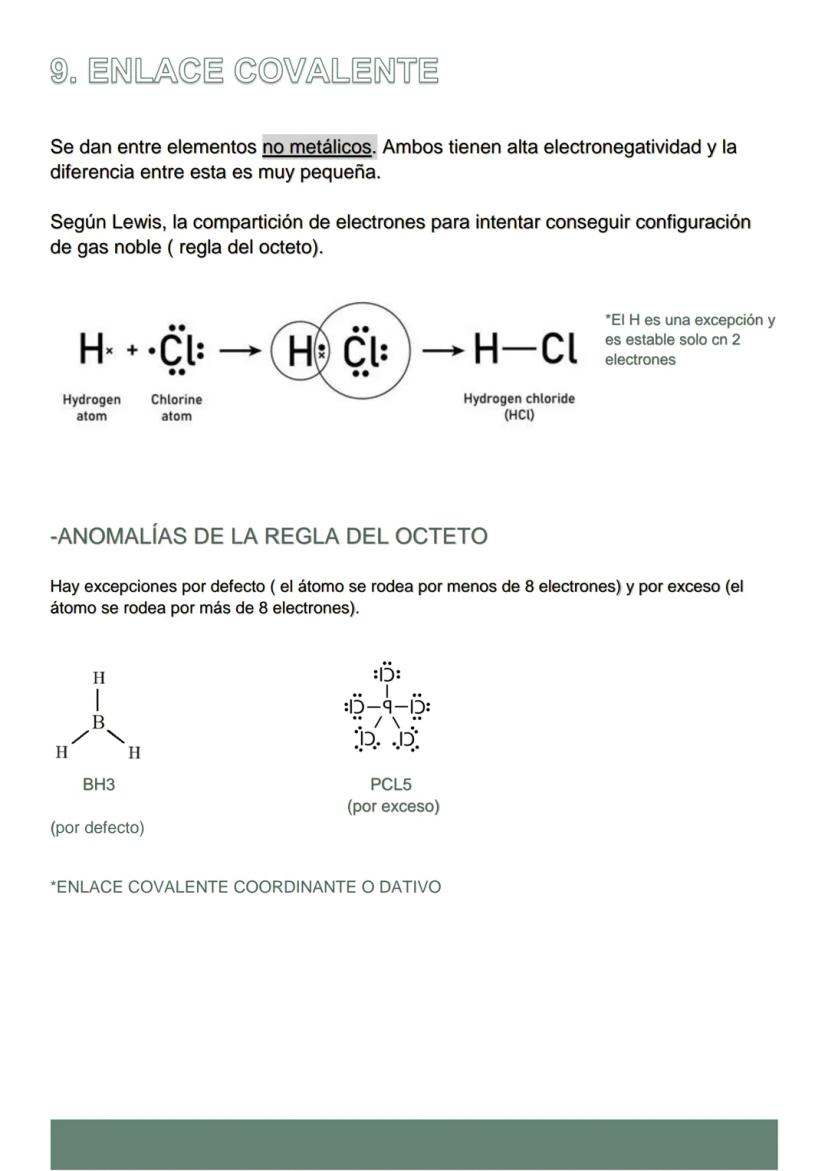
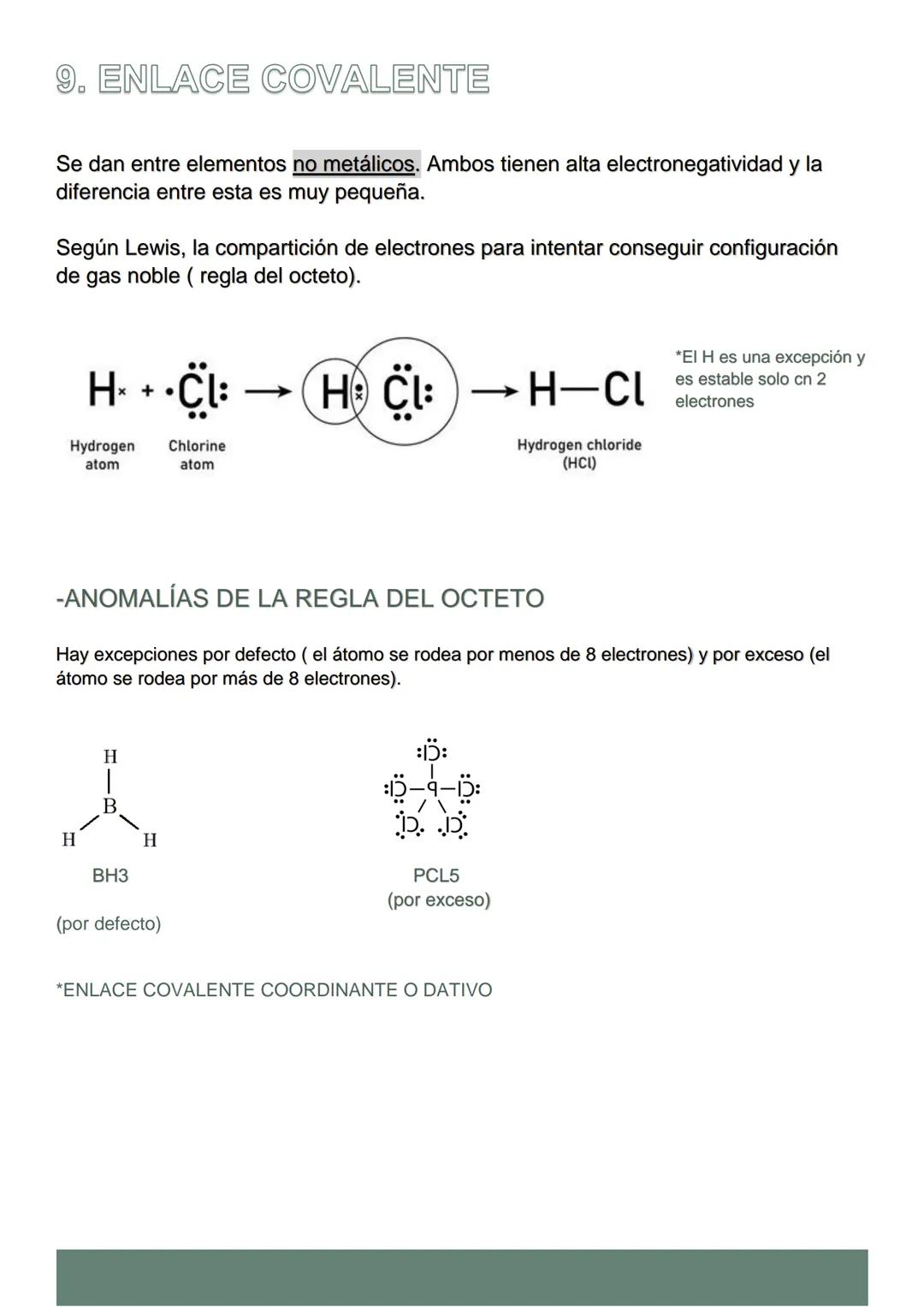
En el enlace covalente, dos átomos no metálicos con electronegatividades similares deciden compartir electrones para alcanzar la estabilidad. Es como dos amigos que comparten sus apuntes porque ambos los necesitan.
La regla del octeto explica por qué se forman estos enlaces: cada átomo busca tener 8 electrones en su capa externa (el hidrógeno solo necesita 2). Al compartir, ambos consiguen lo que quieren.
Pero cuidado: hay excepciones a la regla del octeto. Algunos átomos como el boro se conforman con menos de 8 electrones, mientras que otros como el fósforo pueden tener más de 8 (solo si están en el periodo 3 o superior).
El enlace covalente coordinado es especial: un átomo aporta ambos electrones del par compartido, pero una vez formado funciona igual que cualquier enlace covalente normal.
💡 Recuerda: El hidrógeno es la excepción más común - solo necesita 2 electrones para ser estable.
Geometría Molecular: Las Formas de las Moléculas
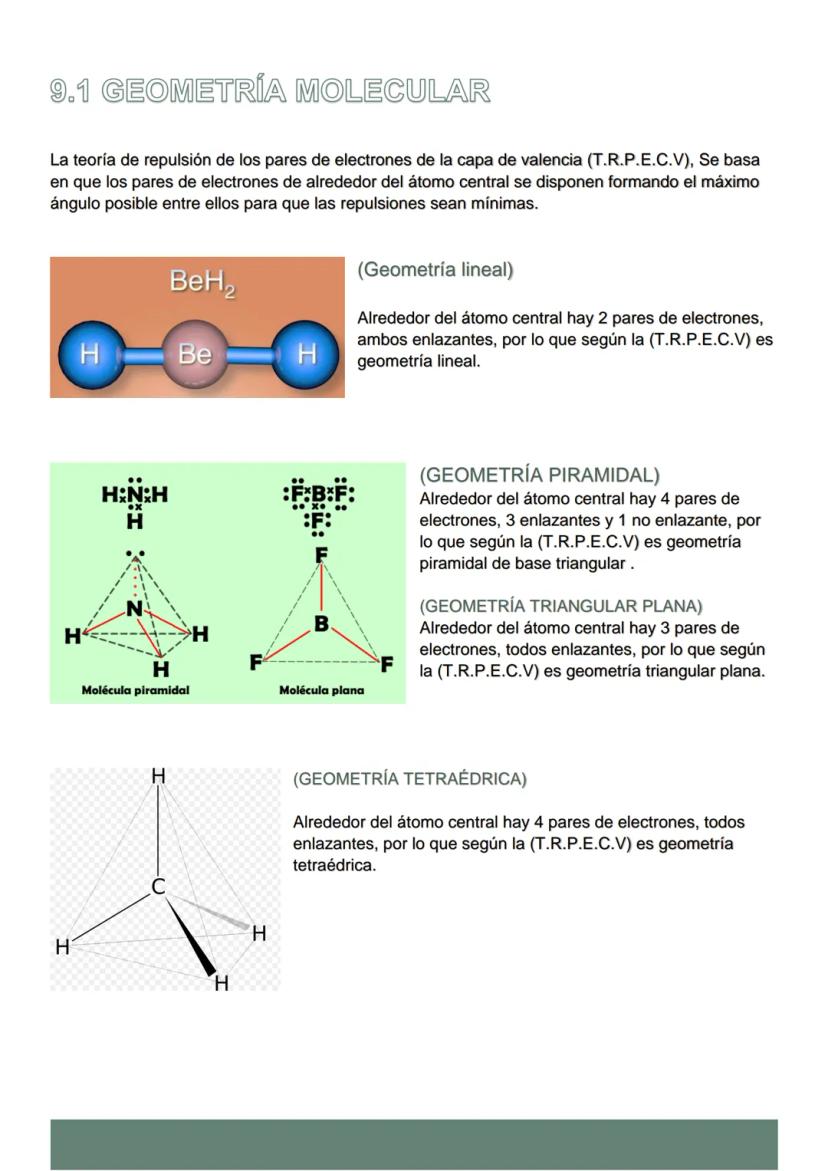
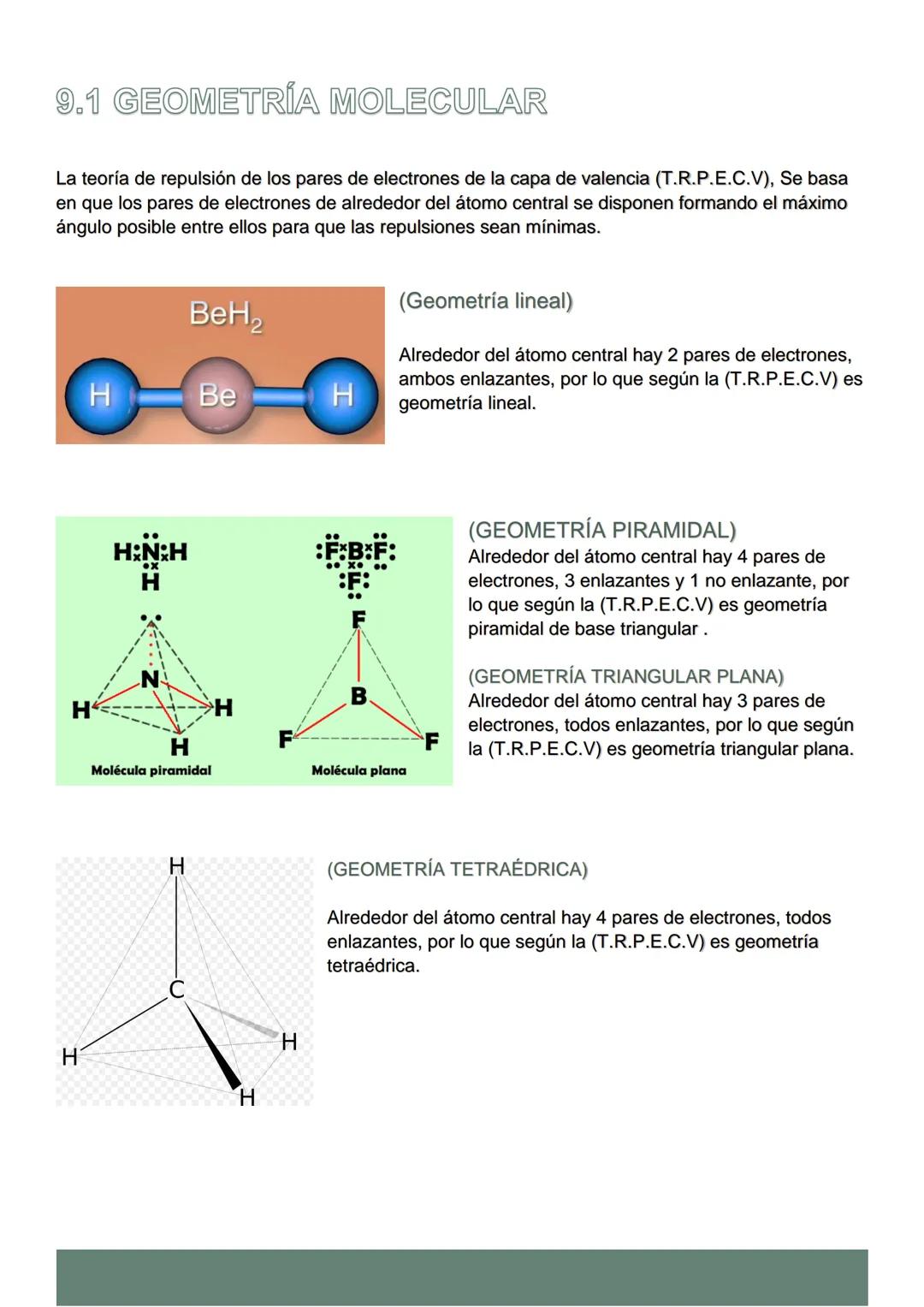
La teoría RPECV (Repulsión de Pares de Electrones de la Capa de Valencia) explica por qué las moléculas tienen formas específicas. Los pares de electrones se repelen y buscan estar lo más alejados posible entre sí.
Con 2 pares de electrones obtienes geometría lineal (como el BeH₂). Con 3 pares todos enlazantes, la molécula es triangular plana (como el BF₃). Si uno de esos 3 pares no enlaza, la geometría se vuelve angular (como el SnCl₂).
Cuando hay 4 pares de electrones, si todos enlazan tienes geometría tetraédrica (como el CH₄). Pero si uno no enlaza, la forma cambia a piramidal (como el NH₃).
La forma de las moléculas es crucial para entender sus propiedades: determina si serán polares o apolares, su reactividad y cómo interactúan con otras moléculas.
💡 Visualiza: Usa palillos y plastilina para construir modelos 3D - te ayudará muchísimo a entender las geometrías.
Polaridad: Cuando los Electrones Tienen Favoritos
La polaridad de enlace depende de si los átomos comparten los electrones equitativamente o no. Si ambos átomos tienen la misma electronegatividad, el enlace es apolar - los electrones se reparten fifty-fifty.
Pero si un átomo es más electronegativo, "tira" más fuerte de los electrones creando un enlace polar. El átomo más electronegativo queda ligeramente negativo (δ-) y el otro ligeramente positivo (δ+).
Las fuerzas intermoleculares mantienen las moléculas unidas y determinan propiedades como los puntos de ebullición. Las fuerzas de van der Waals actúan entre moléculas polares - cuanto más polar, más fuerte la atracción.
Las fuerzas de London son las más débiles y actúan entre moléculas apolares. Aumentan con la masa molecular, por eso el I₂ es sólido mientras que el Cl₂ es gas.
💡 Conexión útil: Las diferencias de electronegatividad pequeñas (menos de 0,4) dan enlaces apolares, grandes (más de 1,7) dan enlaces iónicos.

Fuerzas de London y Puentes de Hidrógeno
Las fuerzas de London son súper débiles pero universales - incluso las moléculas más apolares como el H₂ o Br₂ las experimentan. Se deben a fluctuaciones temporales en la distribución de electrones que crean dipolos instantáneos.
Estas fuerzas explican por qué el Cl₂ es gas, el Br₂ es líquido y el I₂ es sólido a temperatura ambiente. A mayor masa molecular, mayor superficie de contacto y fuerzas de London más intensas.
Los puentes de hidrógeno son las fuerzas intermoleculares más fuertes. Se forman cuando el hidrógeno está unido a flúor, oxígeno o nitrógeno (los elementos más electronegativos y pequeños).
Estos puentes explican por qué el agua tiene propiedades tan especiales: punto de ebullición alto, capacidad de disolver muchas sustancias, y por qué el hielo flota. Sin puentes de hidrógeno, ¡la vida tal como la conocemos sería imposible!
💡 Ejemplo clave: Los puentes de hidrógeno mantienen unidas las dos cadenas del ADN - literalmente sostienen la vida.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: modelo atómico
9Formulación Inorgánica Química 1°BACH
Guía con lo necesario para formular y trucos
mol,moleculas,atomos
como calcular los moles moleculas sus gramos etc
Modelos atomicos
Apuntes de modelos atómicos
El átomo
Explicación de los modelos atómicos, número atómico y másico, tabla periódica, propiedades periódicas de los elementos, electrones desapareados, enlaces y diagrama de Lewis.
Estructura de lewis
Os gusta?
Modelos atómicos de Dalton, THomson, Rutherford y Bohr
Presentación
Átomo
Incluye las propiedades del átomo y los tipos de enlaces
Los átomos
esquema/resumen los átomos
Estructura anatómica
Estructura anatómica modelos atómicos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Introducción a la Estructura Atómica y Enlaces Químicos en el Sistema Periódico
¡Prepárate para dominar uno de los temas más importantes de química! Vamos a explorar desde cómo están organizados los electrones en los átomos hasta cómo se forman los diferentes tipos de enlaces químicos que mantienen unida toda la materia que... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Números Cuánticos: El GPS de los Electrones
¿Te has preguntado cómo podemos localizar un electrón en un átomo? Los números cuánticos son como las coordenadas GPS que nos dicen exactamente dónde encontrar cada electrón.
El número cuántico principal (n) te dice en qué "piso" vive el electrón. Cuanto más alto el número (1, 2, 3...), más lejos del núcleo y con más energía está el electrón.
El número cuántico orbital (l) define el "tipo de habitación": l=0 son orbitales s (esféricos), l=1 son orbitales p (con forma de ocho), l=2 son orbitales d, y l=3 son orbitales f. El número magnético (ml) indica hacia dónde apunta el orbital en el espacio, mientras que el número de espín (ms) nos dice si el electrón gira hacia arriba (+1/2) o hacia abajo (-1/2).
💡 Recuerda: Cada electrón tiene su propia "dirección" única definida por estos cuatro números cuánticos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Configuración Electrónica y el Sistema Periódico
La configuración electrónica es como el plano de un edificio que muestra dónde vive cada electrón. Los electrones son un poco perezosos: siempre ocupan primero los lugares con menos energía siguiendo el principio de Aufbau.
El truco está en la regla n+l: los orbitales se llenan en orden creciente de n+l. Por ejemplo, el 2p se llena después del 3s porque cuando hay empate, gana el de menor n.
En la tabla periódica, las propiedades periódicas siguen patrones súper útiles. De izquierda a derecha aumentan la energía de ionización y la electronegatividad, pero disminuye el tamaño atómico. De arriba hacia abajo es justo lo contrario.
💡 Tip de examen: Dibuja flechas en tu tabla periódica para recordar hacia dónde aumenta cada propiedad.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Afinidad Electrónica: La Atracción por los Electrones
La afinidad electrónica mide cuánta energía se libera cuando un átomo "atrapa" un electrón extra. Es como medir qué tan desesperado está un átomo por conseguir un electrón más.
Esta propiedad sigue las mismas tendencias que la electronegatividad: aumenta hacia la derecha en un periodo porque los átomos tienen más carga nuclear efectiva y "atraen" más fuerte. Hacia abajo en un grupo disminuye porque el electrón nuevo queda más lejos del núcleo.
Los elementos del grupo 17 (halógenos) son los campeones en afinidad electrónica. El flúor y el cloro son especialmente "hambrientos" de electrones.
💡 Conexión clave: La afinidad electrónica te ayuda a predecir qué elementos formarán iones negativos fácilmente.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Electronegatividad y Enlaces Químicos
La electronegatividad es la capacidad de un átomo para "robar" electrones en un enlace covalente. Es como medir qué tan egoísta es cada elemento con los electrones.
Esta propiedad es clave para entender el carácter metálico: cuanto más electronegativo es un elemento, menos metálico se comporta. Los metales son generosos con sus electrones, mientras que los no metales son más posesivos.
Los enlaces químicos se forman porque los átomos buscan estabilidad siguiendo la regla del octeto (8 electrones en su capa externa). Para conseguirlo, pueden ceder, ganar o compartir electrones según su electronegatividad.
La diferencia de electronegatividad entre dos átomos determina qué tipo de enlace formarán: si es muy grande será iónico, si es pequeña será covalente.
💡 Truco mental: La electronegatividad aumenta hacia la esquina superior derecha de la tabla periódica (donde está el flúor).

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace Iónico: Cuando los Opuestos se Atraen
El enlace iónico ocurre entre un metal (que cede electrones fácilmente) y un no metal (que los acepta con gusto). Es como un matrimonio donde uno da y el otro recibe.
Cuando el litio se encuentra con el flúor, el Li pierde un electrón convirtiéndose en Li⁺, mientras que el F gana ese electrón transformándose en F⁻. Los iones resultantes se atraen formando una red cristalina súper ordenada.
La energía reticular mide qué tan fuerte es la atracción entre los iones. Cuanto mayor sea la carga de los iones y menor su tamaño, más fuerte será el enlace y más estable el compuesto.
La fórmula de un compuesto iónico solo indica la proporción mínima de iones, pero en realidad forman estructuras tridimensionales gigantes donde cada ion se rodea del máximo número posible de iones del signo opuesto.
💡 Dato curioso: Los cristales de sal que usas para cocinar son redes cristalinas de Na⁺ y Cl⁻.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades de Compuestos Iónicos y Enlace Metálico
Los compuestos iónicos tienen características muy reconocibles. Son sólidos duros pero quebradizos, con puntos de fusión altos porque hace falta mucha energía para romper esas atracciones entre iones. Se disuelven bien en agua pero solo conducen electricidad cuando están fundidos o disueltos.
El enlace metálico es completamente diferente: imagina un "mar de electrones" flotando libremente entre cationes metálicos. Los átomos metálicos ceden sus electrones de valencia a un fondo común que pertenece a todo el metal.
Esta estructura especial explica por qué los metales brillan, conducen electricidad y calor, y se pueden moldear fácilmente en hilos (ductilidad) o láminas (maleabilidad). Los electrones libres pueden moverse y transmitir energía por todo el material.
La mayoría de metales son sólidos a temperatura ambiente (excepto el mercurio) y tienen propiedades mecánicas excelentes gracias a este enlace flexible pero fuerte.
💡 Aplicación práctica: Los cables eléctricos son de cobre porque el enlace metálico permite que los electrones fluyan libremente.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace Covalente: Compartir es Vivir
En el enlace covalente, dos átomos no metálicos con electronegatividades similares deciden compartir electrones para alcanzar la estabilidad. Es como dos amigos que comparten sus apuntes porque ambos los necesitan.
La regla del octeto explica por qué se forman estos enlaces: cada átomo busca tener 8 electrones en su capa externa (el hidrógeno solo necesita 2). Al compartir, ambos consiguen lo que quieren.
Pero cuidado: hay excepciones a la regla del octeto. Algunos átomos como el boro se conforman con menos de 8 electrones, mientras que otros como el fósforo pueden tener más de 8 (solo si están en el periodo 3 o superior).
El enlace covalente coordinado es especial: un átomo aporta ambos electrones del par compartido, pero una vez formado funciona igual que cualquier enlace covalente normal.
💡 Recuerda: El hidrógeno es la excepción más común - solo necesita 2 electrones para ser estable.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Geometría Molecular: Las Formas de las Moléculas
La teoría RPECV (Repulsión de Pares de Electrones de la Capa de Valencia) explica por qué las moléculas tienen formas específicas. Los pares de electrones se repelen y buscan estar lo más alejados posible entre sí.
Con 2 pares de electrones obtienes geometría lineal (como el BeH₂). Con 3 pares todos enlazantes, la molécula es triangular plana (como el BF₃). Si uno de esos 3 pares no enlaza, la geometría se vuelve angular (como el SnCl₂).
Cuando hay 4 pares de electrones, si todos enlazan tienes geometría tetraédrica (como el CH₄). Pero si uno no enlaza, la forma cambia a piramidal (como el NH₃).
La forma de las moléculas es crucial para entender sus propiedades: determina si serán polares o apolares, su reactividad y cómo interactúan con otras moléculas.
💡 Visualiza: Usa palillos y plastilina para construir modelos 3D - te ayudará muchísimo a entender las geometrías.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Polaridad: Cuando los Electrones Tienen Favoritos
La polaridad de enlace depende de si los átomos comparten los electrones equitativamente o no. Si ambos átomos tienen la misma electronegatividad, el enlace es apolar - los electrones se reparten fifty-fifty.
Pero si un átomo es más electronegativo, "tira" más fuerte de los electrones creando un enlace polar. El átomo más electronegativo queda ligeramente negativo (δ-) y el otro ligeramente positivo (δ+).
Las fuerzas intermoleculares mantienen las moléculas unidas y determinan propiedades como los puntos de ebullición. Las fuerzas de van der Waals actúan entre moléculas polares - cuanto más polar, más fuerte la atracción.
Las fuerzas de London son las más débiles y actúan entre moléculas apolares. Aumentan con la masa molecular, por eso el I₂ es sólido mientras que el Cl₂ es gas.
💡 Conexión útil: Las diferencias de electronegatividad pequeñas (menos de 0,4) dan enlaces apolares, grandes (más de 1,7) dan enlaces iónicos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fuerzas de London y Puentes de Hidrógeno
Las fuerzas de London son súper débiles pero universales - incluso las moléculas más apolares como el H₂ o Br₂ las experimentan. Se deben a fluctuaciones temporales en la distribución de electrones que crean dipolos instantáneos.
Estas fuerzas explican por qué el Cl₂ es gas, el Br₂ es líquido y el I₂ es sólido a temperatura ambiente. A mayor masa molecular, mayor superficie de contacto y fuerzas de London más intensas.
Los puentes de hidrógeno son las fuerzas intermoleculares más fuertes. Se forman cuando el hidrógeno está unido a flúor, oxígeno o nitrógeno (los elementos más electronegativos y pequeños).
Estos puentes explican por qué el agua tiene propiedades tan especiales: punto de ebullición alto, capacidad de disolver muchas sustancias, y por qué el hielo flota. Sin puentes de hidrógeno, ¡la vida tal como la conocemos sería imposible!
💡 Ejemplo clave: Los puentes de hidrógeno mantienen unidas las dos cadenas del ADN - literalmente sostienen la vida.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: modelo atómico
9Formulación Inorgánica Química 1°BACH
Guía con lo necesario para formular y trucos
mol,moleculas,atomos
como calcular los moles moleculas sus gramos etc
Modelos atomicos
Apuntes de modelos atómicos
El átomo
Explicación de los modelos atómicos, número atómico y másico, tabla periódica, propiedades periódicas de los elementos, electrones desapareados, enlaces y diagrama de Lewis.
Estructura de lewis
Os gusta?
Modelos atómicos de Dalton, THomson, Rutherford y Bohr
Presentación
Átomo
Incluye las propiedades del átomo y los tipos de enlaces
Los átomos
esquema/resumen los átomos
Estructura anatómica
Estructura anatómica modelos atómicos
Contenidos más populares de Física y Química
9Descubriendo la Física y Química: Conceptos Medios
Explora los fundamentos de la física y química con este conjunto de tarjetas de estudio diseñado para estudiantes de 8vo grado. ¡Aprende de manera divertida y efectiva!
física y química: reacciones químic
Conceptos clave sobre reacciones químicas, incluyendo reactivos y productos, para entender las transformaciones de la materia.
Símbolos y Nombres de Elementos Químicos
Identifica los símbolos químicos y nombres de los elementos más comunes presentes en la tabla periódica.
Química Orgánica
Apuntes sobre cómo hacer química orgánico con ejemplos
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Formulación orgánica apuntes con ejercicios
apuntes bien redactados y hechos
Cinematica 4ESO/1BAT/2BAT/EVAU
aqui os dejo mis apuntes de cinematica, si no entendeis algo me podeis hablar sin compromiso por insta: marieta__15 <3
basic de energía fyq
Aprende los fundamentos de la biología y geología de manera fácil y divertida con este conjunto de tarjetas de estudio.
química examen
Conceptos clave sobre reacciones químicas, teoría de colisiones y catalizadores para comprender procesos químicos.
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.