¡Prepárate para entender cómo funciona la química a nivel atómico... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
1,129
•
Actualizado May 9, 2026
•
¡Prepárate para entender cómo funciona la química a nivel atómico... Mostrar más










¿Te has preguntado por qué las reacciones químicas siguen patrones tan precisos? Todo empezó con tres leyes ponderales fundamentales que cambiaron la química para siempre.
La ley de Lavoisier nos dice que en una reacción química la masa se conserva - nada desaparece mágicamente. La ley de Proust estableció que los elementos siempre se combinan en proporciones fijas de masa. Y la ley de Dalton demostró que cuando un elemento se combina con cantidades fijas de otro para formar diferentes compuestos, lo hace en proporciones de números enteros sencillos.
Dalton revolucionó todo esto con su teoría atómica en 1803. Propuso que los elementos están formados por átomos indestructibles, que los átomos del mismo elemento son idénticos, y que los compuestos se forman por unión de átomos en proporciones numéricas sencillas.
Para determinar masas atómicas, los químicos comparaban las proporciones en que se combinaban los elementos. Por ejemplo, si el azufre se combina con hierro en proporción 1:1,74, significa que el átomo de hierro es 1,74 veces más pesado que el de azufre. Actualmente usamos como referencia la doceava parte del carbono-12.
Dato curioso: La determinación de masas atómicas precisas llevó más de 50 años de investigación y múltiples métodos experimentales.

Los isótopos son átomos del mismo elemento con diferente número de neutrones - químicamente idénticos pero con distintas masas. Esto explica por qué las masas atómicas de la tabla periódica no son números enteros: son promedios ponderados de todos los isótopos naturales.
El mol es tu mejor amigo en química - piénsalo como la "docena del químico". Un mol contiene exactamente 6,022 × 10²³ partículas (número de Avogadro), ya sean átomos, moléculas o iones.
La fórmula clave es n = m/Mm, donde n son los moles, m es la masa en gramos y Mm es la masa molecular. Esto significa que un mol de cualquier sustancia tiene una masa en gramos igual a su masa atómica o molecular.
En las reacciones químicas, los coeficientes estequiométricos te indican directamente la proporción de moles. Por ejemplo, en Cl₂ + H₂ → 2HCl, un mol de cloro reacciona con un mol de hidrógeno para producir dos moles de cloruro de hidrógeno.
Truco de estudio: Memoriza que 1 mol = masa molecular en gramos = 6,022 × 10²³ partículas. Esta relación resolverá la mayoría de problemas estequiométricos.

Los gases siguen patrones predecibles que puedes dominar fácilmente. La ley de Boyle dice que presión y volumen son inversamente proporcionales . La ley de Charles establece que volumen y temperatura son directamente proporcionales .
La ecuación general PV = nRT es tu herramienta más poderosa. Aquí R = 0,082 cuando usas atmósferas, litros y Kelvin. Esta ecuación te permite calcular cualquier variable si conoces las otras tres.
Un mol de cualquier gas ocupa 22,4 L a condiciones normales (0°C y 1 atm) - esto es el volumen molar. No importa si es hidrógeno o dióxido de carbono, siempre 22,4 L por mol.
La ley de Dalton para presiones parciales dice que cada gas en una mezcla contribuye a la presión total según su fracción molar: Pi = XiPt. Esto es crucial para entender cómo funcionan los tanques de buceo o la respiración en altitud.
Para calcular la densidad de un gas usa: PMm = dRT. Esta fórmula te permite encontrar la masa molecular de un gas desconocido midiendo su densidad.
Consejo práctico: Siempre convierte temperatura a Kelvin y presión a atmósferas antes de usar PV = nRT.

En las mezclas de gases, es fundamental entender que el porcentaje en volumen = porcentaje en presión = porcentaje en moles, pero NO igual al porcentaje en masa. Esto se debe a que las moléculas tienen masas diferentes.
La masa molecular aparente de una mezcla se calcula como: Mma = Σ(Xi × Mmi), donde Xi es la fracción molar de cada componente.
Para determinar fórmulas empíricas, sigue estos pasos: convierte porcentajes a gramos (asume 100g de muestra), divide cada masa por su masa atómica para obtener moles, divide todos los valores entre el menor para obtener proporciones, y aproxima a números enteros.
Si te sale algo como 2,5 o 1,5, multiplica todos los valores por 2. Si sale 2,33 o 1,67, multiplica por 3. La clave es buscar la relación de números enteros más simple.
Para la fórmula molecular, necesitas la masa molecular real. Usa datos experimentales (como densidad de gases) para calcularla con PV = nRT, luego divide la masa molecular real entre la de tu fórmula empírica. Ese cociente te dice cuántas veces debes multiplicar la fórmula empírica.
Error común: No confundas fórmula empírica (C₃H₆O) con molecular (C₆H₁₂O₂). La empírica es la proporción más simple, la molecular es la cantidad real de átomos.

Continuando con nuestro ejemplo práctico: partiendo de 62,1% C, 10,3% H y 27,6% O, obtuvimos proporciones molares de 5,18:10,3:1,73. Dividiendo entre el menor (1,73), conseguimos 3:6:1, dándonos la fórmula empírica C₃H₆O.
Para encontrar la fórmula molecular, usamos datos experimentales: 2,5g de la sustancia ocupan 800 mL a 1,05 atm y 200°C. Aplicando PV = nRT en la forma Mm = mRT/PV:
Mm = (2,5 × 0,082 × 473)/(1,05 × 0,8) = 115,4 g/mol
Como la masa de C₃H₆O es 58 g/mol, tenemos: n = 115,4/58 ≈ 2. Por tanto, la fórmula molecular es (C₃H₆O)₂ = C₆H₁₂O₂.
Es normal que n no sea exactamente un número entero debido a errores experimentales - valores como 1,95 o 2,03 se redondean a 2. Lo importante es que siempre debe estar cerca de un número entero.
Recuerda que el resultado final no se escribe como (C₃H₆O)₂, sino desarrollado: C₆H₁₂O₂. Esta diferencia es importante en exámenes.
Estrategia de examen: Si te dan datos de gases (P, V, T), seguramente necesitarás calcular la masa molecular para encontrar la fórmula molecular completa.

Las disoluciones son mezclas homogéneas donde puedes distinguir el disolvente (mayor cantidad) y el soluto (menor cantidad). Sin embargo, en mezclas sólido-líquido, por convención llamamos disolvente al líquido aunque esté en menor proporción.
Existen varios tipos: diluidas (poco soluto), concentradas (mucho soluto) y saturadas (máximo soluto posible a esa temperatura). Una disolución saturada puede ser diluida o concentrada según la solubilidad del soluto.
Las formas más importantes de expresar concentración son:
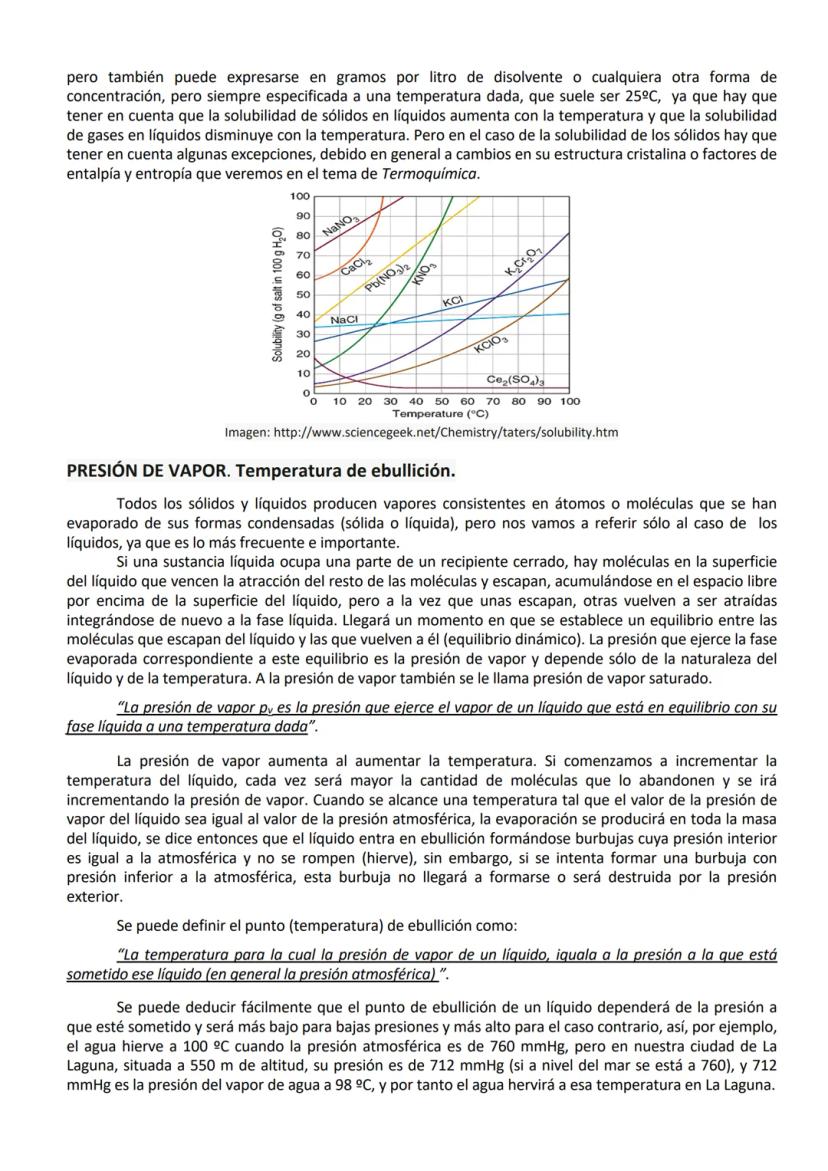
La solubilidad es la cantidad máxima de soluto que se disuelve en una cantidad dada de disolvente a temperatura específica. Para sólidos en líquidos, la solubilidad aumenta con la temperatura; para gases en líquidos, disminuye con la temperatura.
Tip de laboratorio: La molalidad es independiente de la temperatura (usa masa), mientras que la molaridad sí depende (usa volumen que varía con T).

La presión de vapor es la presión que ejerce el vapor de un líquido en equilibrio con su fase líquida. Imagínate moléculas escapando de la superficie del líquido y otras regresando - cuando se igualan, tienes equilibrio dinámico.
Esta presión aumenta con la temperatura y es característica de cada sustancia. Cuando la presión de vapor iguala a la presión atmosférica, el líquido hierve. Por eso el agua hierve a 100°C al nivel del mar (1 atm), pero a menor temperatura en las montañas donde la presión es menor.
En La Laguna (550m de altitud), la presión es ~712 mmHg, por lo que el agua hierve a 98°C. Este principio explica por qué es difícil hacer un buen té en las montañas - el agua hierve antes de alcanzar 100°C.
La olla a presión funciona al revés: aumenta la presión interior hasta ~2,3 atm, obligando al agua a hervir a 120-125°C. La cocción es más rápida porque la temperatura es mayor.
La temperatura de ebullición es aquella donde la presión de vapor del líquido iguala la presión externa. Es un concepto relativo - no hay una temperatura fija de ebullición sin especificar la presión.
Conexión real: Por esto los alpinistas usan ollas a presión - compensan la menor presión atmosférica de la altitud para cocinar eficientemente.

Las propiedades coligativas son fascinantes porque dependen solo del número de partículas disueltas, no de su naturaleza. Son cuatro: descenso de presión de vapor, aumento del punto de ebullición, descenso del punto de congelación y presión osmótica.
El descenso de la presión de vapor sigue la ley de Raoult: P = Xdisolvente × P₀. Cuando añades soluto no volátil, reduces la fracción molar del disolvente y por tanto su presión de vapor. Menos moléculas de disolvente en la superficie significa menor evaporación.
El aumento de la temperatura de ebullición (ebullioscopía) usa la fórmula: Te = Te₀ + Ke × m. Como la presión de vapor es menor, necesitas más temperatura para igualar la presión atmosférica. Ke es la constante ebulloscópica del disolvente.
El descenso de la temperatura de congelación (crioscopía) sigue: Tc = Tc₀ - Kc × m. La congelación ocurre cuando las presiones de vapor del líquido y sólido se igualan. El soluto retrasa este equilibrio.
Aplicaciones prácticas: Los anticongelantes del coche bajan el punto de congelación del agua (evitan roturas del radiador) y suben el de ebullición (evitan sobrecalentamiento). También puedes determinar masas moleculares midiendo estas propiedades.
Dato útil: En química forense se usa crioscopía para determinar la concentración de alcohol en sangre y otros fluidos biológicos.

La ósmosis es el movimiento de disolvente a través de una membrana semipermeable desde la disolución diluida hacia la concentrada, hasta igualar concentraciones. La presión osmótica (Π) es la presión necesaria para detener este flujo.
La fórmula de Van't Hoff es: Π = CRT, equivalente a ΠV = nRT (¡como los gases!). Aquí C es la molaridad, R = 0,082 atm·L/(K·mol) y T en Kelvin.
El osmómetro mide esta presión usando un émbolo que se eleva hasta que la presión de la columna líquida equilibra la presión osmótica. Es como un manómetro especializado.
La ósmosis inversa aplica presión superior a la osmótica para forzar el paso de disolvente hacia la disolución diluida. Así funcionan las plantas desalinizadoras - aplican presión al agua salada para obtener agua pura.
Las disoluciones isotónicas tienen igual presión osmótica que las células. Las bebidas isotónicas mantienen este equilibrio para evitar deshidratación o hinchazón celular. Las hipertónicas (más concentradas) deshidratan células, las hipotónicas (menos concentradas) las hinchan.
En medicina, los sueros intravenosos deben ser isotónicos para no dañar glóbulos rojos - de lo contrario se arrugarían o explotarían.
Curiosidad biológica: Las plantas marchitas recuperan turgencia cuando les das agua porque las células absorben agua por ósmosis hasta equilibrar las concentraciones.

Los solutos iónicos complican un poco el panorama porque se disocian en iones. Cuando NaCl se disuelve: NaCl → Na⁺ + Cl⁻, obtienes dos partículas por cada unidad de soluto original.
Para las propiedades coligativas, esto significa que debes multiplicar la concentración por el número de iones producidos. Si 0,1 M de NaCl produce 0,2 M de partículas totales , el efecto coligativo se duplica.
Las fórmulas siguen siendo las mismas, pero incluyes un factor de multiplicación igual al número de iones. Para NaCl es 2, para CaCl₂ es 3 , para Al₂(SO₄)₃ sería 5 .
Este concepto explica por qué la sal es más efectiva que el azúcar para derretir hielo en las carreteras - produce más partículas por mol disuelto. También por qué el suero fisiológico (NaCl al 0,9%) es isotónico aunque parezca una concentración baja.
En la práctica, la disociación no siempre es completa debido a la formación de pares iónicos, especialmente en disoluciones concentradas. Pero para cálculos básicos, asumimos disociación completa.
Aplicación real: Los deportistas pierden electrolitos (iones) al sudar, no solo agua. Las bebidas deportivas reponen estos iones para mantener el equilibrio osmótico celular.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
¡Prepárate para entender cómo funciona la química a nivel atómico y molecular! Este tema te llevará desde las leyes básicas que rigen las reacciones químicas hasta comprender por qué el agua hierve a diferentes temperaturas según la altitud y cómo... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Te has preguntado por qué las reacciones químicas siguen patrones tan precisos? Todo empezó con tres leyes ponderales fundamentales que cambiaron la química para siempre.
La ley de Lavoisier nos dice que en una reacción química la masa se conserva - nada desaparece mágicamente. La ley de Proust estableció que los elementos siempre se combinan en proporciones fijas de masa. Y la ley de Dalton demostró que cuando un elemento se combina con cantidades fijas de otro para formar diferentes compuestos, lo hace en proporciones de números enteros sencillos.
Dalton revolucionó todo esto con su teoría atómica en 1803. Propuso que los elementos están formados por átomos indestructibles, que los átomos del mismo elemento son idénticos, y que los compuestos se forman por unión de átomos en proporciones numéricas sencillas.
Para determinar masas atómicas, los químicos comparaban las proporciones en que se combinaban los elementos. Por ejemplo, si el azufre se combina con hierro en proporción 1:1,74, significa que el átomo de hierro es 1,74 veces más pesado que el de azufre. Actualmente usamos como referencia la doceava parte del carbono-12.
Dato curioso: La determinación de masas atómicas precisas llevó más de 50 años de investigación y múltiples métodos experimentales.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los isótopos son átomos del mismo elemento con diferente número de neutrones - químicamente idénticos pero con distintas masas. Esto explica por qué las masas atómicas de la tabla periódica no son números enteros: son promedios ponderados de todos los isótopos naturales.
El mol es tu mejor amigo en química - piénsalo como la "docena del químico". Un mol contiene exactamente 6,022 × 10²³ partículas (número de Avogadro), ya sean átomos, moléculas o iones.
La fórmula clave es n = m/Mm, donde n son los moles, m es la masa en gramos y Mm es la masa molecular. Esto significa que un mol de cualquier sustancia tiene una masa en gramos igual a su masa atómica o molecular.
En las reacciones químicas, los coeficientes estequiométricos te indican directamente la proporción de moles. Por ejemplo, en Cl₂ + H₂ → 2HCl, un mol de cloro reacciona con un mol de hidrógeno para producir dos moles de cloruro de hidrógeno.
Truco de estudio: Memoriza que 1 mol = masa molecular en gramos = 6,022 × 10²³ partículas. Esta relación resolverá la mayoría de problemas estequiométricos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los gases siguen patrones predecibles que puedes dominar fácilmente. La ley de Boyle dice que presión y volumen son inversamente proporcionales . La ley de Charles establece que volumen y temperatura son directamente proporcionales .
La ecuación general PV = nRT es tu herramienta más poderosa. Aquí R = 0,082 cuando usas atmósferas, litros y Kelvin. Esta ecuación te permite calcular cualquier variable si conoces las otras tres.
Un mol de cualquier gas ocupa 22,4 L a condiciones normales (0°C y 1 atm) - esto es el volumen molar. No importa si es hidrógeno o dióxido de carbono, siempre 22,4 L por mol.
La ley de Dalton para presiones parciales dice que cada gas en una mezcla contribuye a la presión total según su fracción molar: Pi = XiPt. Esto es crucial para entender cómo funcionan los tanques de buceo o la respiración en altitud.
Para calcular la densidad de un gas usa: PMm = dRT. Esta fórmula te permite encontrar la masa molecular de un gas desconocido midiendo su densidad.
Consejo práctico: Siempre convierte temperatura a Kelvin y presión a atmósferas antes de usar PV = nRT.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
En las mezclas de gases, es fundamental entender que el porcentaje en volumen = porcentaje en presión = porcentaje en moles, pero NO igual al porcentaje en masa. Esto se debe a que las moléculas tienen masas diferentes.
La masa molecular aparente de una mezcla se calcula como: Mma = Σ(Xi × Mmi), donde Xi es la fracción molar de cada componente.
Para determinar fórmulas empíricas, sigue estos pasos: convierte porcentajes a gramos (asume 100g de muestra), divide cada masa por su masa atómica para obtener moles, divide todos los valores entre el menor para obtener proporciones, y aproxima a números enteros.
Si te sale algo como 2,5 o 1,5, multiplica todos los valores por 2. Si sale 2,33 o 1,67, multiplica por 3. La clave es buscar la relación de números enteros más simple.
Para la fórmula molecular, necesitas la masa molecular real. Usa datos experimentales (como densidad de gases) para calcularla con PV = nRT, luego divide la masa molecular real entre la de tu fórmula empírica. Ese cociente te dice cuántas veces debes multiplicar la fórmula empírica.
Error común: No confundas fórmula empírica (C₃H₆O) con molecular (C₆H₁₂O₂). La empírica es la proporción más simple, la molecular es la cantidad real de átomos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Continuando con nuestro ejemplo práctico: partiendo de 62,1% C, 10,3% H y 27,6% O, obtuvimos proporciones molares de 5,18:10,3:1,73. Dividiendo entre el menor (1,73), conseguimos 3:6:1, dándonos la fórmula empírica C₃H₆O.
Para encontrar la fórmula molecular, usamos datos experimentales: 2,5g de la sustancia ocupan 800 mL a 1,05 atm y 200°C. Aplicando PV = nRT en la forma Mm = mRT/PV:
Mm = (2,5 × 0,082 × 473)/(1,05 × 0,8) = 115,4 g/mol
Como la masa de C₃H₆O es 58 g/mol, tenemos: n = 115,4/58 ≈ 2. Por tanto, la fórmula molecular es (C₃H₆O)₂ = C₆H₁₂O₂.
Es normal que n no sea exactamente un número entero debido a errores experimentales - valores como 1,95 o 2,03 se redondean a 2. Lo importante es que siempre debe estar cerca de un número entero.
Recuerda que el resultado final no se escribe como (C₃H₆O)₂, sino desarrollado: C₆H₁₂O₂. Esta diferencia es importante en exámenes.
Estrategia de examen: Si te dan datos de gases (P, V, T), seguramente necesitarás calcular la masa molecular para encontrar la fórmula molecular completa.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las disoluciones son mezclas homogéneas donde puedes distinguir el disolvente (mayor cantidad) y el soluto (menor cantidad). Sin embargo, en mezclas sólido-líquido, por convención llamamos disolvente al líquido aunque esté en menor proporción.
Existen varios tipos: diluidas (poco soluto), concentradas (mucho soluto) y saturadas (máximo soluto posible a esa temperatura). Una disolución saturada puede ser diluida o concentrada según la solubilidad del soluto.
Las formas más importantes de expresar concentración son:
La solubilidad es la cantidad máxima de soluto que se disuelve en una cantidad dada de disolvente a temperatura específica. Para sólidos en líquidos, la solubilidad aumenta con la temperatura; para gases en líquidos, disminuye con la temperatura.
Tip de laboratorio: La molalidad es independiente de la temperatura (usa masa), mientras que la molaridad sí depende (usa volumen que varía con T).

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La presión de vapor es la presión que ejerce el vapor de un líquido en equilibrio con su fase líquida. Imagínate moléculas escapando de la superficie del líquido y otras regresando - cuando se igualan, tienes equilibrio dinámico.
Esta presión aumenta con la temperatura y es característica de cada sustancia. Cuando la presión de vapor iguala a la presión atmosférica, el líquido hierve. Por eso el agua hierve a 100°C al nivel del mar (1 atm), pero a menor temperatura en las montañas donde la presión es menor.
En La Laguna (550m de altitud), la presión es ~712 mmHg, por lo que el agua hierve a 98°C. Este principio explica por qué es difícil hacer un buen té en las montañas - el agua hierve antes de alcanzar 100°C.
La olla a presión funciona al revés: aumenta la presión interior hasta ~2,3 atm, obligando al agua a hervir a 120-125°C. La cocción es más rápida porque la temperatura es mayor.
La temperatura de ebullición es aquella donde la presión de vapor del líquido iguala la presión externa. Es un concepto relativo - no hay una temperatura fija de ebullición sin especificar la presión.
Conexión real: Por esto los alpinistas usan ollas a presión - compensan la menor presión atmosférica de la altitud para cocinar eficientemente.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las propiedades coligativas son fascinantes porque dependen solo del número de partículas disueltas, no de su naturaleza. Son cuatro: descenso de presión de vapor, aumento del punto de ebullición, descenso del punto de congelación y presión osmótica.
El descenso de la presión de vapor sigue la ley de Raoult: P = Xdisolvente × P₀. Cuando añades soluto no volátil, reduces la fracción molar del disolvente y por tanto su presión de vapor. Menos moléculas de disolvente en la superficie significa menor evaporación.
El aumento de la temperatura de ebullición (ebullioscopía) usa la fórmula: Te = Te₀ + Ke × m. Como la presión de vapor es menor, necesitas más temperatura para igualar la presión atmosférica. Ke es la constante ebulloscópica del disolvente.
El descenso de la temperatura de congelación (crioscopía) sigue: Tc = Tc₀ - Kc × m. La congelación ocurre cuando las presiones de vapor del líquido y sólido se igualan. El soluto retrasa este equilibrio.
Aplicaciones prácticas: Los anticongelantes del coche bajan el punto de congelación del agua (evitan roturas del radiador) y suben el de ebullición (evitan sobrecalentamiento). También puedes determinar masas moleculares midiendo estas propiedades.
Dato útil: En química forense se usa crioscopía para determinar la concentración de alcohol en sangre y otros fluidos biológicos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La ósmosis es el movimiento de disolvente a través de una membrana semipermeable desde la disolución diluida hacia la concentrada, hasta igualar concentraciones. La presión osmótica (Π) es la presión necesaria para detener este flujo.
La fórmula de Van't Hoff es: Π = CRT, equivalente a ΠV = nRT (¡como los gases!). Aquí C es la molaridad, R = 0,082 atm·L/(K·mol) y T en Kelvin.
El osmómetro mide esta presión usando un émbolo que se eleva hasta que la presión de la columna líquida equilibra la presión osmótica. Es como un manómetro especializado.
La ósmosis inversa aplica presión superior a la osmótica para forzar el paso de disolvente hacia la disolución diluida. Así funcionan las plantas desalinizadoras - aplican presión al agua salada para obtener agua pura.
Las disoluciones isotónicas tienen igual presión osmótica que las células. Las bebidas isotónicas mantienen este equilibrio para evitar deshidratación o hinchazón celular. Las hipertónicas (más concentradas) deshidratan células, las hipotónicas (menos concentradas) las hinchan.
En medicina, los sueros intravenosos deben ser isotónicos para no dañar glóbulos rojos - de lo contrario se arrugarían o explotarían.
Curiosidad biológica: Las plantas marchitas recuperan turgencia cuando les das agua porque las células absorben agua por ósmosis hasta equilibrar las concentraciones.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los solutos iónicos complican un poco el panorama porque se disocian en iones. Cuando NaCl se disuelve: NaCl → Na⁺ + Cl⁻, obtienes dos partículas por cada unidad de soluto original.
Para las propiedades coligativas, esto significa que debes multiplicar la concentración por el número de iones producidos. Si 0,1 M de NaCl produce 0,2 M de partículas totales , el efecto coligativo se duplica.
Las fórmulas siguen siendo las mismas, pero incluyes un factor de multiplicación igual al número de iones. Para NaCl es 2, para CaCl₂ es 3 , para Al₂(SO₄)₃ sería 5 .
Este concepto explica por qué la sal es más efectiva que el azúcar para derretir hielo en las carreteras - produce más partículas por mol disuelto. También por qué el suero fisiológico (NaCl al 0,9%) es isotónico aunque parezca una concentración baja.
En la práctica, la disociación no siempre es completa debido a la formación de pares iónicos, especialmente en disoluciones concentradas. Pero para cálculos básicos, asumimos disociación completa.
Aplicación real: Los deportistas pierden electrolitos (iones) al sudar, no solo agua. Las bebidas deportivas reponen estos iones para mantener el equilibrio osmótico celular.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
19
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS