¿Te parece complicado entender cómo están organizados los elementos químicos... Mostrar más
El átomo y el sistema periódico: Propiedades y enlaces



El átomo y la tabla periódica
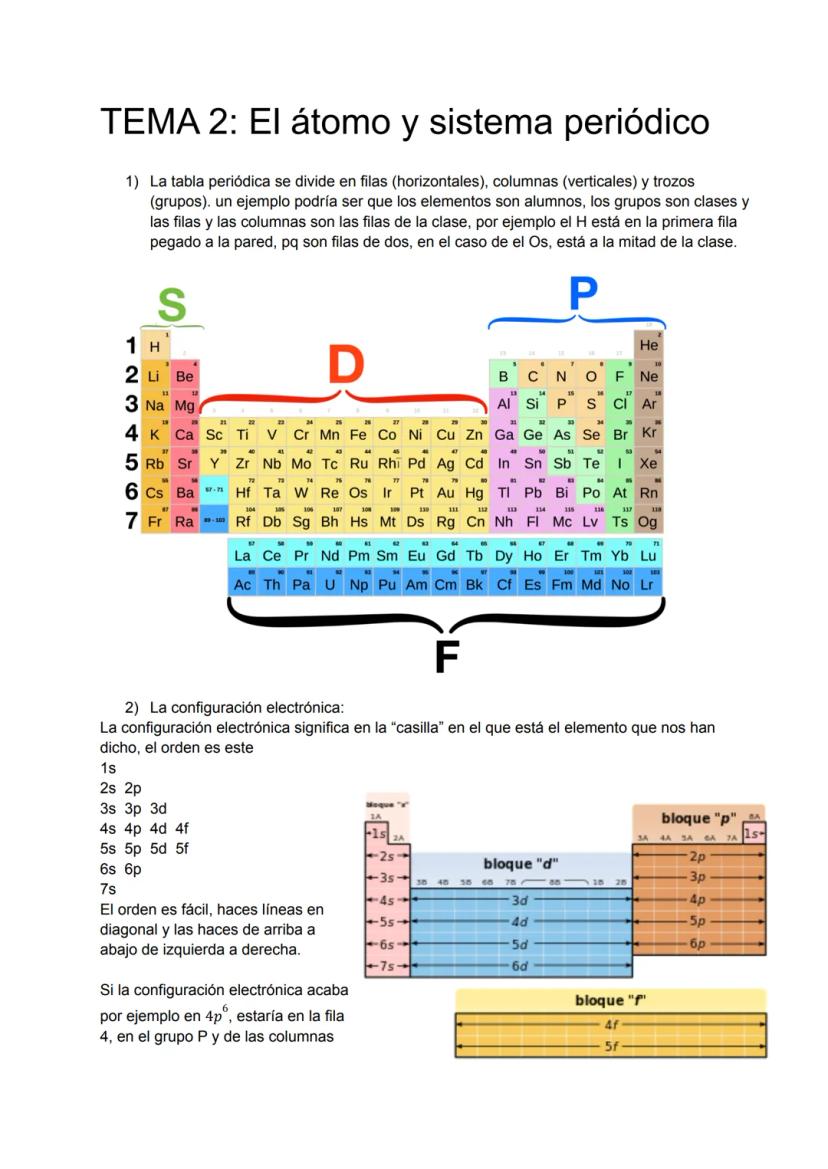
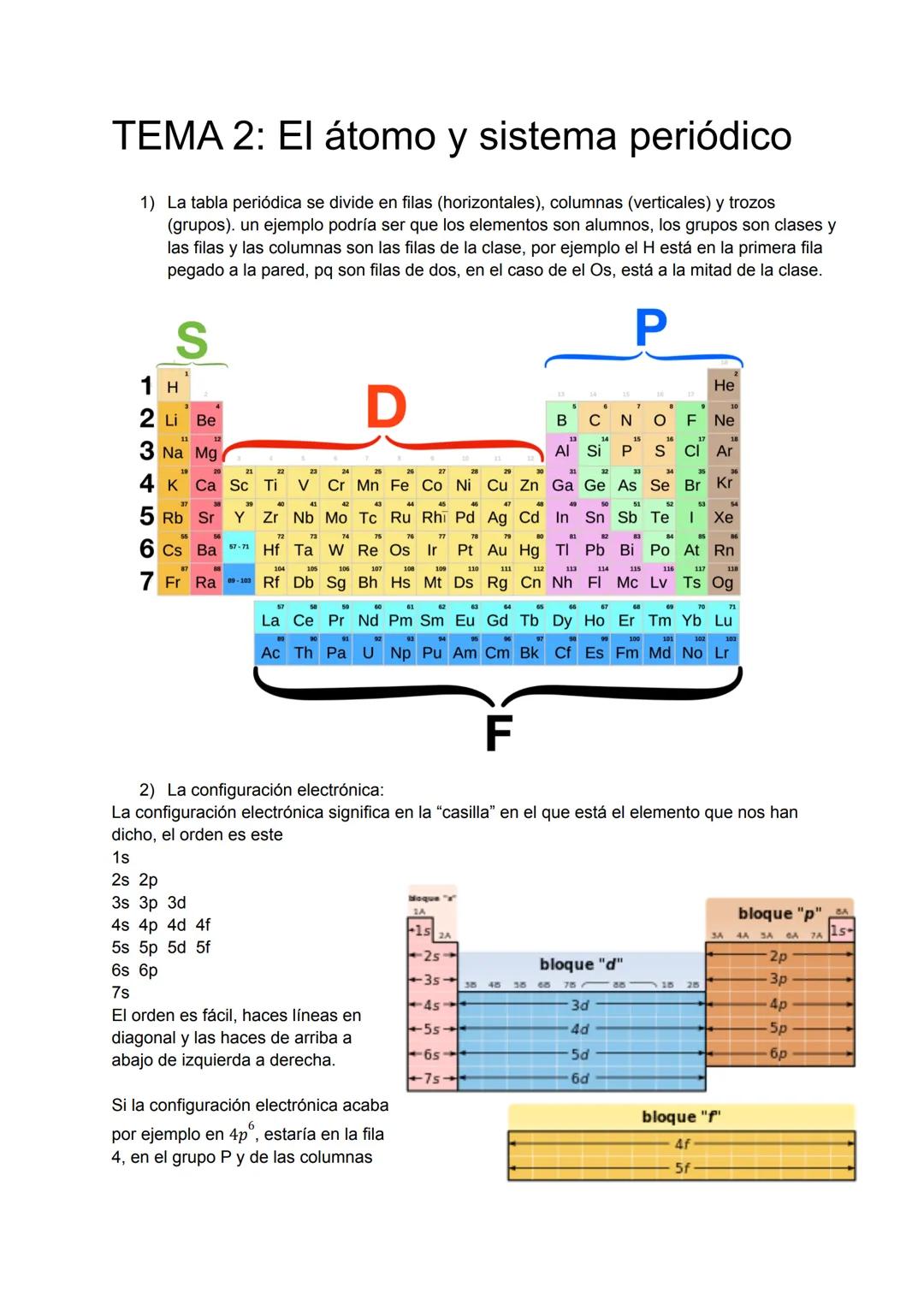
Imagínate que la tabla periódica es como una clase llena de estudiantes. Las filas horizontales son como las filas de pupitres, y las columnas verticales agrupan a estudiantes con características similares. Por ejemplo, el hidrógeno (H) está en la primera fila "pegado a la pared", mientras que elementos como el osmio (Os) están en el medio de la clase.
La configuración electrónica te dice exactamente dónde vive cada elemento en esta "clase". Es como la dirección exacta de cada átomo. Los electrones se organizan en niveles de energía que siguen un orden específico: 1s, 2s, 2p, 3s, 3p, 4s, 3d, y así sucesivamente.
Para encontrar la configuración, simplemente trazas líneas diagonales de arriba hacia abajo y de izquierda a derecha. Si un elemento termina en 4p⁶, sabrás que está en la fila 4, grupo p, columna 6. ¡Es como seguir un mapa del tesoro!
Truco clave: La configuración electrónica es como el DNI de cada elemento - te dice exactamente dónde encontrarlo en la tabla periódica.

Propiedades atómicas y modelos históricos
Todos los átomos tienen cinco propiedades principales que determinan cómo se comportan: el radio atómico (su tamaño), el carácter metálico (facilidad para perder electrones), el potencial de ionización (energía para quitar electrones), la afinidad electrónica (capacidad de ganar electrones) y la electronegatividad (fuerza para atraer electrones).
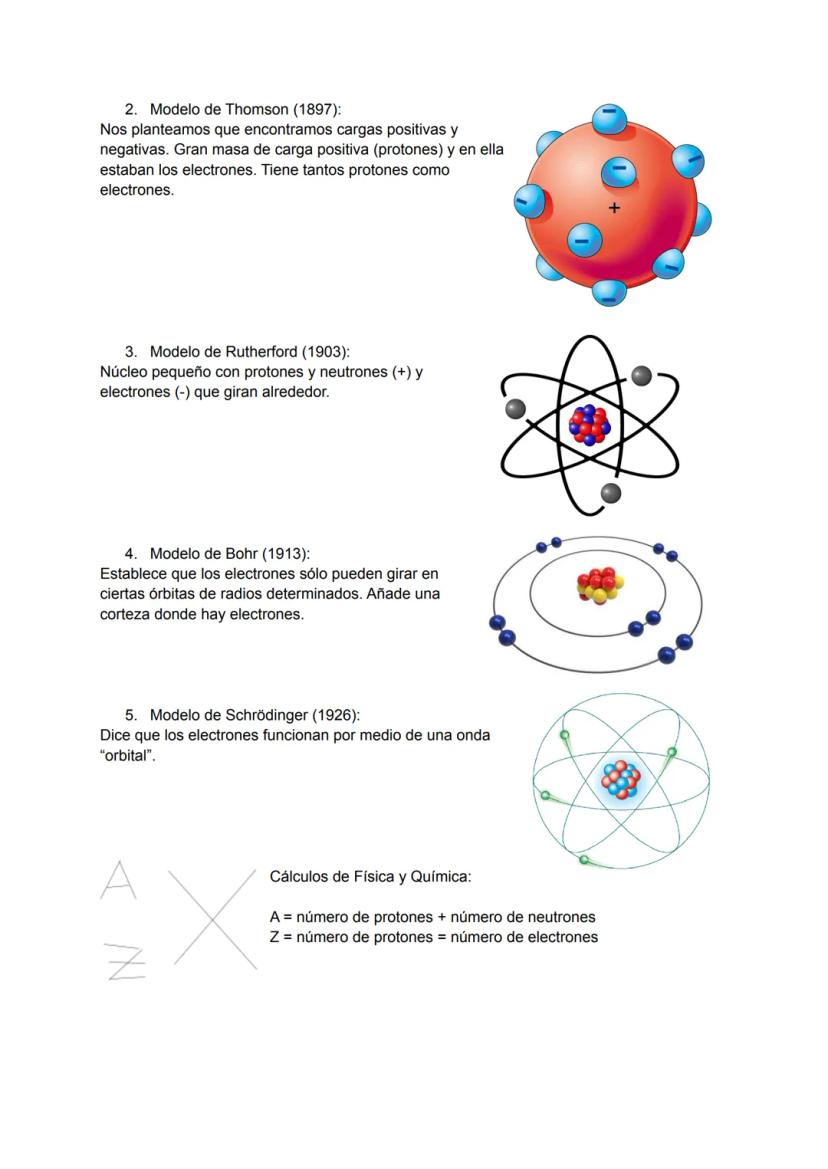
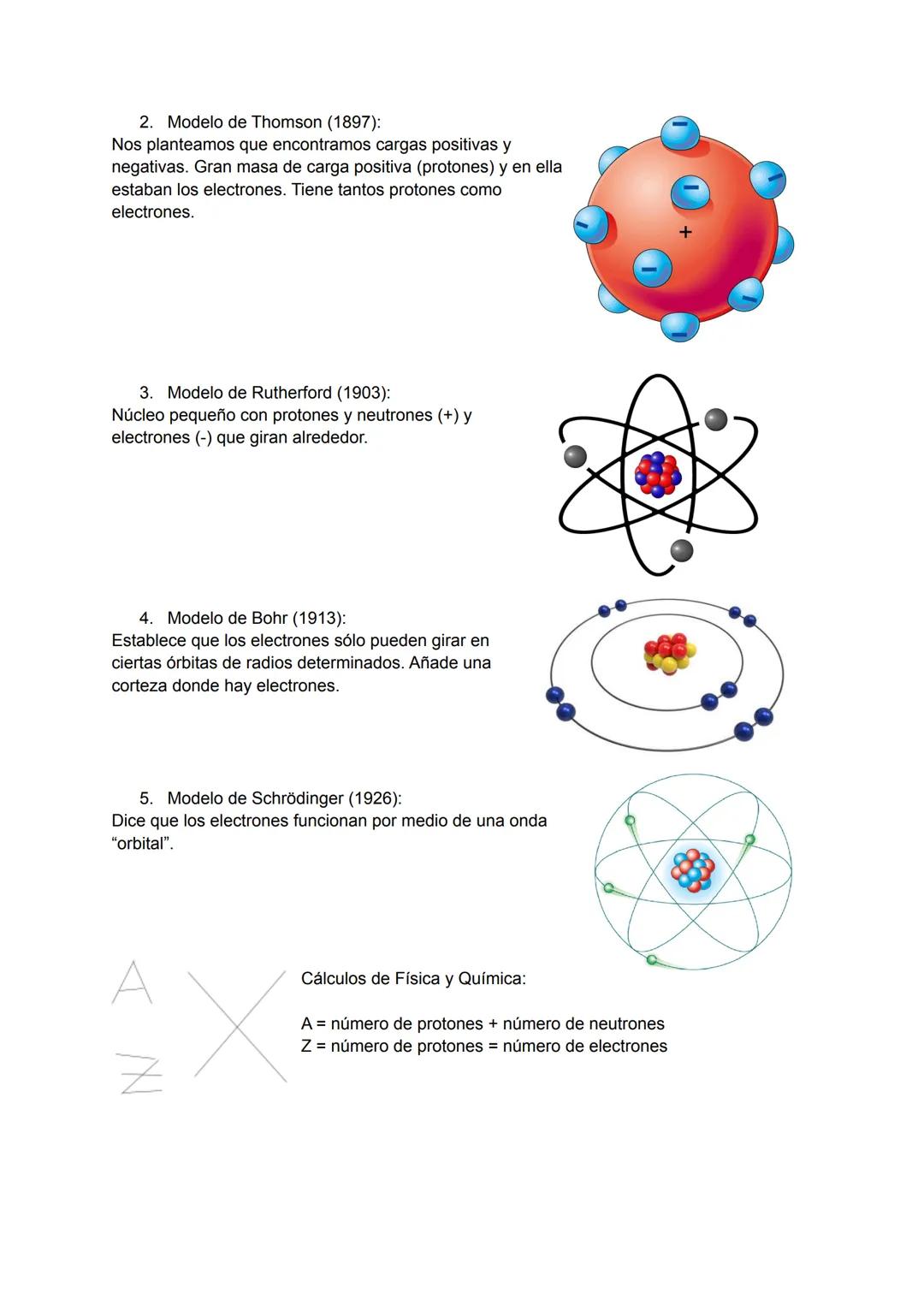
Los científicos tardaron siglos en entender la estructura atómica. Dalton pensaba que eran indivisibles, Thomson los describió como un "pudin de pasas", Rutherford descubrió el núcleo, Bohr añadió las órbitas fijas, y finalmente Schrödinger introdujo el concepto de orbitales como ondas.
Para hacer cálculos básicos, recuerda estas fórmulas sencillas: A = número de protones + neutrones, y Z = número de protones = número de electrones (en átomos neutros). Son las herramientas básicas que necesitarás para resolver problemas.
Dato curioso: Cada modelo atómico fue como una pieza de un puzzle - todos contribuyeron a formar la imagen completa que tenemos hoy.
Enlaces químicos
Los átomos se unen de tres maneras principales para formar compuestos. El enlace iónico ocurre entre metales y no metales, donde uno cede electrones y el otro los acepta. Es como un intercambio: el sodio (Na) le da un electrón al cloro (Cl) para formar sal.
El enlace covalente se da entre no metales que comparten electrones para completar sus capas externas. El agua (H₂O) es un ejemplo perfecto: el oxígeno comparte electrones con dos átomos de hidrógeno.
El enlace metálico permite que los metales compartan electrones libremente, como un "mar de electrones". Por eso los metales brillan, conducen electricidad y se pueden moldear fácilmente.
Cada tipo de enlace le da propiedades específicas a los compuestos. Los iónicos son duros pero frágiles, los covalentes pueden ser gases o líquidos, y los metálicos son maleables y conductores.
Para recordar: Iónico = intercambio, Covalente = compartir entre no metales, Metálico = mar de electrones.

Formulación y concentraciones
La formulación inorgánica te permite escribir correctamente las fórmulas químicas. Los compuestos ternarios incluyen hidróxidos (OH⁻) que son básicos, ácidos oxoácidos que tienen pH ácido, y sales que se forman cuando se neutralizan.
Para calcular concentraciones, usas la fórmula mol/L. Es fundamental entender que la solubilidad (cuánto soluto se puede disolver) aumenta con la temperatura - por eso el azúcar se disuelve mejor en café caliente que frío.
La clave está en practicar estos cálculos paso a paso. Una vez que domines las fórmulas básicas, podrás resolver cualquier problema de concentración que te pongan en el examen.
Consejo de estudio: Practica con los ejercicios T5 26-41 - son 10 ejercicios que cubren todos estos conceptos de forma progresiva.

Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: partículas atómicas
9El átomo
El átomo
Tabla Periódica Frases
Frases de algunas columnas para ayudar a memorizar la tabla periódica
Propiedades periódicas
Apuntes propiedades periódicas 1bach, las actividades son de emestrada.
Enlaces químicos, uniones intermoleculares, reacciones químicas e industria química.
Apunets sobre los enlaces químicos y sus tipos, las uniones intermoleculares, reacciones químicas con sus procesos y factores e información y estaciones en la industria química.
Identificación de Átomos: Número Atómico
El número atómico y el número másico son clave para diferenciar átomos de distintos elementos. Ejemplo con el sodio.
Tabla periódica (solo los símbolos químicos y sus nombres 🕺🏼🕺🏼🕺🏼
Faltan algún ya que esos son los que pidió mi profesor espero ayudar 😰😰😰
El enlace químico
Profundizamos en el enlace químico
La jerga química: formulación inorgánica
LA JERGA QUÍMICA: FORMULACIÓN INORGÁNICA
Peroxidos
Formulación
Contenidos más populares de Física i Química
9Formulario Dinámica y Cinemática
Aquí un esquema de todas las formulas, válido sobre todo para bachillerato y 4ESO. También incluyo un ejercicio de dinámica resuelto bastante completo
Resumen Dinamica fisica 1 bach
Resumen Dinamica fisica 1 bachillerato
Tabla periódica
Aprende sobre la tabla periódica.
DINÁMICA
teoría + ejercicios resueltos
Cinemática y dinámica
- Magnitudes del movimiento, MRU, MRUA, Caída libre/tiro vertical
Mcu y mcua
Movimiento circular uniforme y movimiento circular uniforme acelerado
fuerzas
apuntes sobre fuerzas
Fuerzas
física y química
MRU Y MRUA
movimiento rectilíneo uniforme y movimiento rectilíneo uniformemente acelerado
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
El átomo y el sistema periódico: Propiedades y enlaces
¿Te parece complicado entender cómo están organizados los elementos químicos y por qué se comportan de manera diferente? En realidad, todo tiene que ver con la estructura del átomo y cómo los electrones se organizan alrededor del núcleo. Una vez... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El átomo y la tabla periódica
Imagínate que la tabla periódica es como una clase llena de estudiantes. Las filas horizontales son como las filas de pupitres, y las columnas verticales agrupan a estudiantes con características similares. Por ejemplo, el hidrógeno (H) está en la primera fila "pegado a la pared", mientras que elementos como el osmio (Os) están en el medio de la clase.
La configuración electrónica te dice exactamente dónde vive cada elemento en esta "clase". Es como la dirección exacta de cada átomo. Los electrones se organizan en niveles de energía que siguen un orden específico: 1s, 2s, 2p, 3s, 3p, 4s, 3d, y así sucesivamente.
Para encontrar la configuración, simplemente trazas líneas diagonales de arriba hacia abajo y de izquierda a derecha. Si un elemento termina en 4p⁶, sabrás que está en la fila 4, grupo p, columna 6. ¡Es como seguir un mapa del tesoro!
Truco clave: La configuración electrónica es como el DNI de cada elemento - te dice exactamente dónde encontrarlo en la tabla periódica.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades atómicas y modelos históricos
Todos los átomos tienen cinco propiedades principales que determinan cómo se comportan: el radio atómico (su tamaño), el carácter metálico (facilidad para perder electrones), el potencial de ionización (energía para quitar electrones), la afinidad electrónica (capacidad de ganar electrones) y la electronegatividad (fuerza para atraer electrones).
Los científicos tardaron siglos en entender la estructura atómica. Dalton pensaba que eran indivisibles, Thomson los describió como un "pudin de pasas", Rutherford descubrió el núcleo, Bohr añadió las órbitas fijas, y finalmente Schrödinger introdujo el concepto de orbitales como ondas.
Para hacer cálculos básicos, recuerda estas fórmulas sencillas: A = número de protones + neutrones, y Z = número de protones = número de electrones (en átomos neutros). Son las herramientas básicas que necesitarás para resolver problemas.
Dato curioso: Cada modelo atómico fue como una pieza de un puzzle - todos contribuyeron a formar la imagen completa que tenemos hoy.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces químicos
Los átomos se unen de tres maneras principales para formar compuestos. El enlace iónico ocurre entre metales y no metales, donde uno cede electrones y el otro los acepta. Es como un intercambio: el sodio (Na) le da un electrón al cloro (Cl) para formar sal.
El enlace covalente se da entre no metales que comparten electrones para completar sus capas externas. El agua (H₂O) es un ejemplo perfecto: el oxígeno comparte electrones con dos átomos de hidrógeno.
El enlace metálico permite que los metales compartan electrones libremente, como un "mar de electrones". Por eso los metales brillan, conducen electricidad y se pueden moldear fácilmente.
Cada tipo de enlace le da propiedades específicas a los compuestos. Los iónicos son duros pero frágiles, los covalentes pueden ser gases o líquidos, y los metálicos son maleables y conductores.
Para recordar: Iónico = intercambio, Covalente = compartir entre no metales, Metálico = mar de electrones.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Formulación y concentraciones
La formulación inorgánica te permite escribir correctamente las fórmulas químicas. Los compuestos ternarios incluyen hidróxidos (OH⁻) que son básicos, ácidos oxoácidos que tienen pH ácido, y sales que se forman cuando se neutralizan.
Para calcular concentraciones, usas la fórmula mol/L. Es fundamental entender que la solubilidad (cuánto soluto se puede disolver) aumenta con la temperatura - por eso el azúcar se disuelve mejor en café caliente que frío.
La clave está en practicar estos cálculos paso a paso. Una vez que domines las fórmulas básicas, podrás resolver cualquier problema de concentración que te pongan en el examen.
Consejo de estudio: Practica con los ejercicios T5 26-41 - son 10 ejercicios que cubren todos estos conceptos de forma progresiva.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenidos más populares: partículas atómicas
9El átomo
El átomo
Tabla Periódica Frases
Frases de algunas columnas para ayudar a memorizar la tabla periódica
Propiedades periódicas
Apuntes propiedades periódicas 1bach, las actividades son de emestrada.
Enlaces químicos, uniones intermoleculares, reacciones químicas e industria química.
Apunets sobre los enlaces químicos y sus tipos, las uniones intermoleculares, reacciones químicas con sus procesos y factores e información y estaciones en la industria química.
Identificación de Átomos: Número Atómico
El número atómico y el número másico son clave para diferenciar átomos de distintos elementos. Ejemplo con el sodio.
Tabla periódica (solo los símbolos químicos y sus nombres 🕺🏼🕺🏼🕺🏼
Faltan algún ya que esos son los que pidió mi profesor espero ayudar 😰😰😰
El enlace químico
Profundizamos en el enlace químico
La jerga química: formulación inorgánica
LA JERGA QUÍMICA: FORMULACIÓN INORGÁNICA
Peroxidos
Formulación
Contenidos más populares de Física i Química
9Formulario Dinámica y Cinemática
Aquí un esquema de todas las formulas, válido sobre todo para bachillerato y 4ESO. También incluyo un ejercicio de dinámica resuelto bastante completo
Resumen Dinamica fisica 1 bach
Resumen Dinamica fisica 1 bachillerato
Tabla periódica
Aprende sobre la tabla periódica.
DINÁMICA
teoría + ejercicios resueltos
Cinemática y dinámica
- Magnitudes del movimiento, MRU, MRUA, Caída libre/tiro vertical
Mcu y mcua
Movimiento circular uniforme y movimiento circular uniforme acelerado
fuerzas
apuntes sobre fuerzas
Fuerzas
física y química
MRU Y MRUA
movimiento rectilíneo uniforme y movimiento rectilíneo uniformemente acelerado
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.