¿Sabías que solo seis elementos químicos forman el 99% de... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
265
•
Actualizado May 11, 2026
•
Claudia Fernández
@_claudiafdez
¿Sabías que solo seis elementos químicos forman el 99% de... Mostrar más










Solo seis elementos (C, H, O, N, P, S) forman el 99% de todos los seres vivos. ¿La razón? Estos elementos pueden unirse entre sí formando moléculas complejas que son la base de la vida.
Los seres vivos funcionan gracias a dos tipos de enlaces: los enlaces fuertes (covalentes e iónicos) que forman las moléculas, y los enlaces débiles (puentes de hidrógeno y fuerzas de Van der Waals) que permiten que estas moléculas funcionen correctamente.
El enlace covalente se forma cuando átomos no metálicos comparten electrones siguiendo la regla del octeto - todos los átomos quieren tener 8 electrones en su última capa. Cuando los átomos que se unen son iguales, el enlace es apolar; si son diferentes, es polar porque uno atrae más los electrones.
💡 Recuerda: Los enlaces débiles son tan importantes como los fuertes - sin ellos, las proteínas no tendrían su forma correcta y las enzimas no funcionarían.

El enlace iónico se forma entre un metal y un no metal. El metal cede electrones y el no metal los acepta . Como cargas opuestas se atraen, se forma el enlace.
Las fuerzas intermoleculares son atracciones entre moléculas que no cambian su composición química. Las más importantes son las fuerzas de Van der Waals y los enlaces de hidrógeno.
Las fuerzas de Van der Waals incluyen las fuerzas dipolo-dipolo (entre moléculas polares) y las fuerzas de London (entre moléculas no polares que temporalmente se vuelven polares). Sin estas fuerzas, todas las sustancias serían gases.
Los enlaces de hidrógeno se forman cuando el hidrógeno se une a átomos muy electronegativos como F, O o N. Son enlaces dipolo-dipolo especialmente fuertes y son fundamentales para las propiedades del agua.
💡 Dato curioso: Sin las fuerzas de Van der Waals, el agua sería gas a temperatura ambiente y la vida tal como la conocemos sería imposible.

Los bioelementos son los 70 elementos que forman la materia viva, pero no todos son igual de importantes. Se clasifican según su abundancia y función.
Los bioelementos primarios (C, H, O, N, P, S) forman el 99% de las células. Son perfectos para la vida porque necesitan pocos electrones para completar su última capa, tienen masa atómica baja y forman enlaces covalentes estables.
Los bioelementos secundarios (Na⁺, K⁺, Cl⁻, Ca²⁺, Mg²⁺) aparecen en pequeñas cantidades pero son esenciales. El Na⁺ y K⁺ transmiten impulsos nerviosos, el Ca²⁺ participa en la contracción muscular y el Mg²⁺ está en la clorofila.
Los oligoelementos (Fe, Mn, I, F, Cu, Zn) están presentes en menos del 0,1% pero su deficiencia causa enfermedades. El hierro transporta oxígeno en la hemoglobina y el yodo es necesario para las hormonas tiroideas.
💡 Importante: La falta de oligoelementos puede causar enfermedades graves, pero su exceso también es tóxico. ¡El equilibrio es clave!

El carbono es especial porque tiene cuatro valencias que le permiten unirse a otros carbonos formando cadenas, ramificaciones y anillos. Sus enlaces pueden ser simples , dobles o triples, creando infinitas posibilidades.
Los grupos funcionales dan propiedades específicas a las moléculas orgánicas. Los grupos hidrófilos son polares y se disuelven en agua. Los hidrófobos (radicales alquílicos) son apolares y repelen el agua.
La configuración tetraédrica del carbono permite formar moléculas tridimensionales cuya forma es exactamente la necesaria para su función. Es como una llave que encaja perfectamente en su cerradura.
Las macromoléculas de carbono pueden contener información genética, replicarse y transmitir esa información a los descendientes. Por eso el carbono es la base de la química orgánica, aunque no todos los compuestos de carbono son orgánicos (como el CO₂).
💡 Analogía útil: Piensa en el carbono como las piezas de Lego más versátiles - pueden conectarse de múltiples formas para crear estructuras complejas y funcionales.

El agua representa entre el 65-95% del peso de los seres vivos y es donde surgió la vida. Se encuentra como agua circulante (sangre, savia), intersticial (entre células) e intracelular (dentro de las células).
La molécula de agua tiene forma angular con un ángulo de 104,5°. Aunque es eléctricamente neutra, es polar porque los electrones del hidrógeno se desplazan hacia el oxígeno, creando cargas parciales.
Esta polaridad permite formar puentes de hidrógeno entre moléculas de agua. La carga parcial negativa del oxígeno atrae las cargas parciales positivas de los hidrógenos de otras moléculas, formando grupos de 3-9 moléculas.
Estos puentes duran fracciones de segundo, dando al agua su fluidez característica. En realidad, el agua líquida es como pequeños polímeros con huecos ocupados por moléculas aisladas.
💡 Visualízalo: Imagina las moléculas de agua como imanes débiles que se atraen y repelen constantemente, creando una estructura dinámica pero cohesiva.

El agua tiene propiedades extraordinarias que la hacen única. Su elevada fuerza de cohesión la convierte en un líquido casi incompresible que puede funcionar como esqueleto hidrostático en algunos gusanos.
Su elevada fuerza de adhesión permite que ascienda por tubos capilares, explicando cómo las plantas transportan la savia desde las raíces hasta las hojas a través de los vasos leñosos.
El gran calor específico significa que necesita mucha energía para elevar su temperatura porque primero debe romper los puentes de hidrógeno. Esto la convierte en un excelente estabilizador térmico del organismo.
El elevado calor de vaporización explica por qué sudar es tan efectivo para refrescarse - se necesita mucha energía para evaporar el agua. La mayor densidad en estado líquido hace que el hielo flote, creando una capa aislante que permite la vida acuática en invierno.
💡 Aplicación práctica: Cuando tienes fiebre, tu cuerpo usa las propiedades del agua (sudoración y alta capacidad calorífica) para regular la temperatura.
La elevada constante dieléctrica convierte al agua en el disolvente universal. Las moléculas polares del agua rodean los solutos, separando los compuestos iónicos en aniones y cationes mediante solvatación iónica.
El bajo grado de ionización del agua pura significa que solo 1 de cada 551 millones de moléculas se encuentra ionizada, manteniendo concentraciones muy bajas de H₃O⁺ y OH⁻.
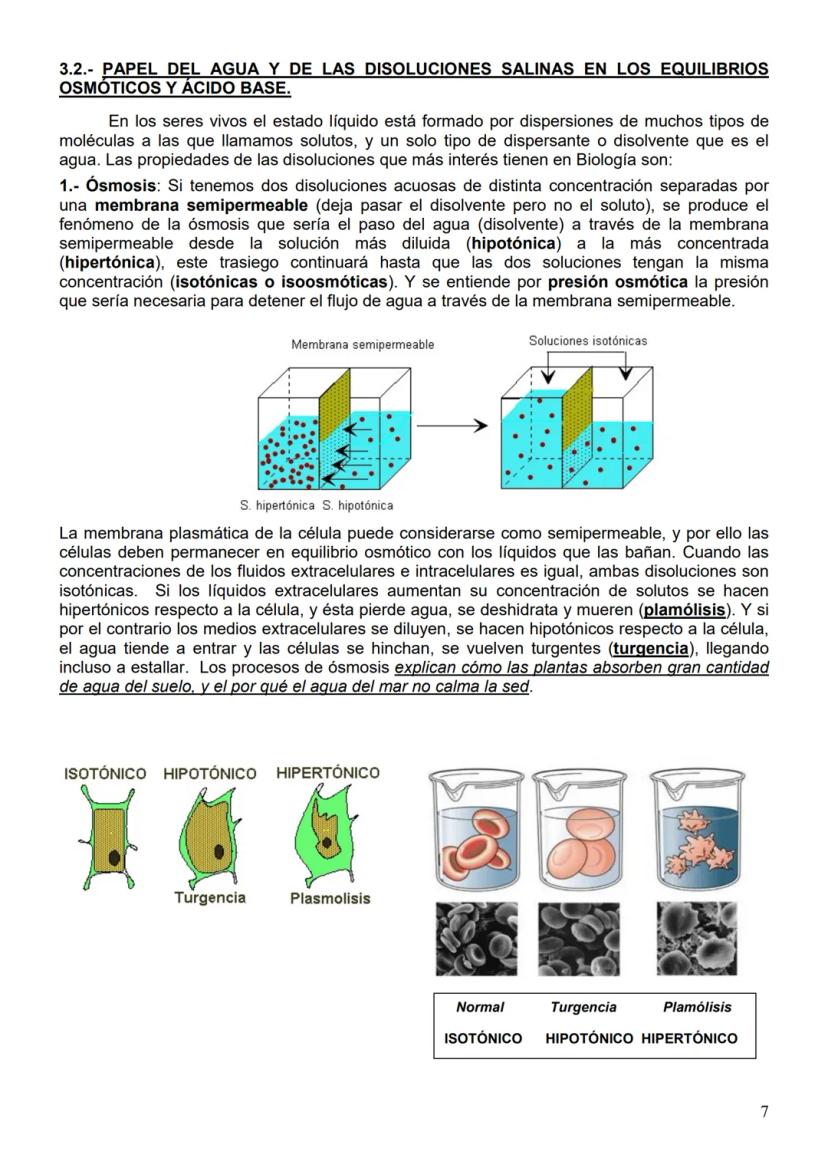
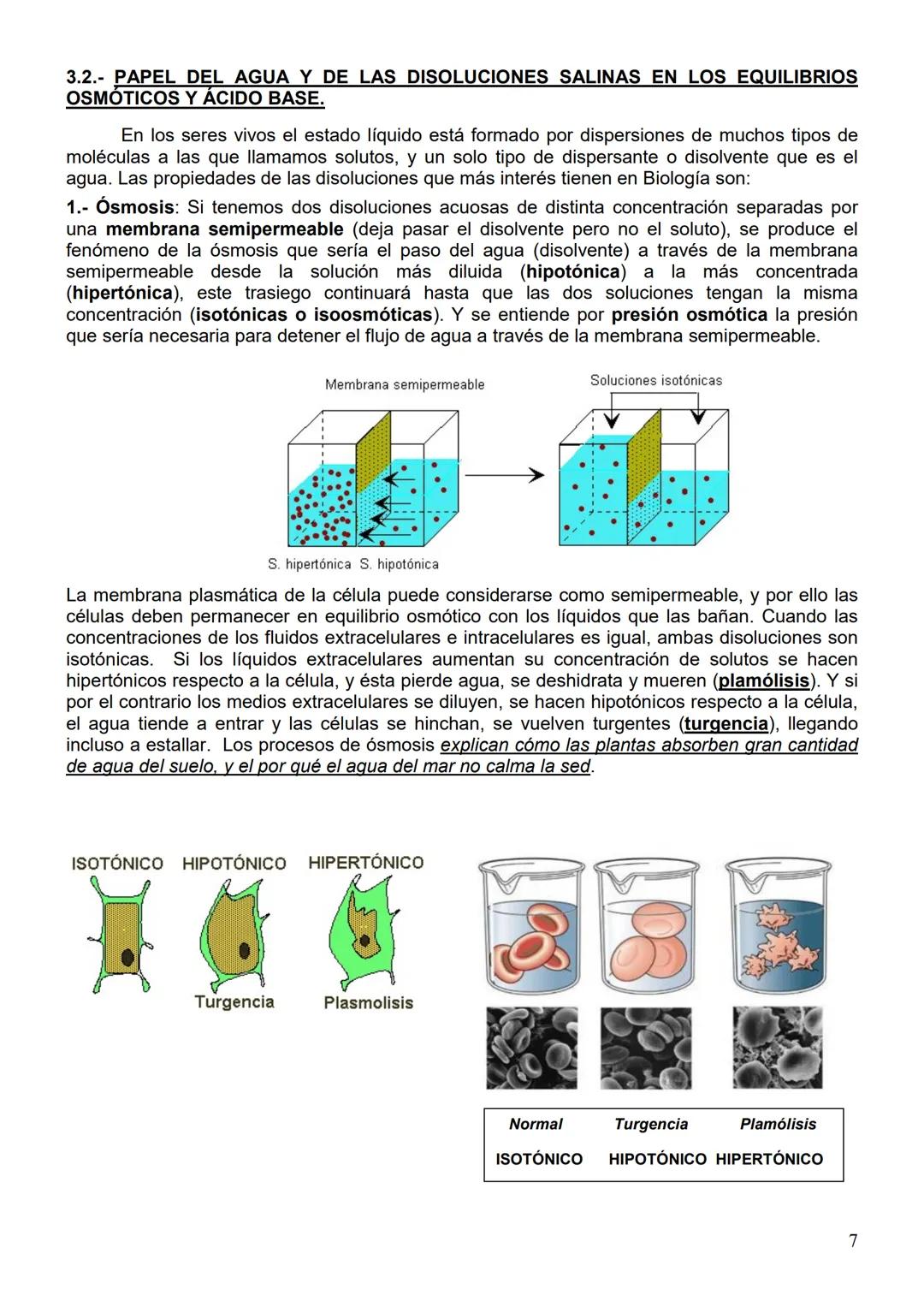
La ósmosis es el paso de agua a través de membranas semipermeables desde disoluciones hipotónicas (menos concentradas) hacia hipertónicas (más concentradas) hasta alcanzar equilibrio isotónico.
Cuando las células están en medio hipotónico se hinchan (turgencia), cuando están en medio hipertónico se deshidratan (plasmólisis). Este proceso explica por qué el agua del mar no calma la sed y cómo las plantas absorben agua del suelo.
💡 Ejemplo cotidiano: Las células de lechuga se arrugan con sal (plasmólisis) pero se recuperan en agua dulce (turgencia). ¡Tu cuerpo hace esto constantemente para mantener el equilibrio!

El pH mide la acidez de una disolución en escala de 0 a 14. pH = 7 es neutro, < 7 es ácido y > 7 es básico. Los seres vivos mantienen el pH constante porque las enzimas solo funcionan en rangos específicos.
Las disoluciones tampón (principalmente sales minerales) mantienen el pH estable. Si aumenta la acidez, el tampón absorbe los H⁺ excesivos; si disminuye, libera H⁺ para compensar.
El sistema tampón fosfato mantiene el pH celular en 7,2 mediante la reacción reversible entre dihidrógeno fosfato e hidrógeno fosfato. Las grandes cantidades de fosfato en células y huesos lo hacen muy eficaz.
El sistema tampón bicarbonato regula el pH sanguíneo. Cuando aumenta la acidez, se forma CO₂ que se elimina por los pulmones. Cuando disminuye, se toma CO₂ del exterior y el bicarbonato se elimina por los riñones.
💡 Dato médico: Los trastornos del pH sanguíneo (acidosis o alcalosis) pueden ser mortales. Tu cuerpo trabaja constantemente para mantenerlo entre 7,35-7,45.

El agua realiza funciones vitales gracias a sus propiedades únicas. Como disolvente, facilita todas las reacciones químicas del metabolismo mediante solvatación iónica.
Como reactivo, participa directamente en reacciones como la hidrólisis que descompone moléculas complejas. Como transportadora, mueve nutrientes y desechos tanto dentro como fuera de los organismos.
Su función estructural mantiene la forma celular mediante presión osmótica, especialmente en células sin pared rígida. Como amortiguador mecánico, protege articulaciones y órganos del rozamiento y impactos.
La función termorreguladora es crucial para mantener la temperatura corporal estable gracias a su alto calor específico y de vaporización.
💡 Reflexión: Cada vez que bebes agua, no solo te hidratas - estás proporcionando a tu cuerpo el disolvente, reactivo, transportador y termorregulador más eficaz que existe.

Las sales minerales son compuestos inorgánicos que desempeñan funciones diferentes según su solubilidad en agua. No las produces, pero son esenciales para vivir.
Las sales insolubles precipitan formando estructuras sólidas de protección y sostén. Los caparazones de moluscos (carbonato cálcico), huesos de vertebrados (fosfatos y carbonatos de calcio) y otolitos del oído (equilibrio) son ejemplos clave.
Las sales solubles se disocian en cationes (Na⁺, K⁺, Mg²⁺, Fe²⁺) y aniones (Cl⁻, PO₄³⁻, CO₃²⁻) que realizan funciones reguladoras como control del pH y activación enzimática.
También tienen funciones específicas fundamentales: Na⁺ y K⁺ transmiten impulsos nerviosos, Ca²⁺ contrae músculos, Mg²⁺ activa enzimas y los fosfatos almacenan energía en forma de ATP.
💡 Consejo de salud: Una dieta equilibrada te aporta todas las sales minerales necesarias. Los suplementos solo son necesarios en casos específicos diagnosticados por profesionales.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
Claudia Fernández
@_claudiafdez
¿Sabías que solo seis elementos químicos forman el 99% de todo lo que está vivo? En este tema verás por qué el carbono, hidrógeno, oxígeno, nitrógeno, fósforo y azufre son tan especiales y cómo se combinan para crear la vida.... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Solo seis elementos (C, H, O, N, P, S) forman el 99% de todos los seres vivos. ¿La razón? Estos elementos pueden unirse entre sí formando moléculas complejas que son la base de la vida.
Los seres vivos funcionan gracias a dos tipos de enlaces: los enlaces fuertes (covalentes e iónicos) que forman las moléculas, y los enlaces débiles (puentes de hidrógeno y fuerzas de Van der Waals) que permiten que estas moléculas funcionen correctamente.
El enlace covalente se forma cuando átomos no metálicos comparten electrones siguiendo la regla del octeto - todos los átomos quieren tener 8 electrones en su última capa. Cuando los átomos que se unen son iguales, el enlace es apolar; si son diferentes, es polar porque uno atrae más los electrones.
💡 Recuerda: Los enlaces débiles son tan importantes como los fuertes - sin ellos, las proteínas no tendrían su forma correcta y las enzimas no funcionarían.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El enlace iónico se forma entre un metal y un no metal. El metal cede electrones y el no metal los acepta . Como cargas opuestas se atraen, se forma el enlace.
Las fuerzas intermoleculares son atracciones entre moléculas que no cambian su composición química. Las más importantes son las fuerzas de Van der Waals y los enlaces de hidrógeno.
Las fuerzas de Van der Waals incluyen las fuerzas dipolo-dipolo (entre moléculas polares) y las fuerzas de London (entre moléculas no polares que temporalmente se vuelven polares). Sin estas fuerzas, todas las sustancias serían gases.
Los enlaces de hidrógeno se forman cuando el hidrógeno se une a átomos muy electronegativos como F, O o N. Son enlaces dipolo-dipolo especialmente fuertes y son fundamentales para las propiedades del agua.
💡 Dato curioso: Sin las fuerzas de Van der Waals, el agua sería gas a temperatura ambiente y la vida tal como la conocemos sería imposible.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los bioelementos son los 70 elementos que forman la materia viva, pero no todos son igual de importantes. Se clasifican según su abundancia y función.
Los bioelementos primarios (C, H, O, N, P, S) forman el 99% de las células. Son perfectos para la vida porque necesitan pocos electrones para completar su última capa, tienen masa atómica baja y forman enlaces covalentes estables.
Los bioelementos secundarios (Na⁺, K⁺, Cl⁻, Ca²⁺, Mg²⁺) aparecen en pequeñas cantidades pero son esenciales. El Na⁺ y K⁺ transmiten impulsos nerviosos, el Ca²⁺ participa en la contracción muscular y el Mg²⁺ está en la clorofila.
Los oligoelementos (Fe, Mn, I, F, Cu, Zn) están presentes en menos del 0,1% pero su deficiencia causa enfermedades. El hierro transporta oxígeno en la hemoglobina y el yodo es necesario para las hormonas tiroideas.
💡 Importante: La falta de oligoelementos puede causar enfermedades graves, pero su exceso también es tóxico. ¡El equilibrio es clave!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El carbono es especial porque tiene cuatro valencias que le permiten unirse a otros carbonos formando cadenas, ramificaciones y anillos. Sus enlaces pueden ser simples , dobles o triples, creando infinitas posibilidades.
Los grupos funcionales dan propiedades específicas a las moléculas orgánicas. Los grupos hidrófilos son polares y se disuelven en agua. Los hidrófobos (radicales alquílicos) son apolares y repelen el agua.
La configuración tetraédrica del carbono permite formar moléculas tridimensionales cuya forma es exactamente la necesaria para su función. Es como una llave que encaja perfectamente en su cerradura.
Las macromoléculas de carbono pueden contener información genética, replicarse y transmitir esa información a los descendientes. Por eso el carbono es la base de la química orgánica, aunque no todos los compuestos de carbono son orgánicos (como el CO₂).
💡 Analogía útil: Piensa en el carbono como las piezas de Lego más versátiles - pueden conectarse de múltiples formas para crear estructuras complejas y funcionales.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El agua representa entre el 65-95% del peso de los seres vivos y es donde surgió la vida. Se encuentra como agua circulante (sangre, savia), intersticial (entre células) e intracelular (dentro de las células).
La molécula de agua tiene forma angular con un ángulo de 104,5°. Aunque es eléctricamente neutra, es polar porque los electrones del hidrógeno se desplazan hacia el oxígeno, creando cargas parciales.
Esta polaridad permite formar puentes de hidrógeno entre moléculas de agua. La carga parcial negativa del oxígeno atrae las cargas parciales positivas de los hidrógenos de otras moléculas, formando grupos de 3-9 moléculas.
Estos puentes duran fracciones de segundo, dando al agua su fluidez característica. En realidad, el agua líquida es como pequeños polímeros con huecos ocupados por moléculas aisladas.
💡 Visualízalo: Imagina las moléculas de agua como imanes débiles que se atraen y repelen constantemente, creando una estructura dinámica pero cohesiva.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El agua tiene propiedades extraordinarias que la hacen única. Su elevada fuerza de cohesión la convierte en un líquido casi incompresible que puede funcionar como esqueleto hidrostático en algunos gusanos.
Su elevada fuerza de adhesión permite que ascienda por tubos capilares, explicando cómo las plantas transportan la savia desde las raíces hasta las hojas a través de los vasos leñosos.
El gran calor específico significa que necesita mucha energía para elevar su temperatura porque primero debe romper los puentes de hidrógeno. Esto la convierte en un excelente estabilizador térmico del organismo.
El elevado calor de vaporización explica por qué sudar es tan efectivo para refrescarse - se necesita mucha energía para evaporar el agua. La mayor densidad en estado líquido hace que el hielo flote, creando una capa aislante que permite la vida acuática en invierno.
💡 Aplicación práctica: Cuando tienes fiebre, tu cuerpo usa las propiedades del agua (sudoración y alta capacidad calorífica) para regular la temperatura.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La elevada constante dieléctrica convierte al agua en el disolvente universal. Las moléculas polares del agua rodean los solutos, separando los compuestos iónicos en aniones y cationes mediante solvatación iónica.
El bajo grado de ionización del agua pura significa que solo 1 de cada 551 millones de moléculas se encuentra ionizada, manteniendo concentraciones muy bajas de H₃O⁺ y OH⁻.
La ósmosis es el paso de agua a través de membranas semipermeables desde disoluciones hipotónicas (menos concentradas) hacia hipertónicas (más concentradas) hasta alcanzar equilibrio isotónico.
Cuando las células están en medio hipotónico se hinchan (turgencia), cuando están en medio hipertónico se deshidratan (plasmólisis). Este proceso explica por qué el agua del mar no calma la sed y cómo las plantas absorben agua del suelo.
💡 Ejemplo cotidiano: Las células de lechuga se arrugan con sal (plasmólisis) pero se recuperan en agua dulce (turgencia). ¡Tu cuerpo hace esto constantemente para mantener el equilibrio!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El pH mide la acidez de una disolución en escala de 0 a 14. pH = 7 es neutro, < 7 es ácido y > 7 es básico. Los seres vivos mantienen el pH constante porque las enzimas solo funcionan en rangos específicos.
Las disoluciones tampón (principalmente sales minerales) mantienen el pH estable. Si aumenta la acidez, el tampón absorbe los H⁺ excesivos; si disminuye, libera H⁺ para compensar.
El sistema tampón fosfato mantiene el pH celular en 7,2 mediante la reacción reversible entre dihidrógeno fosfato e hidrógeno fosfato. Las grandes cantidades de fosfato en células y huesos lo hacen muy eficaz.
El sistema tampón bicarbonato regula el pH sanguíneo. Cuando aumenta la acidez, se forma CO₂ que se elimina por los pulmones. Cuando disminuye, se toma CO₂ del exterior y el bicarbonato se elimina por los riñones.
💡 Dato médico: Los trastornos del pH sanguíneo (acidosis o alcalosis) pueden ser mortales. Tu cuerpo trabaja constantemente para mantenerlo entre 7,35-7,45.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El agua realiza funciones vitales gracias a sus propiedades únicas. Como disolvente, facilita todas las reacciones químicas del metabolismo mediante solvatación iónica.
Como reactivo, participa directamente en reacciones como la hidrólisis que descompone moléculas complejas. Como transportadora, mueve nutrientes y desechos tanto dentro como fuera de los organismos.
Su función estructural mantiene la forma celular mediante presión osmótica, especialmente en células sin pared rígida. Como amortiguador mecánico, protege articulaciones y órganos del rozamiento y impactos.
La función termorreguladora es crucial para mantener la temperatura corporal estable gracias a su alto calor específico y de vaporización.
💡 Reflexión: Cada vez que bebes agua, no solo te hidratas - estás proporcionando a tu cuerpo el disolvente, reactivo, transportador y termorregulador más eficaz que existe.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las sales minerales son compuestos inorgánicos que desempeñan funciones diferentes según su solubilidad en agua. No las produces, pero son esenciales para vivir.
Las sales insolubles precipitan formando estructuras sólidas de protección y sostén. Los caparazones de moluscos (carbonato cálcico), huesos de vertebrados (fosfatos y carbonatos de calcio) y otolitos del oído (equilibrio) son ejemplos clave.
Las sales solubles se disocian en cationes (Na⁺, K⁺, Mg²⁺, Fe²⁺) y aniones (Cl⁻, PO₄³⁻, CO₃²⁻) que realizan funciones reguladoras como control del pH y activación enzimática.
También tienen funciones específicas fundamentales: Na⁺ y K⁺ transmiten impulsos nerviosos, Ca²⁺ contrae músculos, Mg²⁺ activa enzimas y los fosfatos almacenan energía en forma de ATP.
💡 Consejo de salud: Una dieta equilibrada te aporta todas las sales minerales necesarias. Los suplementos solo son necesarios en casos específicos diagnosticados por profesionales.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
5
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS