¿Te has preguntado alguna vez qué elementos químicos forman tu... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
761
•
Actualizado Apr 22, 2026
•
Miriam
@miriamsm07
¿Te has preguntado alguna vez qué elementos químicos forman tu... Mostrar más










Imagínate que tu cuerpo es como una receta gigante: solo necesitas unos pocos ingredientes principales para "cocinarte". De los 100 elementos químicos que existen, los seres vivos solo usamos unos cuantos, y los llamamos bioelementos.
Los bioelementos primarios son los protagonistas absolutos y representan más del 97% de tu peso. El oxígeno (65%) es el más abundante y el que más "roba" electrones. El carbono (18,5%) es súper especial porque puede formar cuatro enlaces diferentes, creando cadenas largas como collares de átomos que forman todas las moléculas orgánicas de tu cuerpo.
El hidrógeno (9,5%) se une al carbono formando esas cadenas, mientras que el nitrógeno (3,2%) aparece en los aminoácidos y el ADN. El fósforo y el azufre completan el grupo, siendo clave en el ATP (la "batería" de las células) y las proteínas respectivamente.
Dato curioso: El carbono puede formar enlaces simples, dobles o triples, y adoptar formas lineales o circulares. ¡Es como el Lego de la química!

Los bioelementos secundarios como el sodio, potasio, calcio, magnesio y cloro solo representan un 2%, pero son imprescindibles. El potasio es el jefe dentro de las células y necesario para que funcionen tus músculos y nervios. El sodio hace lo mismo pero fuera de las células, mientras que el calcio forma tus huesos y dientes.
Los oligoelementos están en cantidades súper pequeñas (menos del 0,1%) pero son vitales. El hierro de tu sangre, el zinc de tu sistema inmune o el yodo de tu tiroides entran en esta categoría.
Todos estos elementos se combinan para formar biomoléculas. Las hay inorgánicas (como el agua y las sales) que también están en la materia no viva, y orgánicas (glúcidos, lípidos, proteínas, ácidos nucleicos) que solo existen en los seres vivos.
Muchas biomoléculas son macromoléculas: polímeros gigantes hechos de piezas pequeñas llamadas monómeros, como un collar hecho de cuentas idénticas.
Recuerda: Las enzimas y vitaminas son como los "técnicos especialistas" de tu cuerpo: pocas en cantidad pero fundamentales para que todo funcione.

¿Cómo se mantienen unidas las moléculas en tu cuerpo? Existen tres tipos principales de enlaces que debes conocer.
El enlace iónico ocurre cuando un átomo "generoso" (como el sodio) le regala un electrón a otro "egoísta" (como el cloro). Uno queda positivo y otro negativo, y se atraen como imanes opuestos formando sales como el NaCl.
El enlace covalente es más "democrático": los átomos comparten electrones. Puede ser simple, doble o triple según cuántos pares de electrones compartan. Cuando uno de los átomos es más "egoísta" con los electrones, se forma un enlace covalente polar, creando zonas con pequeñas cargas positivas (δ+) y negativas (δ-).
Los puentes de hidrógeno son enlaces débiles que se forman entre las zonas δ+ y δ- de diferentes moléculas. Son como "abrazos suaves" que, aunque individualmente débiles, cuando hay muchos juntos dan gran estabilidad a las moléculas.
Tip de examen: Los enlaces covalentes son los más fuertes, después los iónicos, y por último los puentes de hidrógeno. ¡Pero estos últimos son clave para las propiedades del agua!

Los grupos funcionales son como las "herramientas especializadas" de las biomoléculas. Cada grupo tiene una función específica: el grupo hidroxilo en alcoholes, el carboxilo en ácidos, el amino en aminoácidos, etc.
Para representar las moléculas orgánicas tienes tres opciones. Las fórmulas desarrolladas muestran todos los átomos y enlaces (muy completa pero laboriosa). Las fórmulas semidesarrolladas simplifican agrupando átomos y son las más usadas.
Las fórmulas empíricas solo indican cuántos átomos de cada elemento hay (como C₆H₁₂O₆ para la glucosa), pero no dicen nada sobre la estructura. Es como saber los ingredientes de una receta pero no cómo combinarlos.
Cuando las moléculas son muy complejas, se usan representaciones simplificadas. Por ejemplo, las cadenas largas de los ácidos grasos se dibujan como líneas quebradas.
Importante: Moléculas diferentes pueden tener la misma fórmula empírica pero distinta estructura. ¡La forma importa tanto como la composición!

El agua es literalmente la protagonista de la vida. Está en todas partes: dentro de tus células (citosol), entre las células (líquido intersticial) y en todos los fluidos corporales (sangre, saliva, sudor).
Tu contenido de agua depende de tres factores: la especie (las medusas son 98% agua, las semillas solo 10%), tu edad (un feto de 4 meses es 94% agua, una persona de 65 años solo 56%) y el tipo de tejido (tu plasma sanguíneo es 93% agua, tus dientes solo 10%).
La estructura del agua es clave para entender sus propiedades. Tiene dos hidrógenos y un oxígeno unidos en un ángulo de 104,5°. Aunque la molécula es eléctricamente neutra, es un dipolo: el oxígeno atrae más los electrones (δ-) dejando a los hidrógenos con carga parcial positiva (δ+).
Esta polaridad permite que cada molécula de agua forme puentes de hidrógeno con otras cuatro moléculas, creando una estructura reticular súper cohesionada que explica todas sus propiedades especiales.
Dato fascinante: El agua también forma puentes de hidrógeno con otras moléculas polares como alcoholes y aminoácidos. ¡Por eso puede disolver tantas sustancias!

El carácter dipolar del agua le da propiedades únicas. Primero, es líquida a temperatura ambiente gracias a los puentes de hidrógeno, mientras que moléculas similares como el metano son gases.
Su gran poder de disolución la convierte en el disolvente universal. Disuelve sales (como NaCl) y moléculas polares (azúcares, aminoácidos), permitiendo las reacciones metabólicas y el transporte de nutrientes. Las sustancias polares son hidrófilas (aman el agua), mientras que las apolares son hidrófobas (la repelen).
Las sustancias anfipáticas tienen una parte hidrófila y otra hidrófoba. En agua, se organizan formando micelas (esferas) o bicapas (como las membranas celulares). Es como cuando el aceite forma gotas en el agua.
El elevado calor específico hace que el agua actúe como amortiguador térmico. Para calentarse necesita mucha energía porque parte se usa en romper puentes de hidrógeno. Esto te protege de cambios bruscos de temperatura que dañarían tus proteínas.
Función clave: El agua es incompresible, actuando como esqueleto hidrostático en gusanos y amortiguador mecánico en tus articulaciones.

El elevado calor de vaporización del agua es tu sistema de refrigeración natural. Para evaporarse necesita absorber mucha energía, por eso el sudor te enfría tan eficazmente: cada gota que se evapora se lleva muchísimo calor de tu cuerpo.
La elevada tensión superficial convierte la superficie del agua en una "membrana" resistente. Por eso algunos insectos pueden caminar sobre el agua sin hundirse, y esta propiedad también permite los movimientos dentro de las células.
La capilaridad surge de la cohesión entre moléculas de agua y su adhesión a otras superficies polares. Es fundamental para que las plantas puedan llevar agua desde las raíces hasta las hojas a través de conductos finísimos.
Algo muy peculiar: el hielo es menos denso que el agua líquida, por eso flota. Cuando los lagos se congelan, el hielo de la superficie actúa como aislante térmico, manteniendo el agua del fondo líquida y permitiendo que la vida acuática sobreviva al invierno.
Curiosidad: Sin esta propiedad única del agua, los océanos se congelarían desde el fondo hacia arriba, acabando con la vida marina.

Las sales minerales en tu cuerpo aparecen de tres formas. Precipitadas forman estructuras duras como huesos y dientes. Formando parte de moléculas orgánicas como el hierro en la hemoglobina o el magnesio en la clorofila. Disueltas como iones que regulan el equilibrio osmótico y actúan como tampones.
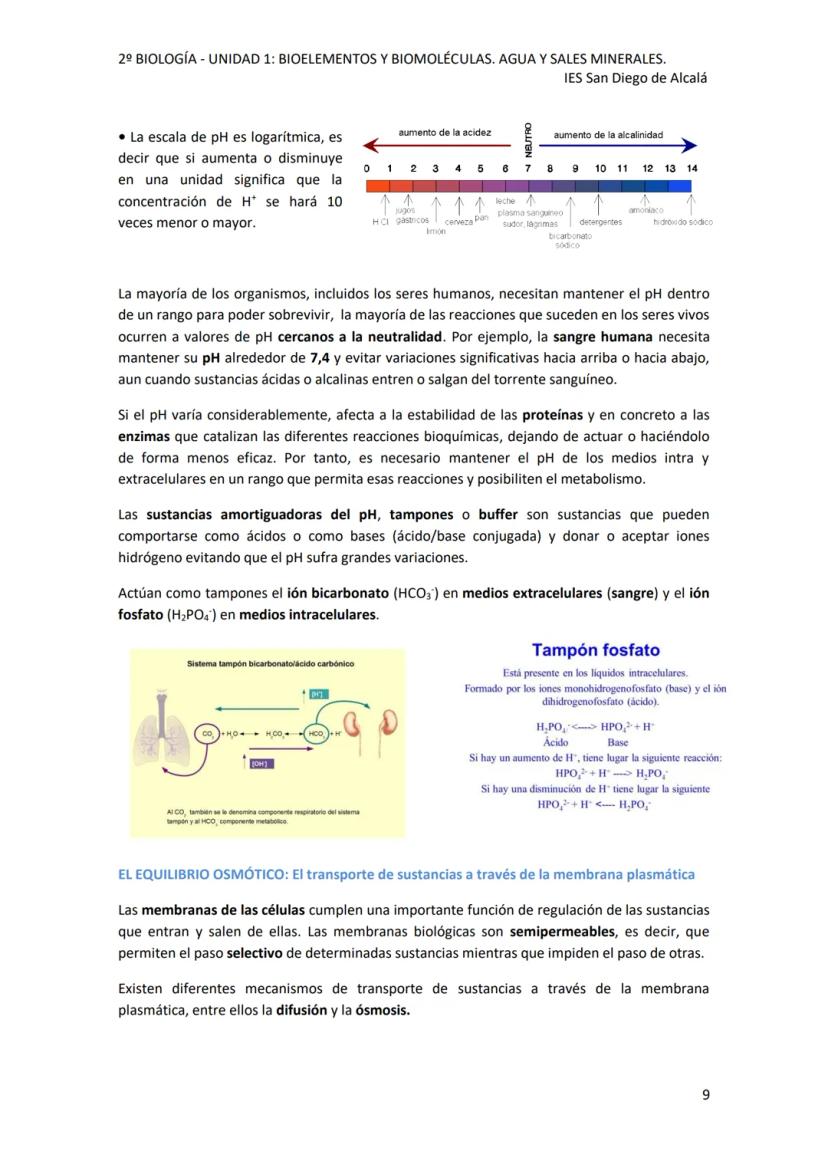
El pH mide la acidez o basicidad de una solución. En agua pura, pH = 7 (neutro). Si pH < 7 es ácido, si pH > 7 es básico. La escala es logarítmica: cada unidad representa un cambio de 10 veces en la concentración de H⁺.
Para sobrevivir necesitas mantener el pH estable. Tu sangre debe estar en 7,4 porque las enzimas (que catalizan todas las reacciones de tu cuerpo) son súper sensibles a cambios de pH. Si varía mucho, dejan de funcionar y tu metabolismo se para.
Los tampones o buffers son sustancias que pueden actuar como ácido o base según se necesite, manteniendo el pH constante. El bicarbonato (HCO₃⁻) regula el pH de tu sangre, mientras que el fosfato (H₂PO₄⁻) lo hace dentro de las células.
Ejemplo práctico: Cuando haces ejercicio produces ácido láctico, pero los tampones de tu sangre evitan que el pH baje peligrosamente.

El sistema tampón fosfato funciona como un regulador automático dentro de tus células. Está formado por dos iones que pueden intercambiar H⁺: si hay exceso de ácido, uno de los iones lo captura; si hay déficit, el otro lo libera. Es como tener un termostato químico.
Las membranas celulares son semipermeables: dejan pasar algunas sustancias pero no otras. Esto es crucial para controlar qué entra y sale de las células.
La difusión ocurre cuando una sustancia se mueve desde donde hay más concentración hacia donde hay menos, hasta equilibrarse. El O₂ y CO₂ difunden libremente entre tus pulmones y sangre.
La ósmosis es la difusión del agua a través de membranas semipermeables. El agua siempre se mueve desde la solución más diluida hacia la más concentrada, intentando igualar las concentraciones. La presión osmótica es la fuerza necesaria para detener este movimiento.
Concepto clave: La ósmosis explica por qué las células se hinchan o encogen según el medio que las rodea. Es fundamental para mantener el equilibrio hídrico.

Según la concentración de solutos, el medio puede ser isotónico (igual concentración que el interior celular), hipertónico (más concentrado) o hipotónico (menos concentrado).
En un medio hipotónico, el agua entra en la célula porque fuera hay menos solutos. Una célula animal se hincharía tanto que podría explotar (lisis celular). Sin embargo, una célula vegetal se vuelve turgente (hinchada pero resistente) gracias a su pared celular que la protege.
En un medio hipertónico, el agua sale de la célula buscando el equilibrio. La célula animal se arruga y puede morir por deshidratación. La célula vegetal pierde turgencia y se "desinfla", pero la pared celular evita que colapse completamente.
Para mantener la vida, las concentraciones dentro y fuera de las células deben estar equilibradas. Tu cuerpo tiene mecanismos sofisticados para mantener este equilibrio osmótico, como los riñones que regulan la concentración de sales en tu sangre.
Aplicación práctica: Por eso cuando estás deshidratado no basta con beber agua, necesitas reponer también las sales perdidas. ¡De ahí las bebidas isotónicas!
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
Miriam
@miriamsm07
¿Te has preguntado alguna vez qué elementos químicos forman tu cuerpo y por qué el agua es tan importante para la vida? En esta unidad vas a descubrir los componentes básicos de todos los seres vivos y entender por qué... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Imagínate que tu cuerpo es como una receta gigante: solo necesitas unos pocos ingredientes principales para "cocinarte". De los 100 elementos químicos que existen, los seres vivos solo usamos unos cuantos, y los llamamos bioelementos.
Los bioelementos primarios son los protagonistas absolutos y representan más del 97% de tu peso. El oxígeno (65%) es el más abundante y el que más "roba" electrones. El carbono (18,5%) es súper especial porque puede formar cuatro enlaces diferentes, creando cadenas largas como collares de átomos que forman todas las moléculas orgánicas de tu cuerpo.
El hidrógeno (9,5%) se une al carbono formando esas cadenas, mientras que el nitrógeno (3,2%) aparece en los aminoácidos y el ADN. El fósforo y el azufre completan el grupo, siendo clave en el ATP (la "batería" de las células) y las proteínas respectivamente.
Dato curioso: El carbono puede formar enlaces simples, dobles o triples, y adoptar formas lineales o circulares. ¡Es como el Lego de la química!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los bioelementos secundarios como el sodio, potasio, calcio, magnesio y cloro solo representan un 2%, pero son imprescindibles. El potasio es el jefe dentro de las células y necesario para que funcionen tus músculos y nervios. El sodio hace lo mismo pero fuera de las células, mientras que el calcio forma tus huesos y dientes.
Los oligoelementos están en cantidades súper pequeñas (menos del 0,1%) pero son vitales. El hierro de tu sangre, el zinc de tu sistema inmune o el yodo de tu tiroides entran en esta categoría.
Todos estos elementos se combinan para formar biomoléculas. Las hay inorgánicas (como el agua y las sales) que también están en la materia no viva, y orgánicas (glúcidos, lípidos, proteínas, ácidos nucleicos) que solo existen en los seres vivos.
Muchas biomoléculas son macromoléculas: polímeros gigantes hechos de piezas pequeñas llamadas monómeros, como un collar hecho de cuentas idénticas.
Recuerda: Las enzimas y vitaminas son como los "técnicos especialistas" de tu cuerpo: pocas en cantidad pero fundamentales para que todo funcione.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Cómo se mantienen unidas las moléculas en tu cuerpo? Existen tres tipos principales de enlaces que debes conocer.
El enlace iónico ocurre cuando un átomo "generoso" (como el sodio) le regala un electrón a otro "egoísta" (como el cloro). Uno queda positivo y otro negativo, y se atraen como imanes opuestos formando sales como el NaCl.
El enlace covalente es más "democrático": los átomos comparten electrones. Puede ser simple, doble o triple según cuántos pares de electrones compartan. Cuando uno de los átomos es más "egoísta" con los electrones, se forma un enlace covalente polar, creando zonas con pequeñas cargas positivas (δ+) y negativas (δ-).
Los puentes de hidrógeno son enlaces débiles que se forman entre las zonas δ+ y δ- de diferentes moléculas. Son como "abrazos suaves" que, aunque individualmente débiles, cuando hay muchos juntos dan gran estabilidad a las moléculas.
Tip de examen: Los enlaces covalentes son los más fuertes, después los iónicos, y por último los puentes de hidrógeno. ¡Pero estos últimos son clave para las propiedades del agua!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los grupos funcionales son como las "herramientas especializadas" de las biomoléculas. Cada grupo tiene una función específica: el grupo hidroxilo en alcoholes, el carboxilo en ácidos, el amino en aminoácidos, etc.
Para representar las moléculas orgánicas tienes tres opciones. Las fórmulas desarrolladas muestran todos los átomos y enlaces (muy completa pero laboriosa). Las fórmulas semidesarrolladas simplifican agrupando átomos y son las más usadas.
Las fórmulas empíricas solo indican cuántos átomos de cada elemento hay (como C₆H₁₂O₆ para la glucosa), pero no dicen nada sobre la estructura. Es como saber los ingredientes de una receta pero no cómo combinarlos.
Cuando las moléculas son muy complejas, se usan representaciones simplificadas. Por ejemplo, las cadenas largas de los ácidos grasos se dibujan como líneas quebradas.
Importante: Moléculas diferentes pueden tener la misma fórmula empírica pero distinta estructura. ¡La forma importa tanto como la composición!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El agua es literalmente la protagonista de la vida. Está en todas partes: dentro de tus células (citosol), entre las células (líquido intersticial) y en todos los fluidos corporales (sangre, saliva, sudor).
Tu contenido de agua depende de tres factores: la especie (las medusas son 98% agua, las semillas solo 10%), tu edad (un feto de 4 meses es 94% agua, una persona de 65 años solo 56%) y el tipo de tejido (tu plasma sanguíneo es 93% agua, tus dientes solo 10%).
La estructura del agua es clave para entender sus propiedades. Tiene dos hidrógenos y un oxígeno unidos en un ángulo de 104,5°. Aunque la molécula es eléctricamente neutra, es un dipolo: el oxígeno atrae más los electrones (δ-) dejando a los hidrógenos con carga parcial positiva (δ+).
Esta polaridad permite que cada molécula de agua forme puentes de hidrógeno con otras cuatro moléculas, creando una estructura reticular súper cohesionada que explica todas sus propiedades especiales.
Dato fascinante: El agua también forma puentes de hidrógeno con otras moléculas polares como alcoholes y aminoácidos. ¡Por eso puede disolver tantas sustancias!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El carácter dipolar del agua le da propiedades únicas. Primero, es líquida a temperatura ambiente gracias a los puentes de hidrógeno, mientras que moléculas similares como el metano son gases.
Su gran poder de disolución la convierte en el disolvente universal. Disuelve sales (como NaCl) y moléculas polares (azúcares, aminoácidos), permitiendo las reacciones metabólicas y el transporte de nutrientes. Las sustancias polares son hidrófilas (aman el agua), mientras que las apolares son hidrófobas (la repelen).
Las sustancias anfipáticas tienen una parte hidrófila y otra hidrófoba. En agua, se organizan formando micelas (esferas) o bicapas (como las membranas celulares). Es como cuando el aceite forma gotas en el agua.
El elevado calor específico hace que el agua actúe como amortiguador térmico. Para calentarse necesita mucha energía porque parte se usa en romper puentes de hidrógeno. Esto te protege de cambios bruscos de temperatura que dañarían tus proteínas.
Función clave: El agua es incompresible, actuando como esqueleto hidrostático en gusanos y amortiguador mecánico en tus articulaciones.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El elevado calor de vaporización del agua es tu sistema de refrigeración natural. Para evaporarse necesita absorber mucha energía, por eso el sudor te enfría tan eficazmente: cada gota que se evapora se lleva muchísimo calor de tu cuerpo.
La elevada tensión superficial convierte la superficie del agua en una "membrana" resistente. Por eso algunos insectos pueden caminar sobre el agua sin hundirse, y esta propiedad también permite los movimientos dentro de las células.
La capilaridad surge de la cohesión entre moléculas de agua y su adhesión a otras superficies polares. Es fundamental para que las plantas puedan llevar agua desde las raíces hasta las hojas a través de conductos finísimos.
Algo muy peculiar: el hielo es menos denso que el agua líquida, por eso flota. Cuando los lagos se congelan, el hielo de la superficie actúa como aislante térmico, manteniendo el agua del fondo líquida y permitiendo que la vida acuática sobreviva al invierno.
Curiosidad: Sin esta propiedad única del agua, los océanos se congelarían desde el fondo hacia arriba, acabando con la vida marina.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las sales minerales en tu cuerpo aparecen de tres formas. Precipitadas forman estructuras duras como huesos y dientes. Formando parte de moléculas orgánicas como el hierro en la hemoglobina o el magnesio en la clorofila. Disueltas como iones que regulan el equilibrio osmótico y actúan como tampones.
El pH mide la acidez o basicidad de una solución. En agua pura, pH = 7 (neutro). Si pH < 7 es ácido, si pH > 7 es básico. La escala es logarítmica: cada unidad representa un cambio de 10 veces en la concentración de H⁺.
Para sobrevivir necesitas mantener el pH estable. Tu sangre debe estar en 7,4 porque las enzimas (que catalizan todas las reacciones de tu cuerpo) son súper sensibles a cambios de pH. Si varía mucho, dejan de funcionar y tu metabolismo se para.
Los tampones o buffers son sustancias que pueden actuar como ácido o base según se necesite, manteniendo el pH constante. El bicarbonato (HCO₃⁻) regula el pH de tu sangre, mientras que el fosfato (H₂PO₄⁻) lo hace dentro de las células.
Ejemplo práctico: Cuando haces ejercicio produces ácido láctico, pero los tampones de tu sangre evitan que el pH baje peligrosamente.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El sistema tampón fosfato funciona como un regulador automático dentro de tus células. Está formado por dos iones que pueden intercambiar H⁺: si hay exceso de ácido, uno de los iones lo captura; si hay déficit, el otro lo libera. Es como tener un termostato químico.
Las membranas celulares son semipermeables: dejan pasar algunas sustancias pero no otras. Esto es crucial para controlar qué entra y sale de las células.
La difusión ocurre cuando una sustancia se mueve desde donde hay más concentración hacia donde hay menos, hasta equilibrarse. El O₂ y CO₂ difunden libremente entre tus pulmones y sangre.
La ósmosis es la difusión del agua a través de membranas semipermeables. El agua siempre se mueve desde la solución más diluida hacia la más concentrada, intentando igualar las concentraciones. La presión osmótica es la fuerza necesaria para detener este movimiento.
Concepto clave: La ósmosis explica por qué las células se hinchan o encogen según el medio que las rodea. Es fundamental para mantener el equilibrio hídrico.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Según la concentración de solutos, el medio puede ser isotónico (igual concentración que el interior celular), hipertónico (más concentrado) o hipotónico (menos concentrado).
En un medio hipotónico, el agua entra en la célula porque fuera hay menos solutos. Una célula animal se hincharía tanto que podría explotar (lisis celular). Sin embargo, una célula vegetal se vuelve turgente (hinchada pero resistente) gracias a su pared celular que la protege.
En un medio hipertónico, el agua sale de la célula buscando el equilibrio. La célula animal se arruga y puede morir por deshidratación. La célula vegetal pierde turgencia y se "desinfla", pero la pared celular evita que colapse completamente.
Para mantener la vida, las concentraciones dentro y fuera de las células deben estar equilibradas. Tu cuerpo tiene mecanismos sofisticados para mantener este equilibrio osmótico, como los riñones que regulan la concentración de sales en tu sangre.
Aplicación práctica: Por eso cuando estás deshidratado no basta con beber agua, necesitas reponer también las sales perdidas. ¡De ahí las bebidas isotónicas!
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
10
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Flashcards Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Está app es muy buena, tiene apuntes que son de mucha ayuda y su IA es fantástica, te explica a la perfección y muy fácil de entender lo que necesites, te ayuda con los deberes, te hace esquemas... en definitiva es una muy buena opción!
Sophia
usuario de Android
Me encanta!!! Me resuelve todo con detalle y me da la explicación correcta. Tiene un montón de funciones, ami me ha ido genial!! Os la recomiendo!!!
Marta
usuaria de Android
La uso casi diariamente, sirve para todas las asignaturas. Yo, por ejemplo la utilizo más en inglés porque se me da bastante mal, ¡Todas las respuestas están correctas! Consta con personas reales que suben sus apuntes y IA para que puedas hacer los deberes muchísimo más fácil, la recomiendo.
Izan
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Esto no es como Chatgpt, es MUCHISMO MEJOR, te hace unos resúmenes espectaculares y gracias a esta app pase de sacar 5-6 a sacar 8-9.
Julyana
usuaria de Android
Es la mejor aplicación del mundo, la uso para revisar los deberes a mi hijo.
Javier
usuario de Android
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Erick
usuario de Android
Me me encanta esta app, todo lo que tiene es de calidad ya que antes de ser publicado es revisado por un equipo de profesionales. Me ha ido genial esta aplicación ya que gracias a ella puedo estudiar mucho mejor, sin tener que agobiarme porque mi profesor no ha hecho teoría o porque no entiendo su teoría. Le doy un 10 de 10!
Mar
usuaria de iOS