¿Sabías que los átomos que forman tu cuerpo se crearon... Mostrar más
Bioelementos y Biomoléculas Inorgánicas: Agua y Sales Minerales







El Origen Estelar de la Vida
Los bioelementos que forman nuestro cuerpo provienen de las reacciones de fusión nuclear que ocurren en las estrellas. Cuando el hidrógeno y helio se fusionan en los núcleos estelares, se crean todos los demás elementos que después encontramos en la Tierra.
Estos elementos aparecen en diferentes proporciones en los seres vivos comparado con la corteza terrestre. La razón es simple: los organismos "eligen" elementos con bajo número atómico y 4 o más electrones en su última capa, porque pueden formar enlaces covalentes estables.
El carbono es el rey de los bioelementos. Puede formar 4 enlaces covalentes (simples, dobles o triples) y crear largas cadenas que forman el esqueleto de las macromoléculas. A estas cadenas se les pueden unir grupos funcionales que les dan propiedades específicas.
Los grupos funcionales más importantes incluyen: hidroxilo en alcoholes, carbonilo en cetonas y aldehídos, carboxilo en ácidos, amino en aminoácidos, y fosfato en nucleótidos.
Dato clave: Los elementos primarios (C, H, O, N, P, S) constituyen el 96% de la materia viva.

Clasificación de Bioelementos y Biomoléculas
Los bioelementos se clasifican según su abundancia: primarios (96% de la materia viva), secundarios (3,3% como iones necesarios para procesos fisiológicos como Ca²⁺ para contracción muscular), y oligoelementos (menos del 0,1% pero esenciales como Fe en hemoglobina).
Las biomoléculas son los componentes que forman los seres vivos y se pueden separar por métodos físicos como centrifugación o cromatografía. Se dividen en inorgánicas (agua, sales minerales) y orgánicas (glúcidos, lípidos, proteínas, ácidos nucleicos).
Los enlaces químicos mantienen unidas estas moléculas. Los enlaces iónicos se forman entre átomos con cargas opuestas, mientras que los enlaces covalentes comparten electrones y pueden ser polares o apolares según la electronegatividad.
Los enlaces intermoleculares como los puentes de hidrógeno y las fuerzas de Van der Waals son más débiles pero cruciales para la estructura de las biomoléculas.
Recuerda: Los enlaces covalentes polares crean moléculas con cargas parciales, fundamental para las propiedades del agua.

El Agua: La Molécula de la Vida
El agua es la biomolécula más abundante, representando desde un 10-20% en semillas hasta un 95% en embriones. Su estructura angular (104,5°) y su carácter polar la convierten en un dipolo eléctrico capaz de formar hasta 4 puentes de hidrógeno por molécula.
Esta capacidad de formar puentes de hidrógeno le confiere propiedades únicas: elevada cohesión molecular (es incompresible), alta fuerza de adhesión (permite la capilaridad), y elevada tensión superficial (forma gotas y permite que algunos insectos caminen sobre ella).
El agua también tiene un elevado calor específico y calor de vaporización, lo que significa que puede absorber mucha energía sin cambiar bruscamente de temperatura. Esto es crucial para la termorregulación de los organismos.
Una propiedad sorprendente es que el hielo es menos denso que el agua líquida, por lo que flota. Esto permite la vida acuática en invierno, ya que los lagos no se congelan completamente.
Dato curioso: Solo 1 de cada 10⁷ moléculas de agua está ionizada, manteniendo un pH neutro esencial para la vida.

Propiedades y Funciones del Agua
El poder disolvente del agua es excepcional para moléculas polares e iónicas. Las moléculas que se disuelven en agua son hidrófilas, las que no se disuelven son hidrófobas, y las que tienen partes polares y apolares son anfipáticas.
Las funciones del agua son múltiples y vitales. Como medio de transporte, constituye el 90% del plasma sanguíneo y permite el movimiento de sustancias. En procesos bioquímicos, sirve como medio donde ocurren las reacciones y participa directamente en hidrólisis y fotosíntesis.
Su función termorreguladora es crucial: amortigua cambios bruscos de temperatura y permite la refrigeración mediante el sudor. Como amortiguador mecánico, protege órganos en líquidos como el sinovial, cefalorraquídeo y amniótico.
Las interacciones hidrofóbicas determinan la formación de estructuras biológicas importantes como membranas celulares, micelas digestivas y el plegamiento correcto de proteínas.
Aplicación práctica: El sudor funciona como sistema de refrigeración porque el agua necesita mucha energía para evaporarse.

Sales Minerales: Los Reguladores Celulares
Las sales minerales se encuentran precipitadas (formando estructuras sólidas como huesos) o disueltas como iones (cationes Na⁺, K⁺, Ca²⁺ y aniones Cl⁻, HCO₃⁻). Son fundamentales para mantener el equilibrio celular.
Su función más crítica es regular la presión osmótica. Las células deben mantenerse en un medio isotónico para funcionar correctamente. En medios hipertónicos pierden agua , mientras que en medios hipotónicos la absorben excesivamente .
Las sales actúan como sistemas tampón para regular el pH. El sistema bicarbonato funciona en la sangre , mientras que el sistema fosfato opera dentro de las células .
Además, muchos iones tienen funciones específicas: Ca²⁺ para contracción muscular, Fe²⁺ para transporte de oxígeno, Mg²⁺ para fotosíntesis, y Na⁺/K⁺ para impulsos nerviosos a través de la bomba sodio-potasio.
Concepto clave: Los sistemas tampón mantienen el pH estable desplazando el equilibrio químico según la concentración de H⁺.

Funciones Especializadas y Dispersiones Coloidales
Las sales minerales tienen roles específicos en procesos vitales. El intercambio Na⁺/K⁺ genera potenciales eléctricos necesarios para impulsos nerviosos y contracción muscular. El Ca²⁺ no solo participa en la contracción sino también en la coagulación sanguínea.
Las dispersiones coloidales son mezclas donde el soluto tiene gran peso molecular, como la sangre o la leche. Pueden estar en estado sol (líquido) o gel (semisólido), y las sales minerales ayudan a estabilizar estas dispersiones.
En el citoplasma celular, el cambio de gel a sol permite el movimiento. El ectoplasma (cerca de la membrana) está en gel, mientras el endoplasma (interior) está en sol. Este cambio se debe a la polimerización/despolimerización de proteínas, proceso donde el Ca²⁺ juega un papel crucial.
Los oligoelementos como Mn²⁺, Zn²⁺ y Cu²⁺ actúan como cofactores enzimáticos, siendo esenciales para reacciones específicas aunque estén en cantidades mínimas.
Ejemplo práctico: El movimiento de las amebas ocurre por el cambio sol-gel del citoplasma, regulado por iones de calcio.
Pigmentos Fotosintéticos y Cadena de Transporte
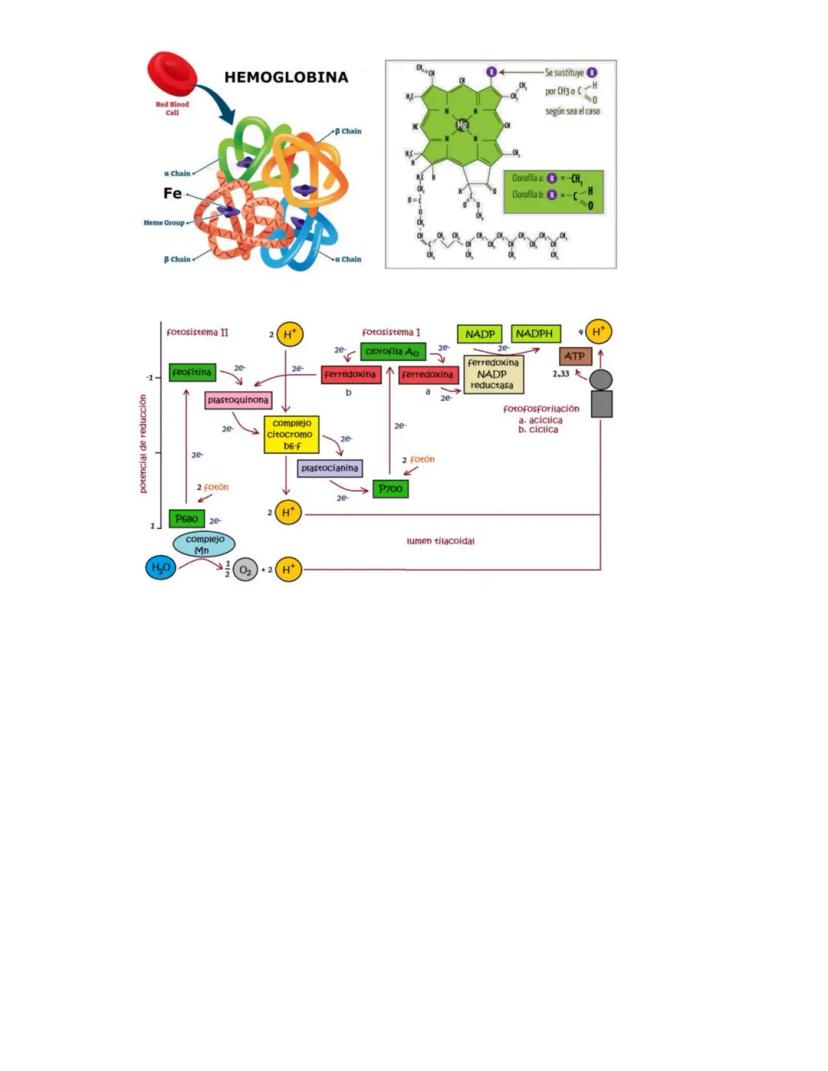
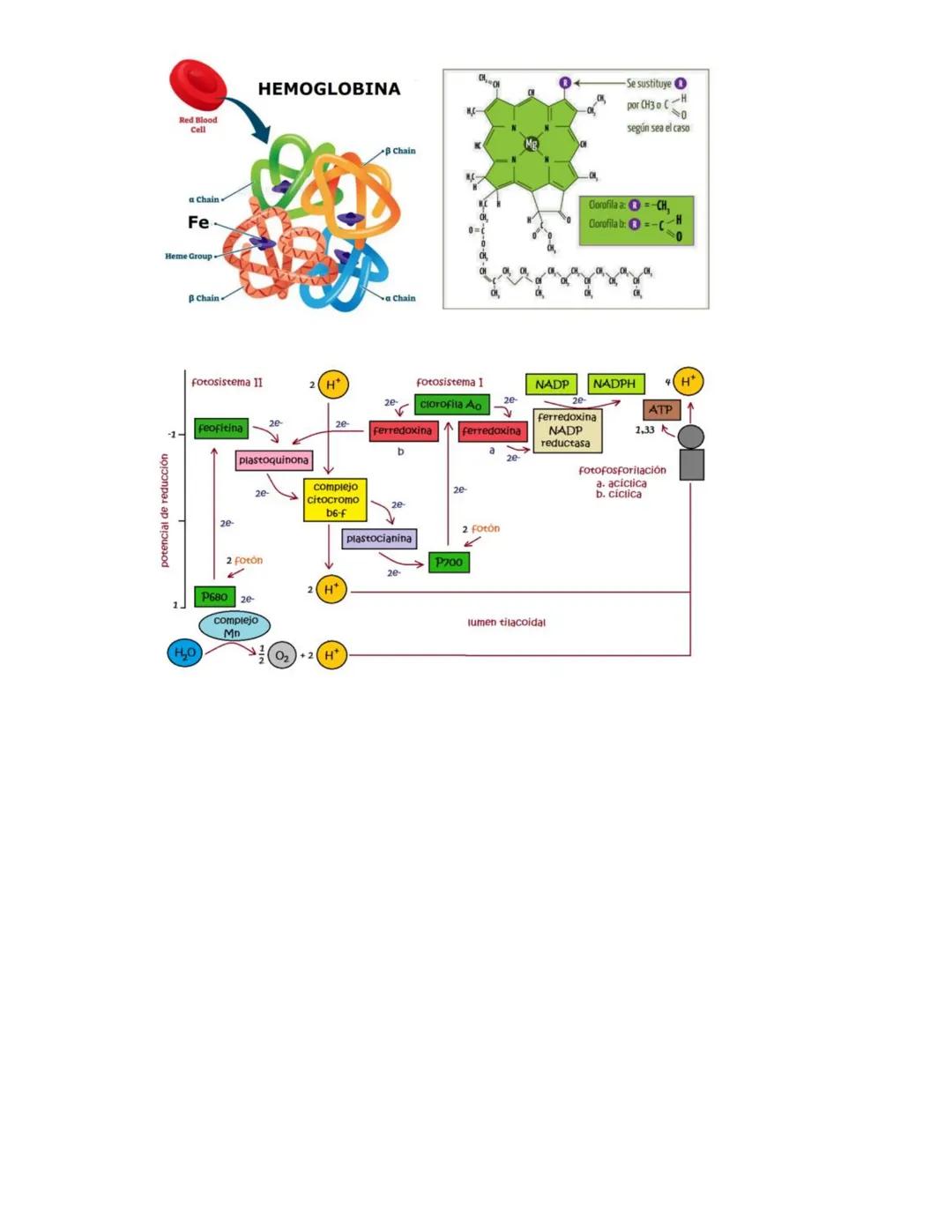
La clorofila y la hemoglobina son ejemplos perfectos de cómo los bioelementos forman estructuras complejas. Ambas tienen estructuras similares con un ion metálico central: Mg²⁺ en clorofila y Fe²⁺ en hemoglobina.
En la fotosíntesis, existen dos fotosistemas (I y II) que trabajan en conjunto. El fotosistema II contiene P680 y el fotosistema I contiene P700, números que indican la longitud de onda de absorción máxima.
La cadena de transporte de electrones en fotosíntesis incluye componentes como plastoquinona, citocromo b₆-f, y plastocianina. Los electrones fluyen desde el agua hasta el NADP⁺, generando ATP y NADPH necesarios para la síntesis de glucosa.
El complejo de manganeso en el fotosistema II es crucial para la fotólisis del agua, liberando oxígeno como subproducto. Este proceso es fundamental para mantener la atmósfera oxigenada que permite la vida aeróbica.
Conexión importante: Sin el Mg²⁺ en la clorofila, las plantas no podrían captar energía luminosa y no existiría la fotosíntesis.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: elementos biológicos
9Apuntes de bioelementos y biomoléculas
Apuntes de bioelementos y biomoléculas
bioelementos agua y sales minerales
agua y sales minerales
BG: bloque 1 pt.1
Agua, ósmosis, sales minerales y bioelementos.
biomoléculas y bioelementos
esquema de conceptos
Bioelementos, agua y sales minerales
Bioelementos, agua y sales minerales
Tema 1 Biología
Biología tema 1: los bioelementos
bioelementos. Agua y sales
Tema de primero y segundo de bachillerato que habla acerca del agua y las sales minerales
T1 - Bioelementos
tema 1 Bioelementos 2° de bachillerato PAU
Tema 1 - los bioelementos y biomoléculas
Trata lo que son los bioelementos y las biomoléculas y sus propiedades correspondientes
Contenidos más populares de Biología
9Descubriendo la vida: Flashcards de Biología
Aprende sobre los fundamentos de la biología con esta colección de flashcards interactivos. ¡Explora los conceptos clave y amplía tus conocimientos sobre la vida en este emocionante viaje de aprendizaje!
Replicación, transcripción y traducción
Esquema del tema de flujo de información genética del bloque de Biología Molecular
Fotosíntesis
Conceptos básicos y reacciones químicas que se producen
Anabolismo y Catabolismo
amabolismo y catabolismo
GENÉTICA MOLECULAR
Genética molecular 2 bachillerato y PAU
Catabolismo y anabolismo
Apuntes “esquematizados” con imágenes y visual
las plantas 🌳🌿
el reino de las plantas
Metabolismo
Apuntes de metabolismo de segundo de bachillerato (biología). También recomiendo acompañar el estudio de este tema con el esquema que he subido para entenderlo mejor.
METABOLISMO CELULAR (CATABOLISMO + ANABOLISMO)
Apuntes completos de catabolismo y anabolismo de 2 bach
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Bioelementos y Biomoléculas Inorgánicas: Agua y Sales Minerales
¿Sabías que los átomos que forman tu cuerpo se crearon en el interior de las estrellas hace millones de años? Los bioelementos son esos elementos químicos fundamentales que constituyen todos los seres vivos, desde las plantas hasta nosotros mismos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El Origen Estelar de la Vida
Los bioelementos que forman nuestro cuerpo provienen de las reacciones de fusión nuclear que ocurren en las estrellas. Cuando el hidrógeno y helio se fusionan en los núcleos estelares, se crean todos los demás elementos que después encontramos en la Tierra.
Estos elementos aparecen en diferentes proporciones en los seres vivos comparado con la corteza terrestre. La razón es simple: los organismos "eligen" elementos con bajo número atómico y 4 o más electrones en su última capa, porque pueden formar enlaces covalentes estables.
El carbono es el rey de los bioelementos. Puede formar 4 enlaces covalentes (simples, dobles o triples) y crear largas cadenas que forman el esqueleto de las macromoléculas. A estas cadenas se les pueden unir grupos funcionales que les dan propiedades específicas.
Los grupos funcionales más importantes incluyen: hidroxilo en alcoholes, carbonilo en cetonas y aldehídos, carboxilo en ácidos, amino en aminoácidos, y fosfato en nucleótidos.
Dato clave: Los elementos primarios (C, H, O, N, P, S) constituyen el 96% de la materia viva.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Clasificación de Bioelementos y Biomoléculas
Los bioelementos se clasifican según su abundancia: primarios (96% de la materia viva), secundarios (3,3% como iones necesarios para procesos fisiológicos como Ca²⁺ para contracción muscular), y oligoelementos (menos del 0,1% pero esenciales como Fe en hemoglobina).
Las biomoléculas son los componentes que forman los seres vivos y se pueden separar por métodos físicos como centrifugación o cromatografía. Se dividen en inorgánicas (agua, sales minerales) y orgánicas (glúcidos, lípidos, proteínas, ácidos nucleicos).
Los enlaces químicos mantienen unidas estas moléculas. Los enlaces iónicos se forman entre átomos con cargas opuestas, mientras que los enlaces covalentes comparten electrones y pueden ser polares o apolares según la electronegatividad.
Los enlaces intermoleculares como los puentes de hidrógeno y las fuerzas de Van der Waals son más débiles pero cruciales para la estructura de las biomoléculas.
Recuerda: Los enlaces covalentes polares crean moléculas con cargas parciales, fundamental para las propiedades del agua.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
El Agua: La Molécula de la Vida
El agua es la biomolécula más abundante, representando desde un 10-20% en semillas hasta un 95% en embriones. Su estructura angular (104,5°) y su carácter polar la convierten en un dipolo eléctrico capaz de formar hasta 4 puentes de hidrógeno por molécula.
Esta capacidad de formar puentes de hidrógeno le confiere propiedades únicas: elevada cohesión molecular (es incompresible), alta fuerza de adhesión (permite la capilaridad), y elevada tensión superficial (forma gotas y permite que algunos insectos caminen sobre ella).
El agua también tiene un elevado calor específico y calor de vaporización, lo que significa que puede absorber mucha energía sin cambiar bruscamente de temperatura. Esto es crucial para la termorregulación de los organismos.
Una propiedad sorprendente es que el hielo es menos denso que el agua líquida, por lo que flota. Esto permite la vida acuática en invierno, ya que los lagos no se congelan completamente.
Dato curioso: Solo 1 de cada 10⁷ moléculas de agua está ionizada, manteniendo un pH neutro esencial para la vida.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades y Funciones del Agua
El poder disolvente del agua es excepcional para moléculas polares e iónicas. Las moléculas que se disuelven en agua son hidrófilas, las que no se disuelven son hidrófobas, y las que tienen partes polares y apolares son anfipáticas.
Las funciones del agua son múltiples y vitales. Como medio de transporte, constituye el 90% del plasma sanguíneo y permite el movimiento de sustancias. En procesos bioquímicos, sirve como medio donde ocurren las reacciones y participa directamente en hidrólisis y fotosíntesis.
Su función termorreguladora es crucial: amortigua cambios bruscos de temperatura y permite la refrigeración mediante el sudor. Como amortiguador mecánico, protege órganos en líquidos como el sinovial, cefalorraquídeo y amniótico.
Las interacciones hidrofóbicas determinan la formación de estructuras biológicas importantes como membranas celulares, micelas digestivas y el plegamiento correcto de proteínas.
Aplicación práctica: El sudor funciona como sistema de refrigeración porque el agua necesita mucha energía para evaporarse.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Sales Minerales: Los Reguladores Celulares
Las sales minerales se encuentran precipitadas (formando estructuras sólidas como huesos) o disueltas como iones (cationes Na⁺, K⁺, Ca²⁺ y aniones Cl⁻, HCO₃⁻). Son fundamentales para mantener el equilibrio celular.
Su función más crítica es regular la presión osmótica. Las células deben mantenerse en un medio isotónico para funcionar correctamente. En medios hipertónicos pierden agua , mientras que en medios hipotónicos la absorben excesivamente .
Las sales actúan como sistemas tampón para regular el pH. El sistema bicarbonato funciona en la sangre , mientras que el sistema fosfato opera dentro de las células .
Además, muchos iones tienen funciones específicas: Ca²⁺ para contracción muscular, Fe²⁺ para transporte de oxígeno, Mg²⁺ para fotosíntesis, y Na⁺/K⁺ para impulsos nerviosos a través de la bomba sodio-potasio.
Concepto clave: Los sistemas tampón mantienen el pH estable desplazando el equilibrio químico según la concentración de H⁺.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Funciones Especializadas y Dispersiones Coloidales
Las sales minerales tienen roles específicos en procesos vitales. El intercambio Na⁺/K⁺ genera potenciales eléctricos necesarios para impulsos nerviosos y contracción muscular. El Ca²⁺ no solo participa en la contracción sino también en la coagulación sanguínea.
Las dispersiones coloidales son mezclas donde el soluto tiene gran peso molecular, como la sangre o la leche. Pueden estar en estado sol (líquido) o gel (semisólido), y las sales minerales ayudan a estabilizar estas dispersiones.
En el citoplasma celular, el cambio de gel a sol permite el movimiento. El ectoplasma (cerca de la membrana) está en gel, mientras el endoplasma (interior) está en sol. Este cambio se debe a la polimerización/despolimerización de proteínas, proceso donde el Ca²⁺ juega un papel crucial.
Los oligoelementos como Mn²⁺, Zn²⁺ y Cu²⁺ actúan como cofactores enzimáticos, siendo esenciales para reacciones específicas aunque estén en cantidades mínimas.
Ejemplo práctico: El movimiento de las amebas ocurre por el cambio sol-gel del citoplasma, regulado por iones de calcio.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pigmentos Fotosintéticos y Cadena de Transporte
La clorofila y la hemoglobina son ejemplos perfectos de cómo los bioelementos forman estructuras complejas. Ambas tienen estructuras similares con un ion metálico central: Mg²⁺ en clorofila y Fe²⁺ en hemoglobina.
En la fotosíntesis, existen dos fotosistemas (I y II) que trabajan en conjunto. El fotosistema II contiene P680 y el fotosistema I contiene P700, números que indican la longitud de onda de absorción máxima.
La cadena de transporte de electrones en fotosíntesis incluye componentes como plastoquinona, citocromo b₆-f, y plastocianina. Los electrones fluyen desde el agua hasta el NADP⁺, generando ATP y NADPH necesarios para la síntesis de glucosa.
El complejo de manganeso en el fotosistema II es crucial para la fotólisis del agua, liberando oxígeno como subproducto. Este proceso es fundamental para mantener la atmósfera oxigenada que permite la vida aeróbica.
Conexión importante: Sin el Mg²⁺ en la clorofila, las plantas no podrían captar energía luminosa y no existiría la fotosíntesis.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
Sí, tienes acceso gratuito a los contenidos de la aplicación y a nuestro compañero de IA. Para desbloquear determinadas funciones de la aplicación, puedes adquirir Knowunity Pro.
Contenido similar
Contenidos más populares: elementos biológicos
9Apuntes de bioelementos y biomoléculas
Apuntes de bioelementos y biomoléculas
bioelementos agua y sales minerales
agua y sales minerales
BG: bloque 1 pt.1
Agua, ósmosis, sales minerales y bioelementos.
biomoléculas y bioelementos
esquema de conceptos
Bioelementos, agua y sales minerales
Bioelementos, agua y sales minerales
Tema 1 Biología
Biología tema 1: los bioelementos
bioelementos. Agua y sales
Tema de primero y segundo de bachillerato que habla acerca del agua y las sales minerales
T1 - Bioelementos
tema 1 Bioelementos 2° de bachillerato PAU
Tema 1 - los bioelementos y biomoléculas
Trata lo que son los bioelementos y las biomoléculas y sus propiedades correspondientes
Contenidos más populares de Biología
9Descubriendo la vida: Flashcards de Biología
Aprende sobre los fundamentos de la biología con esta colección de flashcards interactivos. ¡Explora los conceptos clave y amplía tus conocimientos sobre la vida en este emocionante viaje de aprendizaje!
Replicación, transcripción y traducción
Esquema del tema de flujo de información genética del bloque de Biología Molecular
Fotosíntesis
Conceptos básicos y reacciones químicas que se producen
Anabolismo y Catabolismo
amabolismo y catabolismo
GENÉTICA MOLECULAR
Genética molecular 2 bachillerato y PAU
Catabolismo y anabolismo
Apuntes “esquematizados” con imágenes y visual
las plantas 🌳🌿
el reino de las plantas
Metabolismo
Apuntes de metabolismo de segundo de bachillerato (biología). También recomiendo acompañar el estudio de este tema con el esquema que he subido para entenderlo mejor.
METABOLISMO CELULAR (CATABOLISMO + ANABOLISMO)
Apuntes completos de catabolismo y anabolismo de 2 bach
Contenidos más populares
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encanta - y a tí también.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.